Clear Sky Science · es
Las células T diseñadas contra el complejo Dickkopf-1-A2 pueden usarse para tratar cánceres sólidos y hematológicos HLA-A2+
Nueva esperanza para cánceres difíciles de tratar
Muchas inmunoterapias recientes potentes funcionan bien en cánceres de la sangre, pero tropiezan frente a tumores sólidos como los de páncreas, pulmón y mama. Este estudio presenta una célula T especialmente diseñada que se dirige a una “bandera” molecular presente en una amplia variedad de cánceres pero en gran medida ausente en los tejidos normales, ofreciendo la posibilidad de un tratamiento único que podría atacar de forma segura tanto tumores hematológicos como sólidos en pacientes que poseen un tipo inmunitario común.
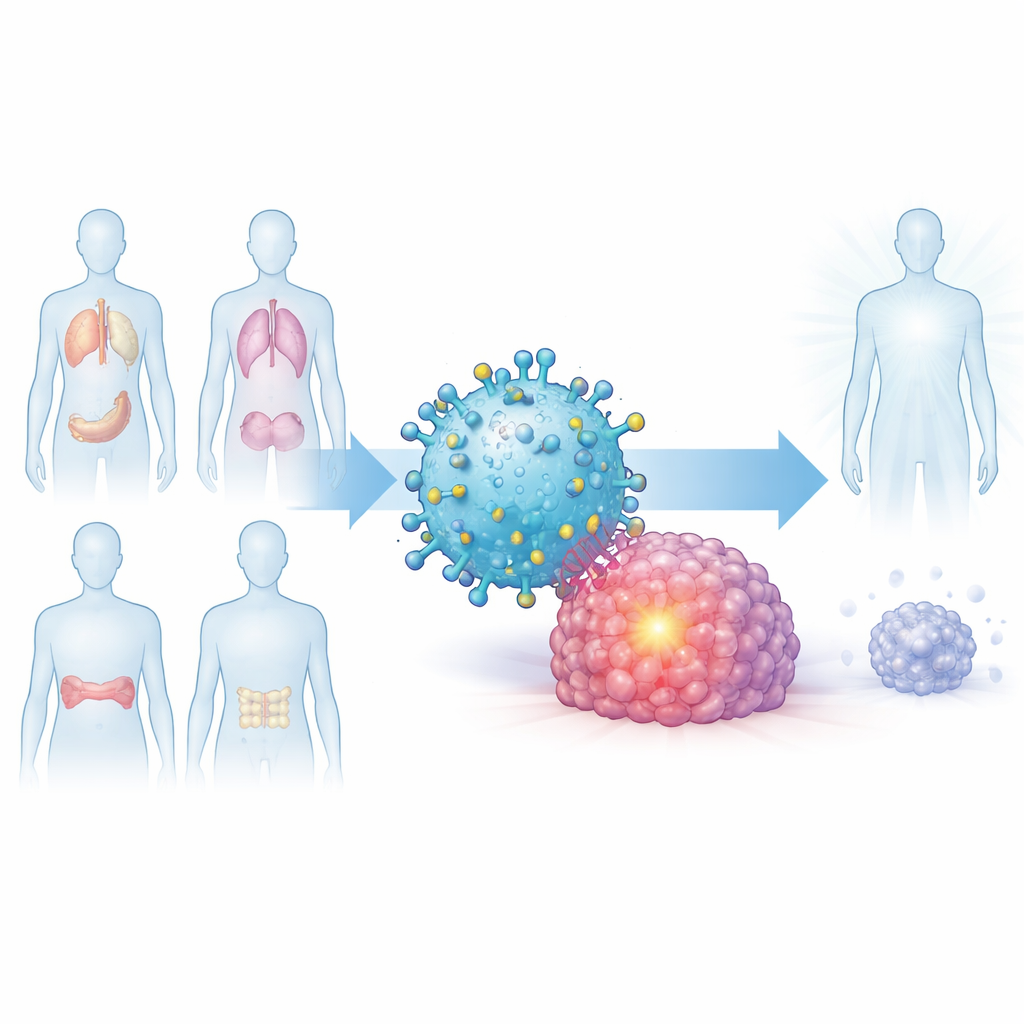
Una señal común compartida por muchos tumores
Los investigadores empezaron preguntándose si existe una característica molecular compartida que aparezca en distintos cánceres pero rara vez en órganos sanos. Se centraron en una proteína llamada Dickkopf-1, o DKK1, que regula vías de crecimiento celular y se encuentra en niveles elevados en mieloma múltiple, cáncer de páncreas, cáncer de pulmón y cáncer de mama triple negativo agresivo. Al analizar grandes bases de datos genómicos públicas y examinar muestras tumorales, mostraron que DKK1 es mucho más abundante en muchos tumores que en los tejidos normales emparejados, y que los pacientes cuyos tumores producen más DKK1 suelen tener peor supervivencia.
Convertir una bandera tumoral en un objetivo preciso
Como DKK1 normalmente flota fuera de las células, no es un punto de agarre obvio para las células T, que reconocen fragmentos cortos de proteínas presentados en la superficie celular por moléculas llamadas HLA. Trabajos previos identificaron un fragmento corto de DKK1 que es mostrado por un tipo de HLA muy común conocido como HLA-A2. El equipo ya había creado un anticuerpo, llamado C2, que reconoce este fragmento de DKK1 cuando está sostenido por HLA-A2 en la superficie de la célula tumoral, pero no en la mayoría de las células sanas. En el estudio actual, construyeron un receptor de antígeno quimérico (CAR) usando la parte de reconocimiento de este anticuerpo, fusionándola con componentes de señalización internos de las células T para que células T ordinarias puedan reprogramarse y reconocer la combinación DKK1–HLA-A2, denominada complejo DKK1-A2.
Células T diseñadas que buscan y destruyen tumores
Los científicos probaron luego estas células CAR-T DKK1-A2 contra un panel amplio de líneas celulares humanas en el laboratorio, incluidas células de mieloma múltiple, páncreas, pulmón y cáncer de mama triple negativo. Siempre que las células tumorales mostraban tanto DKK1 como HLA-A2, las células T diseñadas se multiplicaban vigorosamente, liberaban moléculas inmunitarias potentes y mataban con eficacia las células cancerosas. Cuando se eliminó DKK1 de las células tumorales, o cuando las células carecían de HLA-A2, las CAR-T dejaron de atacar, demostrando que su actividad es altamente específica para el objetivo previsto.
Demostrar eficacia en modelos vivos
Para ver si este enfoque podía reducir cánceres ya establecidos en organismos vivos, el equipo utilizó varios modelos de ratón portadores de tumores humanos. Las CAR-T DKK1-A2 controlaron o eliminaron mieloma múltiple que crecía en la médula ósea, tumores pancreáticos implantados en el páncreas, cáncer de pulmón que se había diseminado por el torrente sanguíneo y cánceres de mama agresivos, mientras que las células CAR-T dirigidas a CD19 usadas como control tuvieron poco efecto. La terapia también funcionó contra tumores derivados de cánceres pancreáticos reales de pacientes trasplantados en ratones, lo que imita más de cerca la enfermedad humana. Una versión humanizada del CAR, diseñada para ser adecuada para uso clínico, mostró un control a largo plazo aún mejor, en parte porque estas células T adoptaron un estado similar al de memoria que les permitió persistir y responder de nuevo cuando los tumores reaparecieron.
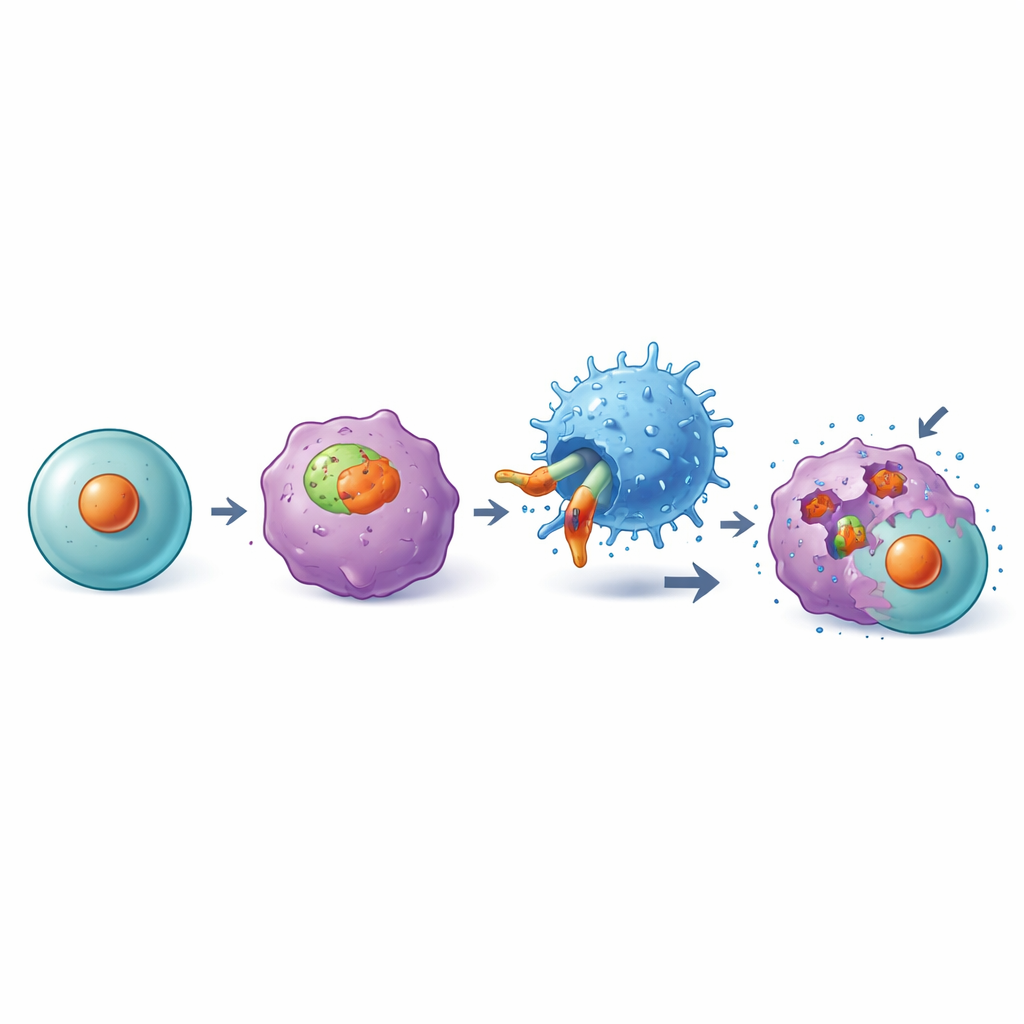
Comprobaciones de seguridad en sangre y órganos sanos
Cualquier terapia dirigida debe respetar los tejidos sanos. Los autores tiñeron por tanto docenas de tipos de tejidos humanos normales y encontraron que, aparte de las amígdalas, el complejo DKK1-A2 estaba esencialmente ausente. En pruebas de laboratorio, las CAR-T DKK1-A2 no dañaron células sanguíneas ni de médula ósea de donantes sanos HLA-A2 positivos, en contraste con las CAR-T contra CD19, que previsiblemente destruyeron las células B normales. En modelos de ratón diseñados para expresar DKK1 y HLA-A2 humanos, las nuevas CAR-T no agotaron poblaciones sanguíneas clave ni plaquetas y causaron menos signos de liberación peligrosa de citocinas que algunos diseños de CAR existentes, lo que respalda un perfil de seguridad favorable.
Qué podría significar esto para los pacientes
En conjunto, los hallazgos sugieren que el complejo DKK1-A2 es un “blanco” prometedor que aparece en muchos cánceres difíciles de tratar pero se mantiene fuera de la mayoría de los tejidos normales. Las células T armadas con el CAR DKK1-A2 pudieron reconocer y destruir diversos tumores en modelos preclínicos mostrando una toxicidad limitada. Si estos resultados se traducen a humanos, este enfoque podría ofrecer una nueva inmunoterapia compartida para pacientes HLA-A2 positivos con mieloma múltiple, cáncer de páncreas, de pulmón y ciertos cánceres de mama, ampliando el alcance del tratamiento con CAR-T más allá de los cánceres de la sangre hacia el ámbito de los tumores sólidos.
Cita: Zhang, Y., Xiong, W., Qian, J. et al. T cells engineered against Dickkopf-1-A2 complex can be used to treat HLA-A2+ solid and hematologic cancers. Nat Commun 17, 2818 (2026). https://doi.org/10.1038/s41467-026-69621-8
Palabras clave: Terapia con células CAR-T, DKK1, cáncer de páncreas, mieloma múltiple, inmunoterapia de tumores sólidos