Clear Sky Science · es
Catión radical y dication aislables de dialumeno
Por qué importa esta historia del aluminio
Los químicos buscan constantemente metales más baratos y abundantes capaces de realizar las tareas sofisticadas que hoy en día llevan a cabo elementos preciosos como el paladio o el platino. Este estudio muestra que el aluminio —un metal más conocido por las latas y la aeronáutica— puede forzarse a adoptar formas inusualmente reactivas que se comportan algo así como pequeños interruptores electrónicos. Entender y controlar estas especies exóticas de aluminio podría, con el tiempo, ayudar a crear nuevos catalizadores para procesos químicos y materiales más limpios.
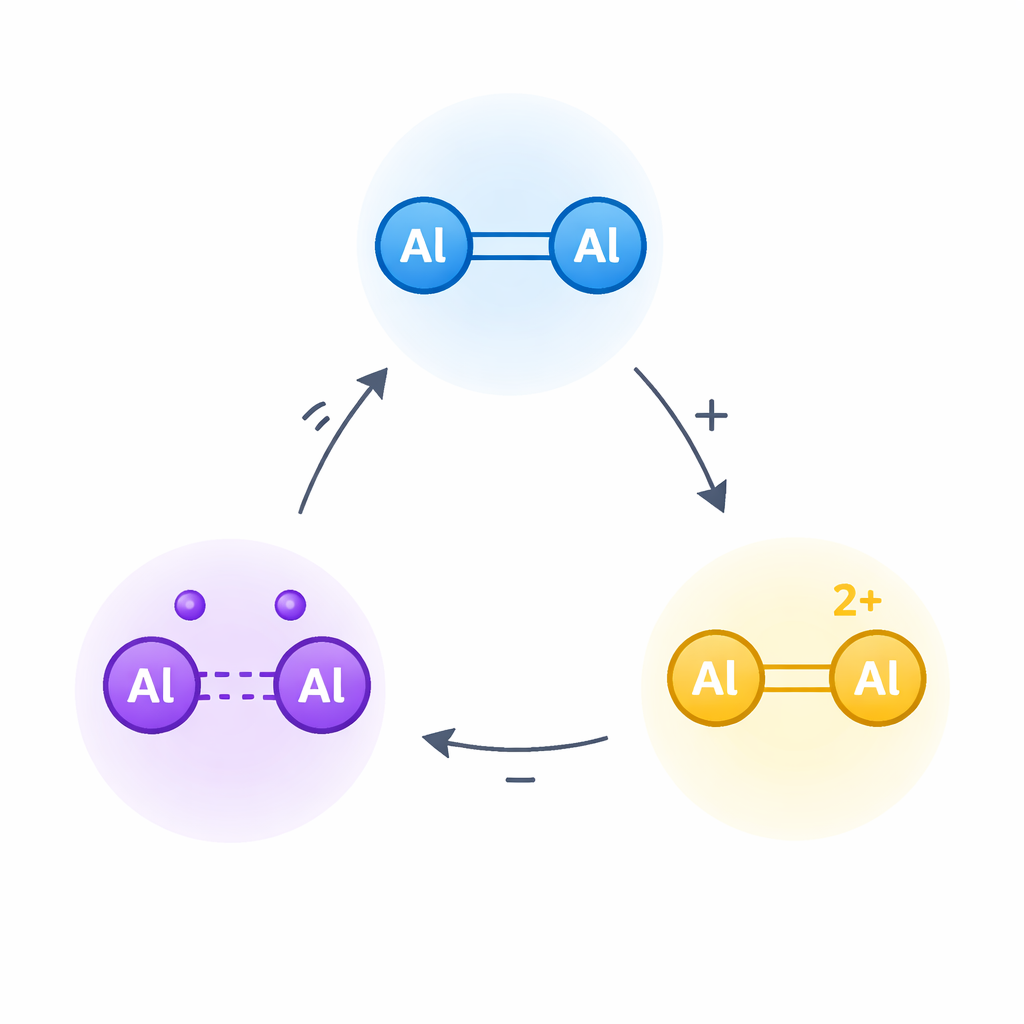
Convertir un enlace familiar en un conmutador electrónico
El trabajo se centra en el dialumeno, una molécula en la que dos átomos de aluminio comparten un doble enlace, de modo parecido al doble enlace carbono–carbono en los alquenos comunes. En las moléculas orgánicas, esos dobles enlaces pueden oxidarse por etapas para dar primero cationes radicalarios y luego dicationes, formas altamente cargadas y reactivas que sustentan muchas reacciones en electroquímica y ciencia de materiales. Los autores se preguntaron si el enlace aluminio–aluminio en el dialumeno podría someterse a una oxidación en dos pasos similar, aun cuando el aluminio es fuertemente deficitario en electrones y tales especies cargadas deberían ser excepcionalmente inestables.
Diseñar un armazón molecular protector
Para domesticar esa reactividad, el equipo construyó un dialumeno rodeado por grupos voluminosos a base de silicio y ligandos «carbeno» fuertemente donantes de electrones. Estos actúan como una armadura acolchada y cojines electrónicos: protegen el delicado núcleo aluminio–aluminio de reacciones indeseadas y ayudan a suministrar densidad electrónica donde se necesita. A partir de este dialumeno neutro, denominado 1, usaron agentes oxidantes cuidadosamente elegidos para extraer primero un electrón y luego un segundo, generando un catión radicalario centrado en aluminio (2) y después un dication (3). La cristalografía de rayos X proporcionó instantáneas de los tres estados, revelando cómo el enlace aluminio–aluminio se alarga gradualmente y cambia de carácter a medida que se extraen electrones.
Demostrar un verdadero ciclo redox de tres vías
Mediciones clave confirmaron que el catión radicalario realmente porta un electrón desapareado centrado entre los dos átomos de aluminio, y no en los ligandos circundantes. La espectroscopía de resonancia paramagnética electrónica mostró una señal clara consistente con un único electrón compartido por ambos centros de aluminio. Estudios computacionales respaldaron esta imagen, indicando que el electrón de enlace restante ocupa un orbital en gran medida aluminio–aluminio. Cuando se elimina el segundo electrón para formar el dication, el enlace se debilita hacia un enlace simple y la carga positiva se acumula en el par de átomos de aluminio. Es importante que los investigadores demostraron que todos estos cambios son reversibles: añadir electrones con un agente reductor regenera primero el catión radicalario y después el dialumeno original, y mezclar las formas neutra y doblemente cargada produce el catión radicalario mediante un proceso de comproporcionamiento. En conjunto, estas reacciones demuestran un ciclo redox robusto y aislable de tres estados sobre una unidad simple aluminio–aluminio.
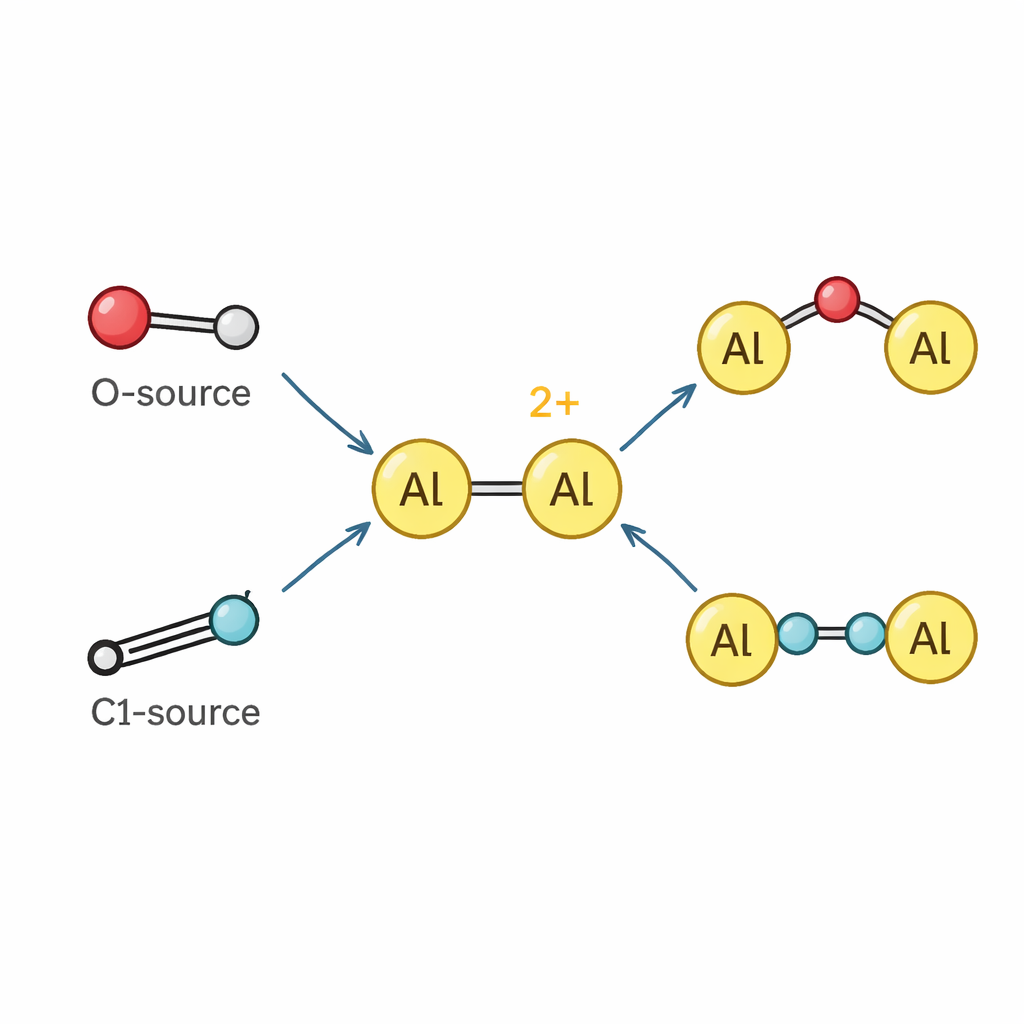
Hacer que el aluminio actúe como un metal de transición
Con el dication en mano, el equipo exploró cómo reacciona con otras moléculas. Debido a que sus átomos de aluminio son fuertemente pobres en electrones, el dication se comporta como un potente ácido de Lewis, uniéndose fácilmente a parejas básicas como la piridina y moléculas relacionadas para dar nuevos complejos de dialuminio. Más allá de la simple coordinación, el dication puede romper e insertarse en enlaces químicos. Extrae átomos de oxígeno del óxido nitroso y de la piridina N-óxido, formando especies estables donde un átomo de oxígeno puentea los dos centros de aluminio o se incorpora en una corta cadena aluminio–oxígeno–silicio reminiscentede un pequeño fragmento de la estructura de una zeolita. También reacciona con isocianuros —pequeñas unidades carbono–nitrógeno usadas como bloques de construcción de un carbono— para enlazarlos formando fragmentos N–C–C–N más largos que se extienden entre dos átomos de aluminio, demostrando un raro ejemplo de «homologación» de isocianuros impulsada por un catión del grupo principal.
Qué implica esto de cara al futuro
En términos cotidianos, los investigadores han convertido un enlace aluminio–aluminio en un conmutador electrónico de tres posiciones controlable que puede alternarse entre estados neutro, con carga simple y con carga doble, cada uno con formas y reactividades distintas. La versión doblemente cargada es especialmente versátil, captando electrones y pequeños fragmentos de otras moléculas de maneras que suelen asociarse con metales de transición más caros. Al demostrar que tal comportamiento es posible con aluminio y que los diferentes estados pueden interconvertirse de forma fiable, este trabajo abre la puerta al diseño de nuevos catalizadores y materiales funcionales sostenibles construidos a partir de uno de los metales más abundantes de la Tierra.
Cita: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Palabras clave: catálisis con aluminio, moléculas con conmutación redox, química de los elementos principales, cationes radicalarios, activación de pequeñas moléculas