Clear Sky Science · es
El eje Treg-γδ determina la dimorfia sexual en la hepatocarcinogénesis
Por qué algunos cánceres de hígado afectan más a los hombres
Los médicos saben desde hace tiempo que el cáncer de hígado afecta a los hombres aproximadamente el doble que a las mujeres, pero las razones van más allá de las diferencias simples en las hormonas sexuales. Este estudio se adentra en las células inmunitarias que habitan dentro de los tumores hepáticos y descubre una conversación oculta entre dos tipos de células T que ayuda a explicar por qué los hígados masculinos son más vulnerables, y cómo este conocimiento podría señalar tratamientos nuevos y más personalizados.
La lucha inmunitaria dentro de los tumores hepáticos
El cáncer de hígado, en particular el carcinoma hepatocelular, crece dentro de un vecindario complejo de células inmunitarias, vasos sanguíneos y tejido cicatrizado. Los autores compararon tumores de hombres y mujeres, tanto en pacientes como en modelos murinos, y encontraron un desequilibrio llamativo: los tumores masculinos estaban llenos de más células T reguladoras, o Tregs, un tipo celular que normalmente ayuda a calmar reacciones inmunitarias excesivas. Al mismo tiempo, el número total de otros linfocitos T comunes no difería mucho entre los sexos. Dado que niveles altos de Tregs se asociaron con una peor supervivencia, el equipo sospechó que estas células no eran meros espectadores, sino cómplices activas que ayudan a los tumores a escapar del ataque inmunitario. 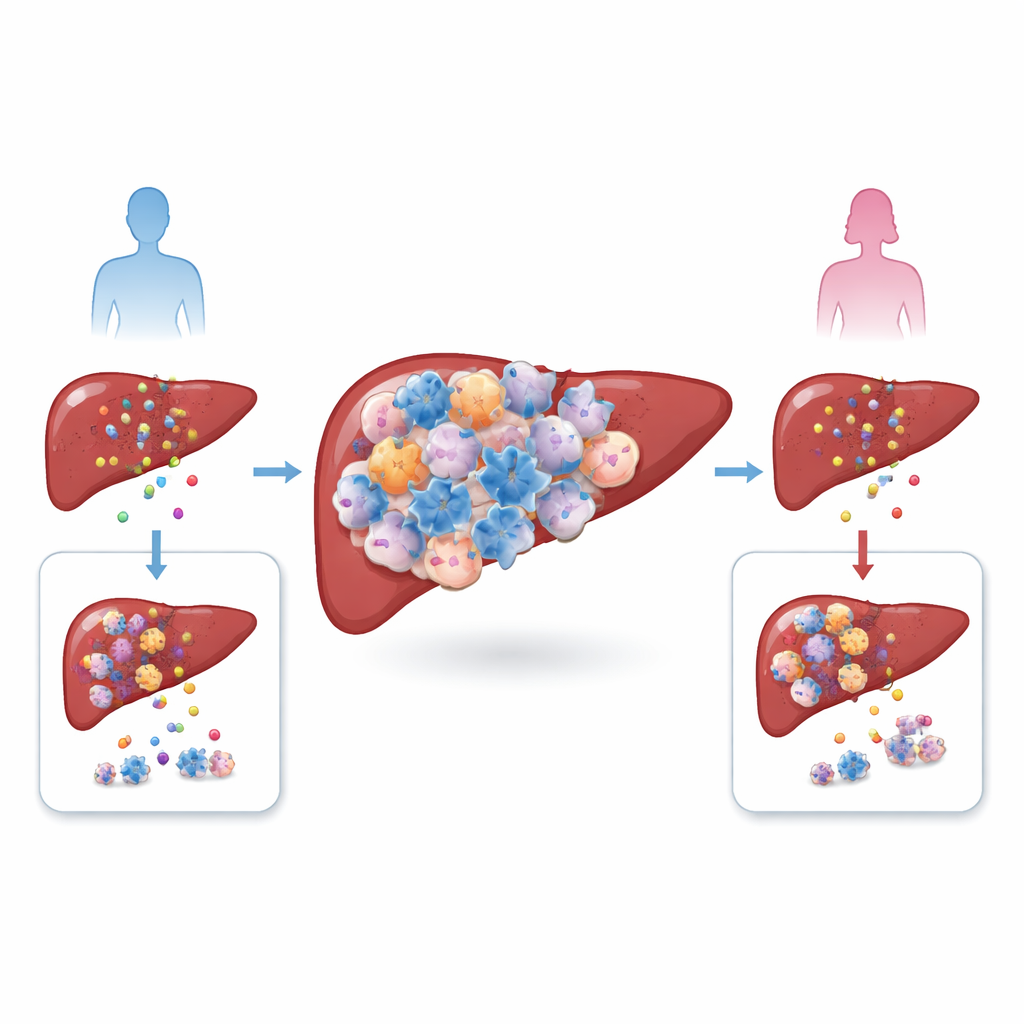
Cómo las hormonas masculinas reclutan células supresoras
Para entender por qué los tumores masculinos atraen más Tregs, los investigadores se centraron en las señales químicas producidas por las células cancerosas. Encontraron que los tumores hepáticos masculinos producían mayores cantidades de una molécula llamada Ccl2, mientras que las Tregs presentaban más de su receptor correspondiente, Ccr2. Este emparejamiento actúa como una señal de orientación que atrae a las Tregs hacia el tumor. Cuando la señal Ccl2 o el receptor Ccr2 fueron eliminados en ratones, los tumores se redujeron y muchas menos Tregs entraron en el hígado, especialmente en los machos. El equipo demostró además que la testosterona, la principal hormona sexual masculina, impulsa este proceso: activa una cadena de proteínas en las células de cáncer hepático que enciende el gen Ccl2, potenciando la llamada química que convoca a las Tregs. Los ratones machos castrados, que producen menos testosterona, presentaron menos Ccl2 en sus tumores y menos Tregs infiltradas.
Células guardián que podrían combatir el cáncer—pero están contenidas
Otro tipo de células T, conocidas como células T gamma-delta, pueden actuar como “guardianes” de respuesta rápida que reconocen y matan células tumorales sin la maquinaria habitual de presentación de antígenos. En el hígado sano, estas células son relativamente escasas, pero en el cáncer hepático pueden ser luchadoras tumorales potentes. El estudio encontró que los tumores femeninos contenían más de estas células gamma-delta y que estaban más activas y mejor equipadas con moléculas tóxicas. La eliminación de las hormonas sexuales masculinas en ratones aumentó el número y el vigor de las células gamma-delta en los tumores, mientras que las clásicas células CD8 citotóxicas se mantenían en gran medida sin cambios. En cultivos, las células gamma-delta dañaron fácilmente las células de cáncer hepático, pero este efecto se debilitó cuando se añadieron Tregs, lo que sugiere que las Tregs reprimen específicamente a esta prometedora población antitumoral.
Hipoxia, paquetes secretos y defensores silenciados
Indagando más, los investigadores se preguntaron cómo las Tregs consiguen apagar a las células gamma-delta. Dentro de los tumores, el oxígeno suele ser escaso, un estado llamado hipoxia. Bajo estas condiciones de bajo oxígeno, las Tregs en tumores masculinos empezaron a producir grandes cantidades de una proteína llamada S100a4. En lugar de actuar directamente como una molécula libre, S100a4 se empaquetó en pequeñas partículas membranosas conocidas como vesículas extracelulares. Estas vesículas brotaron de las Tregs y fueron captadas por las células gamma-delta vecinas. Una vez dentro, S100a4 reprogramó los sistemas de control genético de las células: redujo la accesibilidad de regiones del ADN que controlan moléculas clave de señalización y citotoxicidad y disminuyó su actividad. Las células gamma-delta se volvieron menos capaces de responder a través de sus receptores de células T y menos aptas para liberar proteínas tóxicas y citocinas, embotando efectivamente su filo antitumoral. 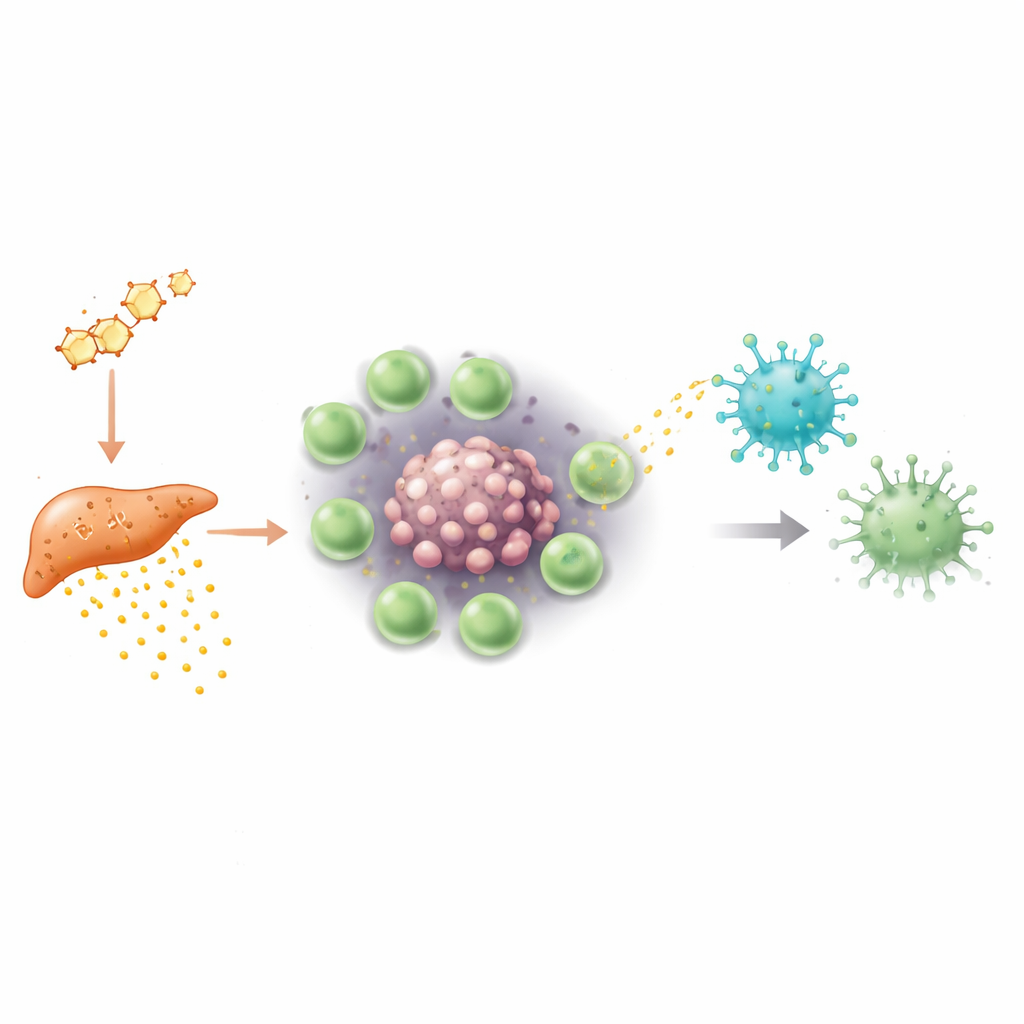
Rompiendo el circuito dañino
Finalmente, el equipo probó qué ocurre si se interrumpe este eje Treg–S100a4–gamma-delta. En ratones diseñados para que las Tregs no puedan producir S100a4, los tumores hepáticos masculinos se redujeron, el nivel global de S100a4 en los tumores cayó y las células T gamma-delta se volvieron más abundantes y más activas. Es notable que el número de Tregs en el tumor no disminuyó: solo se levantó su impacto supresor sobre las células gamma-delta. Este cambio casi borró la brecha habitual en la gravedad tumoral entre ratones machos y hembras, subrayando lo central que es esta vía para las diferencias sexuales en el cáncer de hígado.
Qué significa esto para tratamientos futuros
En términos accesibles, el estudio muestra que las hormonas masculinas inducen a las células del cáncer hepático a enviar señales de “bienvenida” más fuertes para las Tregs inmunosupresoras. Una vez dentro del tumor—y bajo el estrés de la baja oxigenación—estas Tregs envían vesículas llenas de S100a4 que desarman silenciosamente a las células gamma-delta cercanas, que de otro modo podrían mantener el cáncer bajo control. Al dirigirse bien a la señal Ccl2 que trae a las Tregs, bien a los mensajes de S100a4 que silencian a las gamma-delta, futuras terapias podrían restaurar las defensas del propio organismo, especialmente en los hombres. Este trabajo sugiere que el tratamiento del cáncer de hígado podría beneficiarse de tener en cuenta el sexo y de aprovechar, en lugar de ignorar, las fortalezas únicas de las células T gamma-delta.
Cita: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Palabras clave: carcinoma hepatocelular, células T regulatorias, células T gamma-delta, diferencias sexuales, inmunología tumoral