Clear Sky Science · es
Reclutamiento dual de dos moléculas de CCM2 a KRIT1 suprime la expresión de KLF4
Por qué los vasos sanguíneos del cerebro necesitan un control cuidadoso
Los vasos sanguíneos del cerebro deben mantener un delicado equilibrio: tienen que ser lo bastante resistentes para evitar fugas y, al mismo tiempo, lo bastante flexibles para responder a las necesidades del organismo. Cuando este equilibrio falla, las personas pueden desarrollar malformaciones cavernosas cerebrales: agrupaciones de vasos frágiles, en forma de burbuja, que pueden sangrar y provocar convulsiones o ictus. Este estudio descubre un apretón de manos molecular hasta ahora desconocido entre tres proteínas que ayuda a mantener la estabilidad de los vasos cerebrales y muestra cómo la ruptura de ese contacto puede impulsar la enfermedad.
Los guardianes de la salud vascular
Las células que recubren los vasos sanguíneos dependen de un conjunto de interruptores maestros, llamados KLF2 y KLF4, para controlar genes que mantienen la resistencia y la identidad vascular. Si estos interruptores se activan en exceso, los vasos se vuelven anormales y propensos al daño. Se sabe que otras dos proteínas, KRIT1 y CCM2, protegen este sistema. Las personas que heredan versiones defectuosas de cualquiera de estas proteínas tienen un alto riesgo de malformaciones cavernosas cerebrales. Hasta ahora, sin embargo, los científicos no entendían exactamente cómo KRIT1 y CCM2 trabajaban juntos para mantener a KLF4 bajo control.
Un sorprendente equipo de tres
Los investigadores emplearon células humanas con fenotipo endotelial cultivadas en el laboratorio y redujeron selectivamente la cantidad de CCM2 o KRIT1 mediante herramientas genéticas. Cuando se agotaba cualquiera de las dos proteínas, los niveles de KLF4 se disparaban, reproduciendo lo observado en modelos animales y pacientes. Restaurar niveles normales de CCM2 o KRIT1 reducía KLF4, pero solo si las proteínas restauradas seguían pudiendo adherirse entre sí. Al introducir cambios precisos en las regiones donde interactúan CCM2 y KRIT1, el equipo demostró que este contacto físico es esencial para evitar el aumento de KLF4. Estos experimentos sitúan con firmeza la asociación KRIT1–CCM2 en el centro del sistema de control de este potente factor de transcripción.
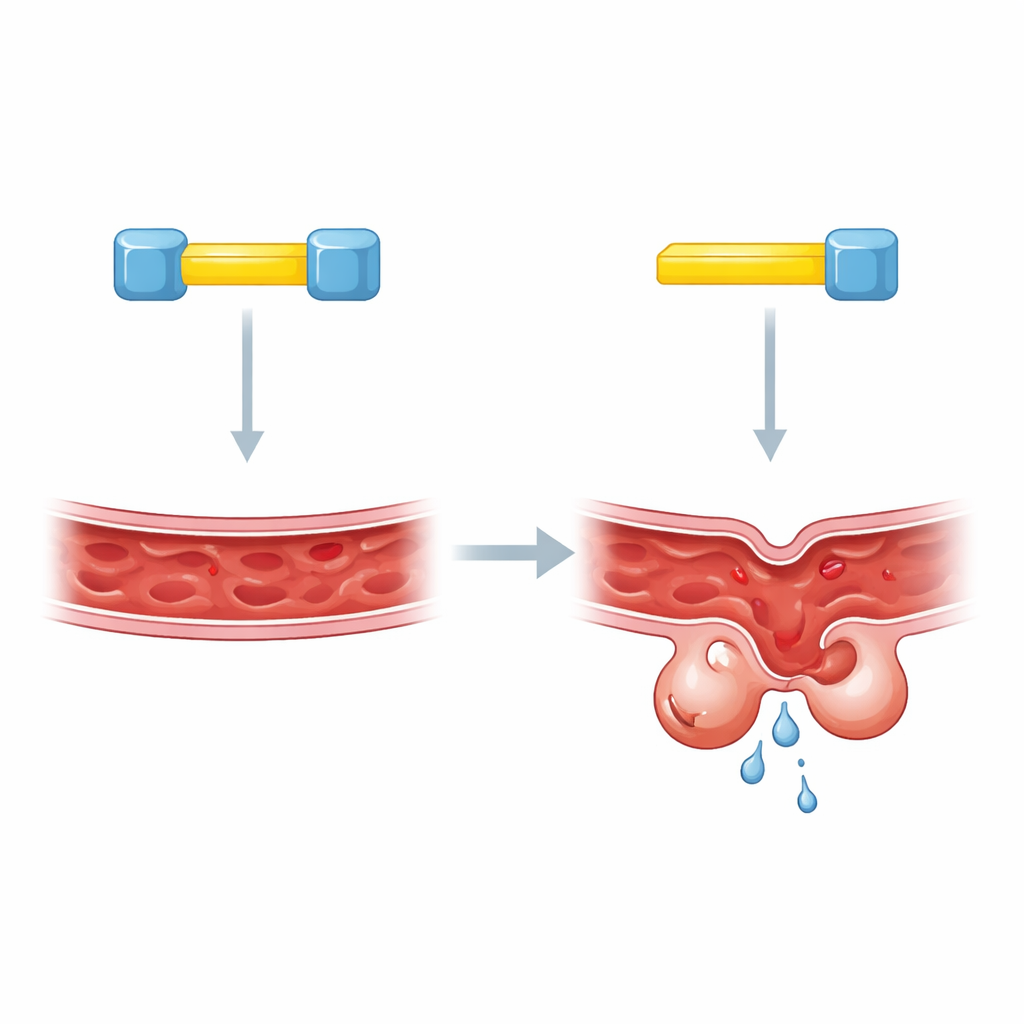
Dos cerraduras para una llave
Para profundizar, los autores se centraron en segmentos cortos dentro de KRIT1 que actúan como sitios de acoplamiento molecular. Trabajos previos sugerían que CCM2 se unía a KRIT1 en uno de esos sitios, pero distintos métodos habían dado respuestas contradictorias sobre cuál era. El nuevo estudio revela que la confusión surgía porque la realidad es más compleja: KRIT1 lleva dos segmentos de acoplamiento próximos, y ambos son necesarios. Cuando se perturbaba cualquiera de los segmentos, los niveles de KLF4 permanecían anormalmente altos, como si KRIT1 faltara por completo. Pruebas bioquímicas en células modificadas demostraron que una sola proteína KRIT1 puede enlazar simultáneamente dos moléculas distintas de CCM2, sugiriendo un ensamblaje inesperado de tres componentes.
Ver la abrazadera molecular en detalle
El equipo purificó entonces las piezas relevantes de CCM2 y KRIT1 y examinó cómo se ensamblan en solución y en cristales. Las medidas de la masa del complejo indicaron que dos copias de una región clave de CCM2 se unen a una sola tira de KRIT1 que contiene el par de sitios de acoplamiento. Instantáneas estructurales de alta resolución confirmaron esta disposición 2:1: un péptido extendido de KRIT1 se interpone entre dos dominios de CCM2, con cada sitio de acoplamiento alojándose en una cavidad similar de una molécula distinta de CCM2. Un breve segmento helicoidal entre los sitios de acoplamiento ayuda a posicionar los dos dominios de CCM2 uno junto al otro, creando una estructura ceñida, semejante a una abrazadera. Este tipo de interacción dual —dos dominios de unión que se enganchan a sitios en tándem de una misma pareja— no se había observado antes en esta familia de módulos proteicos.
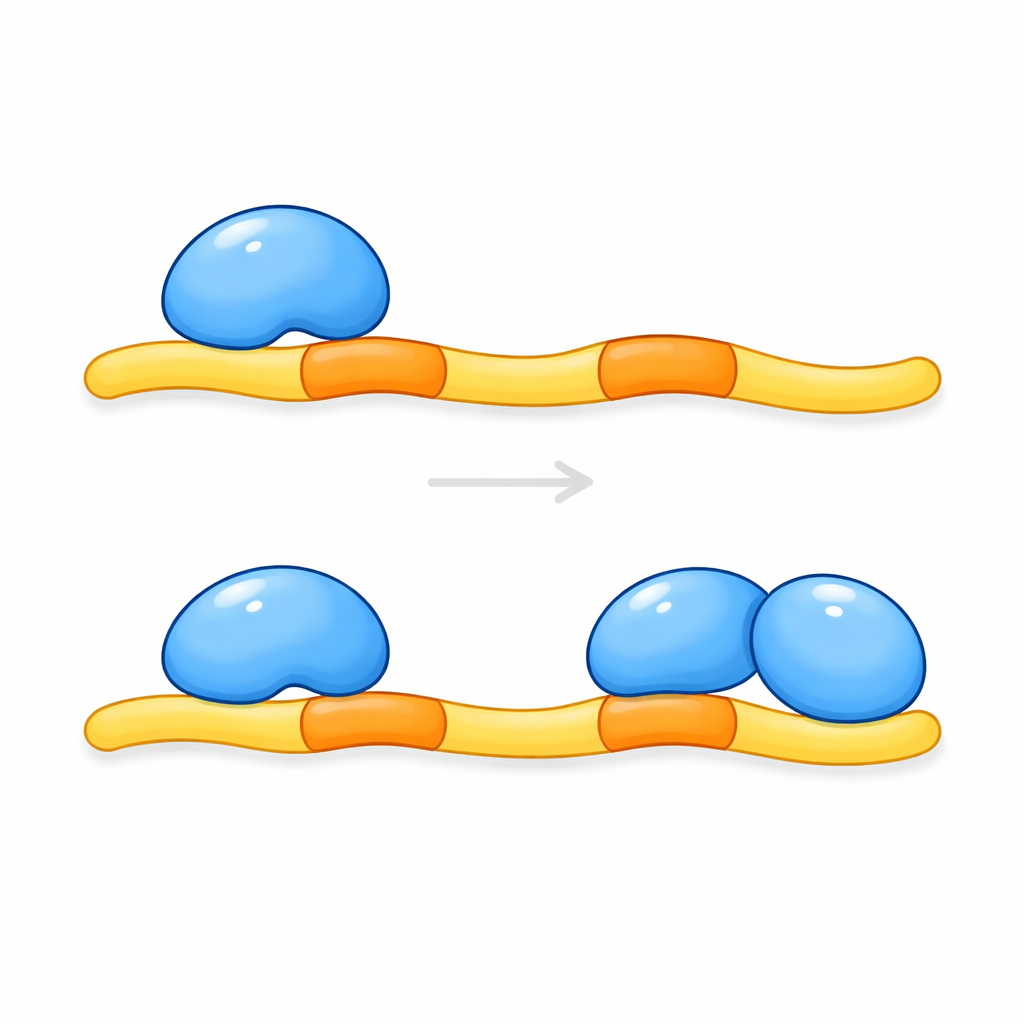
Implicaciones para las enfermedades cerebrales y más allá
Estos hallazgos muestran que KRIT1 no se limita a unirse a una sola molécula de CCM2; en cambio, actúa como un andamiaje que recluta un par de proteínas CCM2. Solo cuando ambos sitios de acoplamiento en KRIT1 están ocupados puede el complejo restringir adecuadamente la producción de KLF4 y, por extensión, ayudar a prevenir el crecimiento de vasos frágiles. Por tanto, se espera que las mutaciones en KRIT1 que interfieren con cualquiera de los sitios de acoplamiento debiliten esta abrazadera protectora y puedan explicar algunas formas hereditarias de malformaciones cavernosas cerebrales. Dado que muchas otras proteínas humanas poseen motivos gemelos de acoplamiento similares, este estudio sugiere además un principio más amplio: la unión dual por pares de dominios relacionados podría ser una forma común en que las células afinan las redes de señalización. Comprender esta interacción tripartita podría, en última instancia, orientar estrategias para estabilizar los vasos sanguíneos en personas con riesgo de hemorragias cerebrales.
Cita: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Palabras clave: malformaciones cavernosas cerebrales, células endoteliales, KRIT1, CCM2, KLF4