Clear Sky Science · es
Identificación sin contraste del estado de la barrera hematoencefálica en glioma mediante IA generativa por difusión y RM sin contraste
Por qué esto importa para los pacientes con tumores cerebrales
Las personas con tumores cerebrales se someten rutinariamente a exploraciones por resonancia magnética (RM), y muchas reciben además un medio de contraste inyectado para que los médicos puedan ver si la barrera protectora del cerebro —la barrera hematoencefálica— ha resultado dañada. Esa información orienta la cirugía, la radiación y el pronóstico, pero el contraste puede conllevar riesgos, añade tiempo y coste, y no siempre está disponible. Este estudio presenta un sistema de inteligencia artificial (IA) que interpreta exploraciones rutinarias de RM sin contraste y recreate virtualmente las imágenes de contraste faltantes, permitiendo a los médicos inferir el estado de la barrera hematoencefálica sin inyectar ningún agente de contraste.
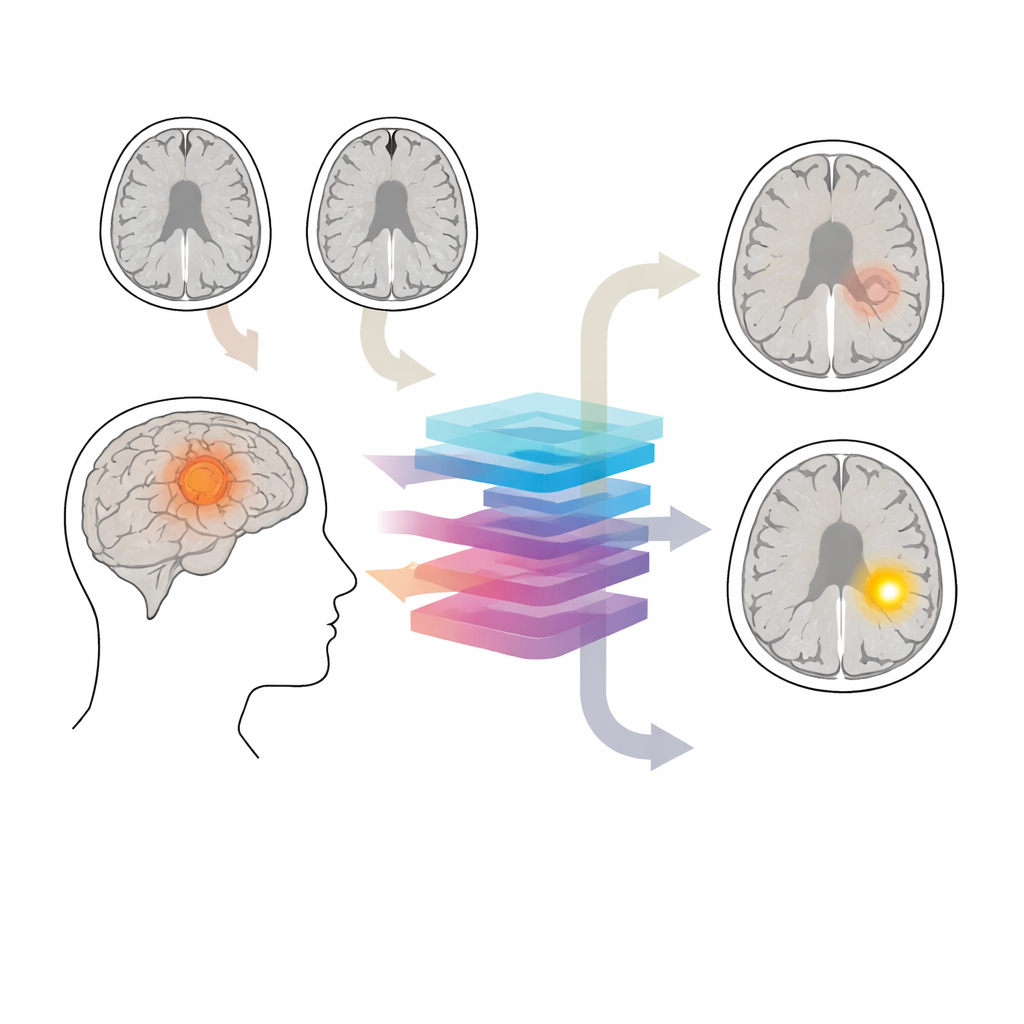
El guardián protector del cerebro
La barrera hematoencefálica actúa como un filtro microscópico alrededor de los vasos sanguíneos en el cerebro, dejando pasar solo moléculas muy pequeñas. En muchos gliomas, esta barrera se vuelve permeable. En la RM con contraste estándar, las zonas permeables se iluminan tras la inyección, mientras que las regiones intactas permanecen oscuras. Estos patrones influyen en la agresividad del tratamiento y ayudan a definir qué extirpar quirúrgicamente o qué segmentar con radiación. Sin embargo, a veces se omiten las exploraciones con contraste —por ejemplo en estudios iniciales o en el seguimiento a largo plazo de tumores de crecimiento lento— y algunos pacientes deben evitar el contraste por enfermedad renal, reacciones alérgicas o preocupaciones sobre la deposición de gadolinio en el cerebro.
Convertir exploraciones ordinarias en contraste virtual
Los autores se preguntaron si las RM sin contraste, que ya se obtienen de forma generalizada, contienen suficiente información sutil para que la IA infiera lo que habría mostrado una exploración con contraste. Se centraron en dos secuencias comunes: T1 y T2‑FLAIR. Aunque estas no muestran directamente la fuga de la barrera hematoencefálica, capturan la estructura tumoral, el edema circundante y el daño tisular que con frecuencia acompañan la ruptura de la barrera. El equipo construyó un sistema llamado CBSI que primero genera imágenes sintéticas con contraste a partir de estas exploraciones sin contraste y luego las utiliza, junto con las imágenes originales, para decidir si la barrera está intacta o alterada en cada glioma.
Cómo funciona el nuevo sistema de IA
En el núcleo de CBSI hay un modelo de difusión —un tipo de IA que parte de imágenes ruidosas y las “desruidosa” iterativamente hasta convertirlas en imágenes realistas. Aquí aprende a transformar las entradas sin contraste en dos imágenes virtuales alternativas con contraste: una asumiendo una barrera intacta y otra asumiendo una barrera permeable. Un mecanismo de guía indica al modelo qué patrón de realce debe generar, y un paso auxiliar de segmentación le ayuda a prestar atención adicional a la región tumoral. En una segunda etapa, una red separada compara los dos resultados sintéticos de cada paciente y valora cuál de ellos es más autoconsistente con los datos originales de RM. Esa decisión se traduce luego en el estado predicho de la barrera hematoencefálica.
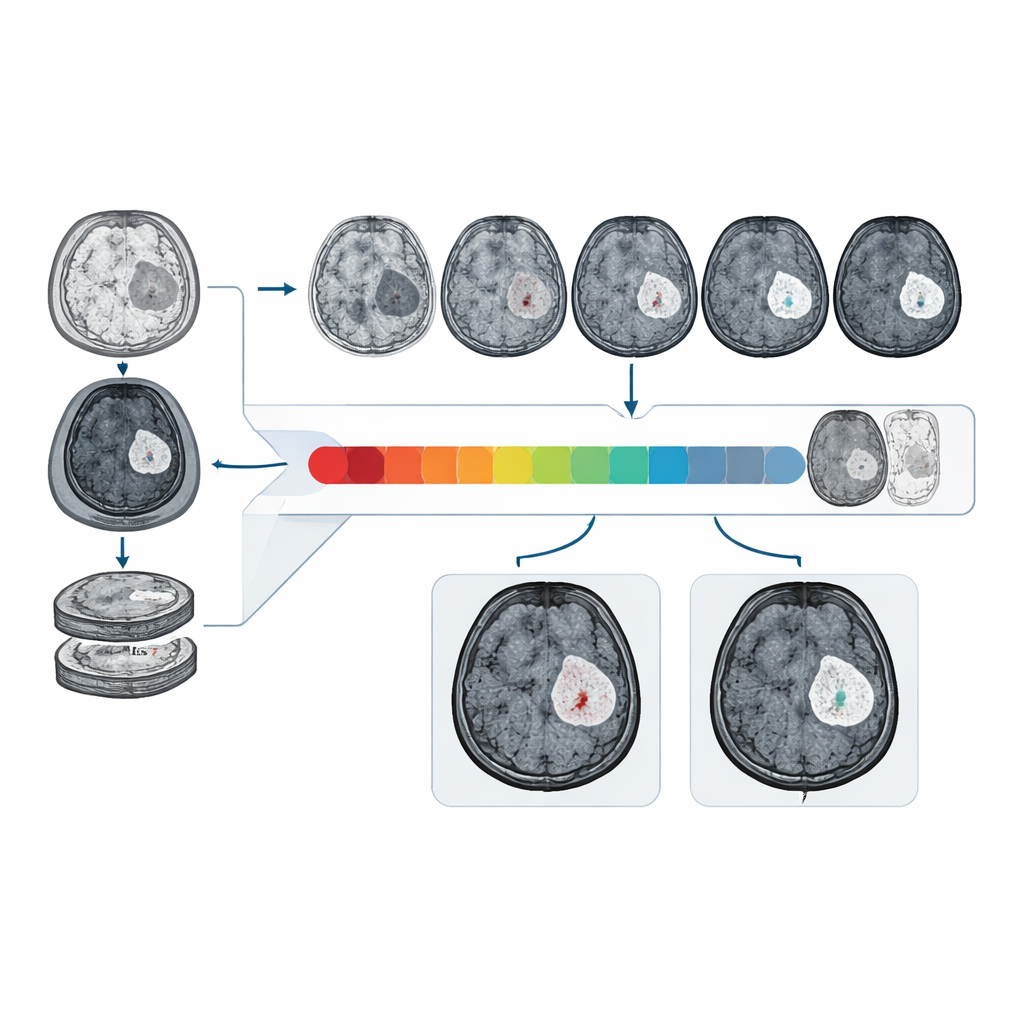
Rendimiento en datos reales y diversos
Los investigadores entrenaron y evaluaron CBSI con datos de RM de 1.535 pacientes con glioma recopilados en varios hospitales y en conjuntos de datos públicos internacionales. En un conjunto de prueba clínico externo, CBSI distinguió barreras intactas de barreras alteradas con un área bajo la curva de aproximadamente el 81%, claramente mejor que modelos que se basaban solo en imágenes sin contraste y acercándose al rendimiento de modelos que disponían de exploraciones con contraste reales. Los radiólogos, cuando vieron mezclas aleatorizadas de imágenes de contraste reales y sintéticas generadas por el sistema, consideraron que más del 90% de las imágenes sintéticas tenían una alta calidad diagnóstica, y su capacidad para identificar realce por contraste en imágenes sintéticas fue similar a su desempeño con exploraciones reales.
Beneficios para la planificación del tratamiento y la atención futura
Puesto que las imágenes de contraste sintéticas producidas por CBSI capturan detalles tumorales y patrones de realce, también mejoraron tareas posteriores como delinear los límites del tumor y estimar el grado tumoral —ambas dependientes en gran medida del comportamiento de la barrera hematoencefálica. El método se generalizó bien a distintos escáneres, protocolos de imagen y poblaciones de pacientes, incluidos datos de África subsahariana y cohortes internacionales más amplias. Aunque los autores reconocen que cualquier sistema de aprendizaje profundo sigue siendo una herramienta estadística más que una ventana directa a la biología, sus resultados sugieren que la imagen de contraste virtual podría reducir la dependencia de agentes inyectados, especialmente para pacientes vulnerables o en entornos donde las exploraciones con contraste son difíciles de obtener. En términos prácticos, este enfoque de IA podría permitir a los médicos extraer información clave que modela el tratamiento sobre la barrera hematoencefálica a partir de las exploraciones que los pacientes ya se realizan —sin una punción adicional.
Cita: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Palabras clave: glioma, barrera hematoencefálica, resonancia magnética cerebral, IA en imagen médica, imagen sin contraste