Clear Sky Science · es
IgG basadas en nanocuerpos inhiben simultáneamente la actividad alergénica y enzimática del alérgeno dominante del veneno de abeja
Por qué importan las alergias a las picaduras de abeja
Para la mayoría de las personas, una picadura de abeja melífera es dolorosa pero de corta duración. Para otras, puede desencadenar una reacción sistémica potencialmente mortal llamada anafilaxia. El tratamiento preventivo principal actual, la inmunoterapia con veneno, funciona para muchos pacientes, pero dura años, requiere inyecciones frecuentes y puede a su vez provocar efectos secundarios alérgicos. Este estudio explora una forma nueva y más dirigida de proteger a las personas con alergia peligrosa al veneno de abeja, desactivando un componente clave del veneno antes de que pueda causar daño.
El principal causante de problemas en el veneno de abeja
El veneno de la abeja melífera es un cóctel de distintas moléculas, pero una proteína, llamada fosfolipasa A2 (o Api m 1), destaca. Es el alérgeno dominante en pacientes alérgicos a la abeja y está presente en casi todos ellos. Api m 1 tiene un doble papel: daña las membranas celulares, contribuyendo al dolor y la inflamación en el lugar de la picadura, y también es un objetivo principal de los anticuerpos que causan alergia, conocidos como IgE. Cuando Api m 1 se une a IgE anclada en células inmunitarias como mastocitos y basófilos, puede desencadenar una reacción en cadena que conduce a la liberación súbita de mediadores inflamatorios y, en casos graves, a la anafilaxia.
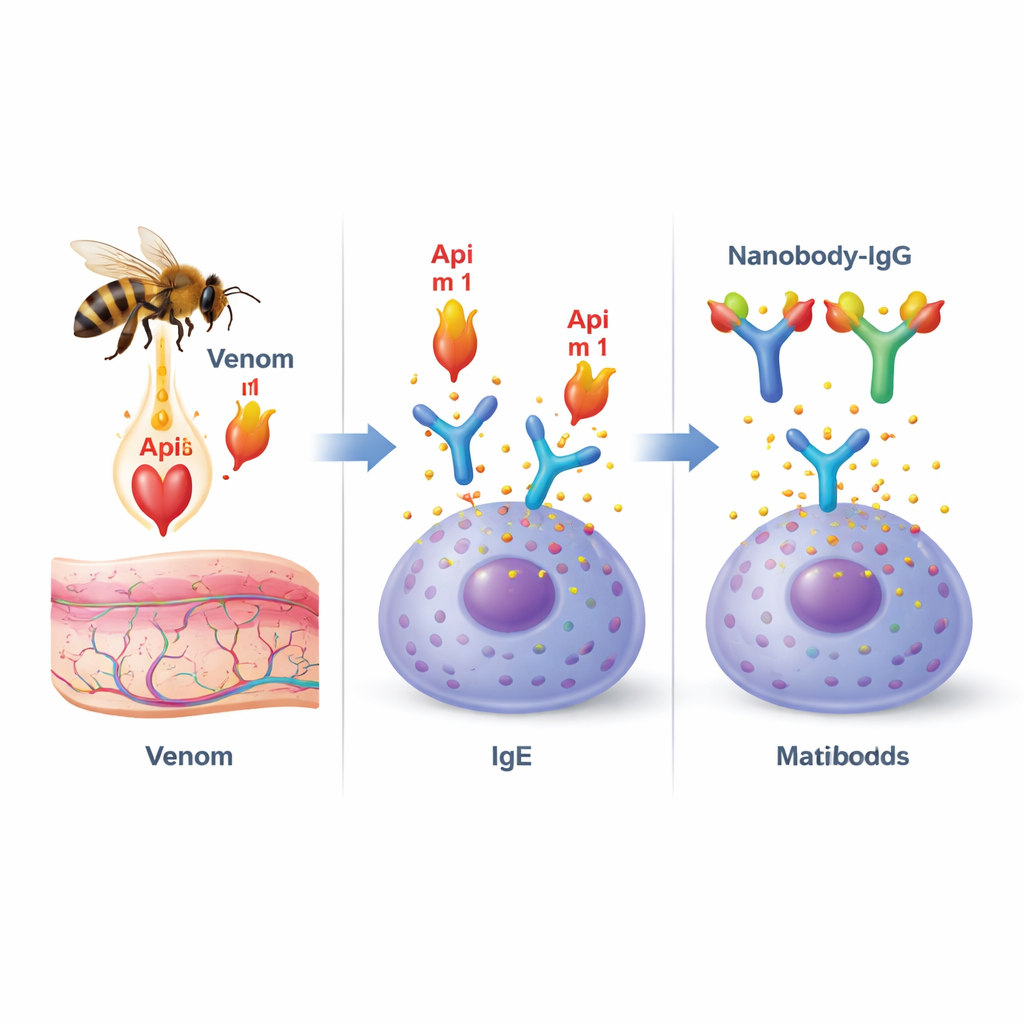
Diseñar anticuerpos diminutos para bloquear el alérgeno
Los investigadores recurrieron a los “nanocuerpos”, fragmentos de anticuerpos diminutos y estables descubiertos originalmente en los camélidos. Debido a su pequeño tamaño y forma alargada, los nanocuerpos encajan especialmente bien en hendiduras y huecos de las proteínas. El equipo aisló nanocuerpos específicos de Api m 1 a partir de una biblioteca inmune y seleccionó dos candidatos destacados, denominados AM1‑1 y AM1‑4. Trabajos estructurales detallados mediante cristalografía de rayos X mostraron que estos dos nanocuerpos se acoplan a lados opuestos de Api m 1 y no interfieren entre sí. Un nanocuerpo, AM1‑1, se sitúa directamente sobre el centro activo de la enzima, lo que sugiere que podría bloquear la función de Api m 1 de dañar membranas, mientras que AM1‑4 se acopla en un bolsillo separado en la superficie de la proteína.
Convertir nanocuerpos en bloqueadores potentes
Para convertir estos pequeños ligandos en fármacos de larga duración, los científicos fusionaron cada nanocuerpo con la porción de cola (región Fc) de la IgG1 humana, creando moléculas más grandes similares a anticuerpos con mayor estabilidad en la sangre. También diseñaron una versión “bispecífica” que incorpora tanto AM1‑1 como AM1‑4 en una única molécula tipo IgG. Pruebas de laboratorio mostraron que estas fusiones nanocuerpo‑IgG se unen a Api m 1 con afinidad extremadamente alta y que, cuando están presentes, pueden reducir de forma contundente la unión de IgE de la sangre de pacientes alérgicos a la abeja a Api m 1. En ensayos celulares, disminuyeron la activación de basófilos, las células inmunitarias que normalmente responden vigorosamente cuando las personas alérgicas se exponen a Api m 1.
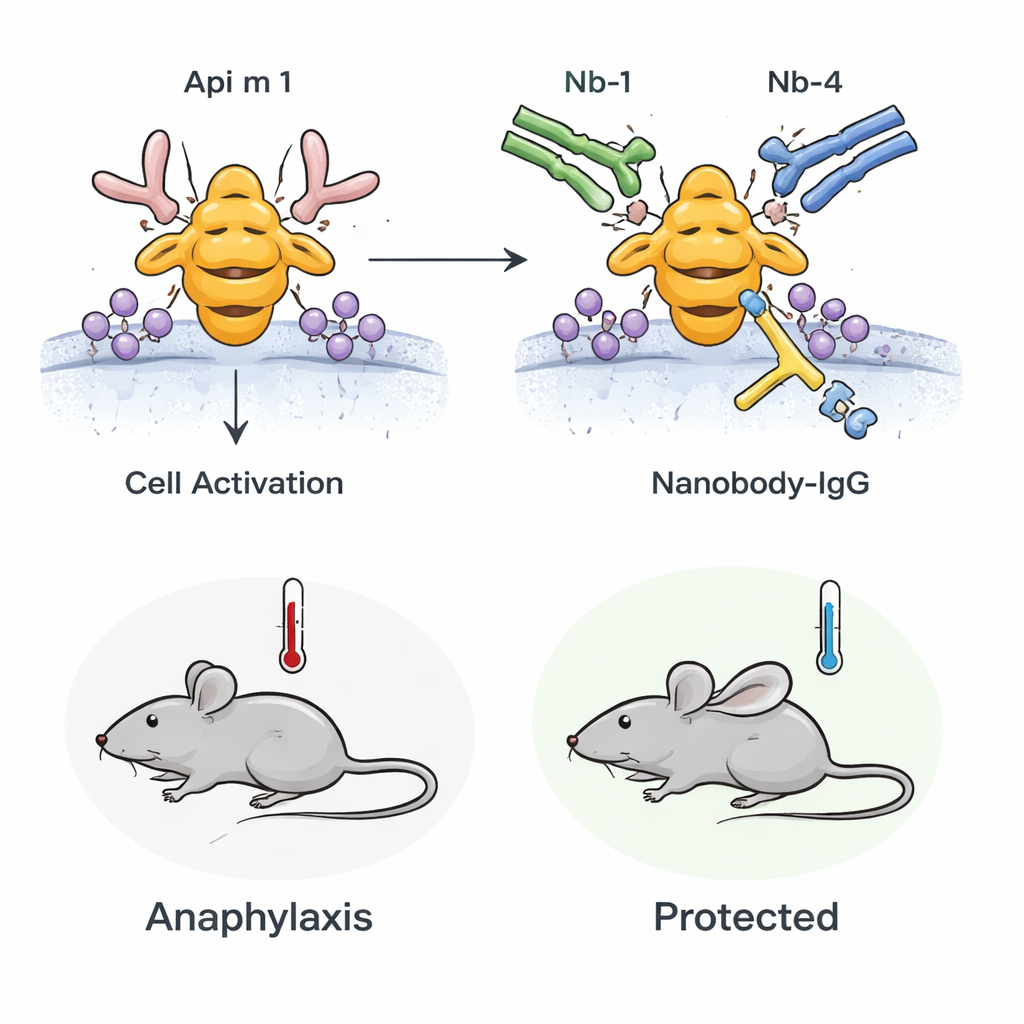
Del tubo de ensayo a animales vivos
El equipo preguntó a continuación si este efecto bloqueador se mantendría en un organismo vivo. Usaron ratones sensibilizados al veneno de abeja para que sus sistemas inmunitarios reaccionaran a Api m 1 de forma que imita la alergia humana. Cuando a estos ratones se les desafió con Api m 1, desarrollaron signos de anafilaxia, incluida una caída de la temperatura corporal y marcadores de activación de mastocitos en la sangre. Sin embargo, si los ratones fueron pretratados con la IgG bispecífica basada en nanocuerpos, tanto la caída de temperatura como la activación de mastocitos se redujeron de manera significativa. Esto demuestra que anticuerpos bloqueadores de alta afinidad preexistentes pueden atenuar la reacción alérgica sistémica a Api m 1 in vivo.
Qué podría significar esto para personas con alergia al veneno de abeja
En conjunto, el estudio muestra que moléculas IgG basadas en nanocuerpos cuidadosamente diseñadas pueden bloquear simultáneamente las acciones alérgicas y enzimáticas de Api m 1, el principal culpable en la alergia al veneno de abeja. Para los pacientes, esto plantea la posibilidad de una inmunización pasiva estacional: unas pocas inyecciones de dichos anticuerpos durante los meses con mayor riesgo de picaduras podrían proporcionar protección temporal contra reacciones graves, sin el compromiso prolongado y los riesgos de la inmunoterapia tradicional con veneno. Aunque se necesita más trabajo para ampliar el enfoque a otros componentes del veneno y para evaluar la seguridad y eficacia en humanos, esta estrategia basada en nanocuerpos ofrece una manera precisa de proteger a las personas vulnerables de picaduras de abeja peligrosas.
Cita: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Palabras clave: alergia al veneno de abeja, nanocuerpos, inmunoterapia pasiva, fosfolipasa A2, prevención de la anafilaxia