Clear Sky Science · es
Reconocimiento cooperativo del promotor mediado por una abrazadera por la ARN polimerasa de los poxvirus y su pareja similar a TBP/TFIIB
Cómo un virus reconfigura el control génico dentro de nuestras células
Los poxvirus, que incluyen al virus históricamente responsable de la viruela, realizan toda su expresión génica en el citoplasma de nuestras células, lejos del centro de control del ADN en el núcleo. Para lograrlo, llevan consigo su propia «fábrica genética» en miniatura. Este estudio revela, con detalle atómico, cómo uno de esos virus, Vaccinia, activa una ola específica de sus genes a mitad de la infección mediante una proteína inesperada en forma de abrazadera que actúa junto con la máquina viral de copiado.
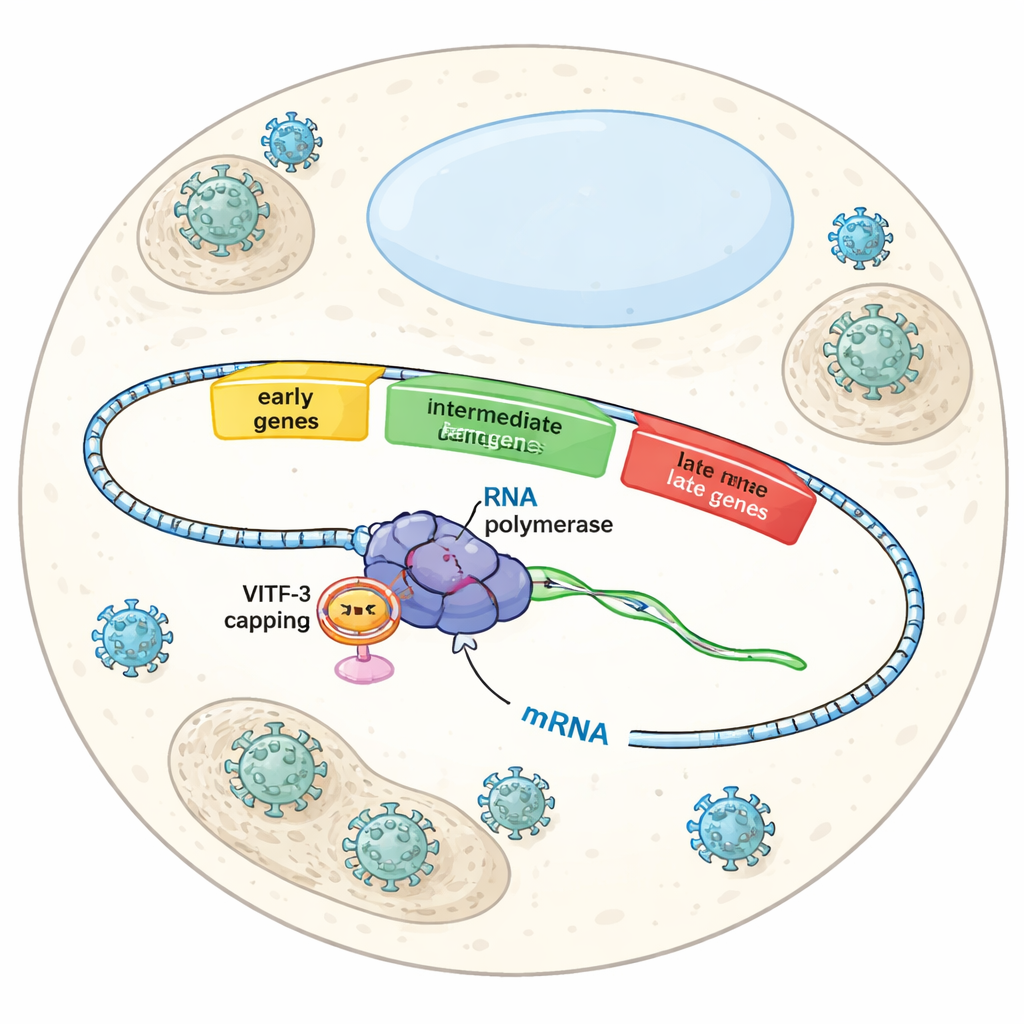
Tres olas en una toma de control viral
Cuando Vaccinia infecta una célula, no enciende todos sus genes a la vez. En lugar de eso, sigue un guion temporizado con genes tempranos, intermedios y tardíos. Los genes tempranos preparan el terreno para la replicación viral, los intermedios contribuyen a ensamblar la maquinaria para producir nuevas partículas víricas, y los tardíos terminan el ensamblaje y empaquetado. Cada ola depende de la misma ARN polimerasa viral —la enzima que lee el ADN para producir ARN— pero factores auxiliares distintos indican a la polimerasa qué grupo de genes activar en cada fase. Hasta ahora, los científicos comprendían bastante bien el control de los genes tempranos, pero cómo el virus reconocía y activaba específicamente los genes intermedios seguía siendo un misterio.
Un ayudante en forma de anillo que necesita pareja
Los investigadores se centraron en una proteína de dos partes llamada VITF‑3, conocida por ser necesaria para activar los genes intermedios. Muchos organismos, incluidos los humanos, usan un par de proteínas denominadas TBP y TFIIB para guiar su ARN polimerasa al punto de inicio correcto en el ADN. El equipo mostró que VITF‑3 es una versión muy modificada de ese mismo par ancestral. Sin embargo, a diferencia de sus homólogas celulares, VITF‑3 por sí sola no se une al ADN. En cambio, sus dos subunidades se entrelazan para formar un anillo cerrado que es inerte frente al ADN a menos que la ARN polimerasa viral esté presente. Esto fue inesperado, porque en la mayoría de los sistemas el componente similar a TBP se une primero al ADN promotor y luego recluta a la polimerasa; aquí, el virus parece haber reprogramado el orden de los acontecimientos.
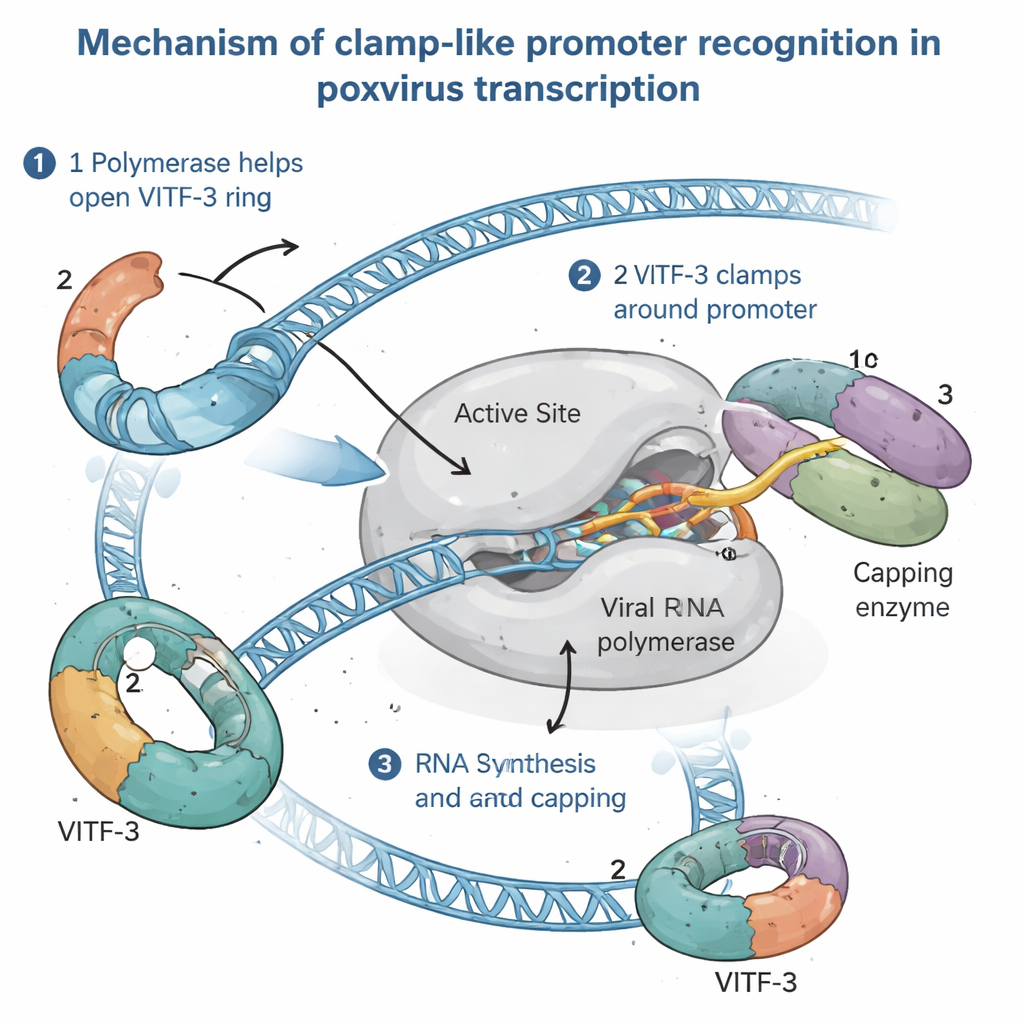
Ver la máquina de transcripción intermedia en acción
Para entender cómo funciona este montaje inusual, los autores aislaron el complejo de pre‑inicio intermedio completo —la ensambladura lista justo antes de que comience la síntesis de ARN— a partir de células humanas infectadas. Usando criomicroscopía electrónica de alta resolución, visualizaron el complejo a un detalle de aproximadamente 2,4 angstroms, lo bastante fino como para ver las cadenas laterales de aminoácidos y bases de ADN individuales. Las imágenes revelaron la ARN polimerasa viral sujetando el ADN promotor, con VITF‑3 formando un anillo apretado alrededor de un tramo rico en AT justo aguas arriba del sitio de inicio. Este anillo dobla bruscamente el ADN en unos 90 grados y lo introduce en una hendidura de la polimerasa. Al mismo tiempo, una enzima viral encargada del capado —responsable de añadir la caperuza protectora al extremo 5′ del ARN viral— está acoplada a la polimerasa, lista para modificar los nuevos transcritos en cuanto emergen.
Mecanismo de cargador de abrazadera tomado en espíritu
Combinando instantáneas estructurales con pruebas bioquímicas, el estudio propone que la ARN polimerasa viral carga activamente a VITF‑3 sobre el ADN, actuando como un «cargador de abrazadera». Primero, la polimerasa se une a un promotor intermedio y ayuda a abrir el anillo de VITF‑3. Luego, junto con la enzima de capado, cierra el anillo alrededor de la región rica en AT, fijando el complejo en su lugar. El ADN se desenrolla cerca del sitio de inicio, y la polimerasa lee directamente una señal corta de cuatro letras (un motivo TAAA) que marca exactamente dónde debe comenzar la síntesis de ARN. A medida que el ARN crece, sigue la misma trayectoria ocupada por parte de VITF‑3 en el complejo inicial, por lo que el ARN emergente probablemente desplaza a VITF‑3, permitiendo que la polimerasa abandone el promotor y continúe a lo largo del gen mientras VITF‑3 podría quedarse atrás para acelerar el reuso del mismo promotor.
Qué significa esto para comprender y atacar a los poxvirus
En términos sencillos, este trabajo muestra que el virus Vaccinia ha reconvertido un módulo universal de control génico en una abrazadera que solo sujeta el ADN cuando su propia ARN polimerasa se lo indica. Ese giro ingenioso permite al virus usar una enzima central para ejecutar tres programas de transcripción muy diferentes, simplemente intercambiando ayudantes específicos de cada fase. Dado que este tipo de factores está conservado en muchos poxvirus, incluidos patógenos humanos, el mecanismo recién revelado de cargador de abrazadera y el anillo único VITF‑3 ofrecen objetivos estructurales concretos para estrategias antivirales destinadas a interrumpir la capacidad del virus de temporizar y controlar sus genes durante la infección.
Cita: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Palabras clave: transcripción de poxvirus, virus Vaccinia, ARN polimerasa, reconocimiento de promotor, factores de transcripción