Clear Sky Science · es
Una célula sintética con autorreplicación de ADN integrada y biosíntesis de lípidos
Construir la vida desde cero
¿Qué convierte a una célula viva en algo más que una bolsa de moléculas? Una respuesta está en su capacidad para copiar sus instrucciones genéticas y fabricar su propia membrana protectora. Este estudio da un paso importante hacia la recreación de ese truco en el laboratorio. Los autores diseñan pequeñas burbujas de grasa, conocidas como liposomas, que pueden leer un fragmento de ADN, copiar ese ADN y producir nuevo material de membrana, todo dentro del mismo compartimento en miniatura. Su trabajo nos acerca a células artificiales que puedan crecer, adaptarse y, quizá algún día, evolucionar por sí solas.
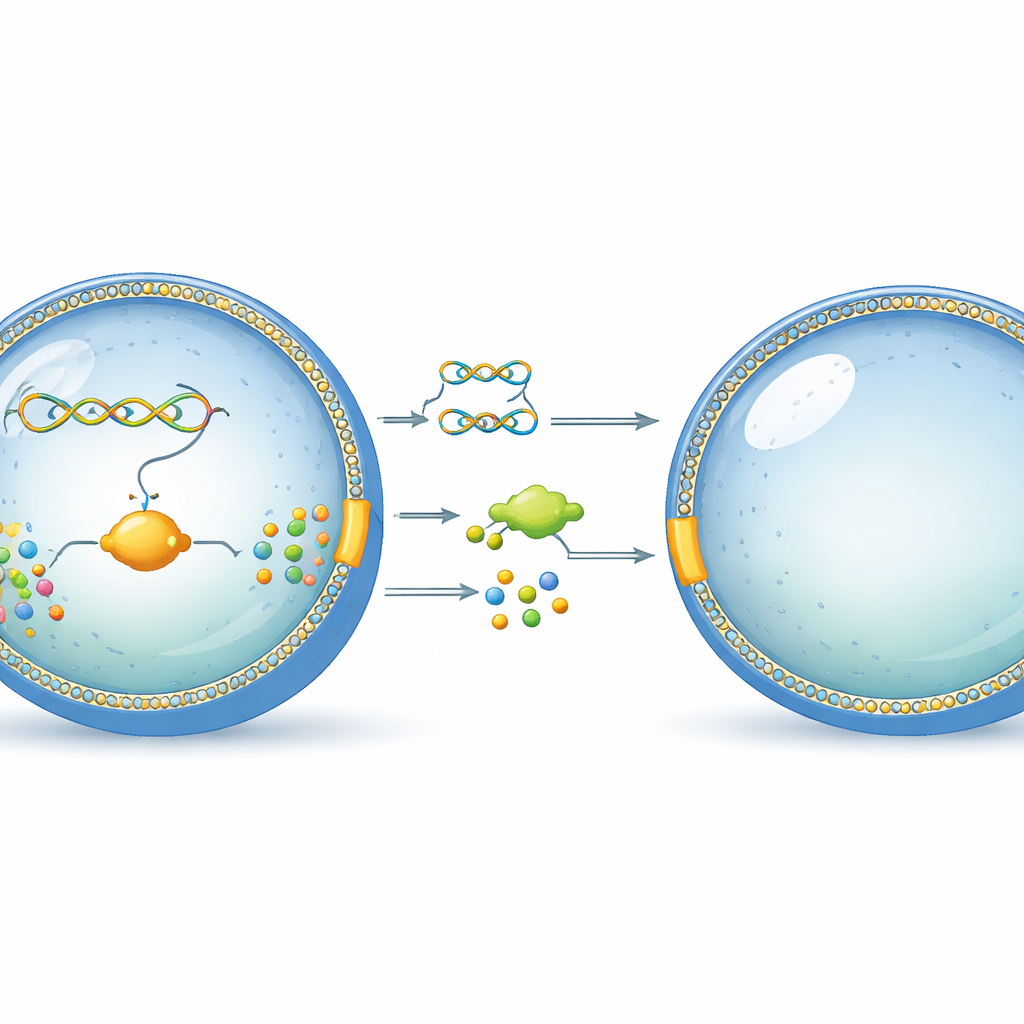
Una burbuja diminuta que actúa como una célula
Los investigadores parten de burbujas simples, del tamaño de una célula, hechas de fosfolípidos, el mismo tipo de moléculas que forman la envoltura exterior de las células reales. En estas burbujas introducen una hebra de ADN cuidadosamente diseñada y un conjunto de máquinas celulares purificadas capaces de leer el ADN y fabricar proteínas. Este montaje, llamado sistema de expresión sin célula, actúa como el núcleo reducido de una célula viva, capaz de transformar información genética en moléculas funcionales sin la presencia de ningún organismo vivo. La idea clave es colocar todo dentro del liposoma para que el programa genético y sus productos permanezcan juntos, al igual que en una célula natural.
Un programa de ADN a medida con dos funciones
En el centro de su célula sintética está una molécula de ADN construida a medida que los autores denominan DNArep-PLsyn. Este ADN contiene instrucciones para seis proteínas. Dos de ellas proceden de un virus que infecta bacterias y, juntas, son capaces de copiar el propio ADN, proporcionando un módulo de autorreplicación integrado. Las otras cuatro proceden de la bacteria intestinal E. coli y forman una cadena de reacciones que convierte materiales de partida simples en un fosfolípido específico usado en membranas. Para ensamblar este genoma inusual, el equipo tuvo que coser fragmentos de ADN en tubos de ensayo y en células de levadura, y luego convertir el resultado en una hebra de ADN lineal que la maquinaria viral de copia pueda reconocer y replicar.
Generar y probar la actividad sintética
Una vez que el ADN y la maquinaria de fabricación de proteínas están sellados dentro de los liposomas, las burbujas se calientan a diferentes temperaturas y se dejan funcionar. El equipo comprueba lo ocurrido usando marcadores fluorescentes: un tinte se ilumina cuando se une al ADN, revelando cuánto ADN está presente, y otro se adhiere al nuevo fosfolípido si este se produce e inserta en la membrana. Con citometría de flujo y microscopía de alta resolución pueden analizar decenas de miles de vesículas individuales. Encuentran que muchas burbujas copian con éxito el genoma, muchas otras fabrican nuevos bloques de construcción de membrana, y una fracción menor pero significativa logra hacer ambas cosas a la vez. Pruebas adicionales mediante cuantificación de ADN y espectrometría de masas confirman que el genoma de longitud completa se amplifica y que las nuevas moléculas de fosfolípidos se sintetizan realmente, aunque en cantidades modestas.
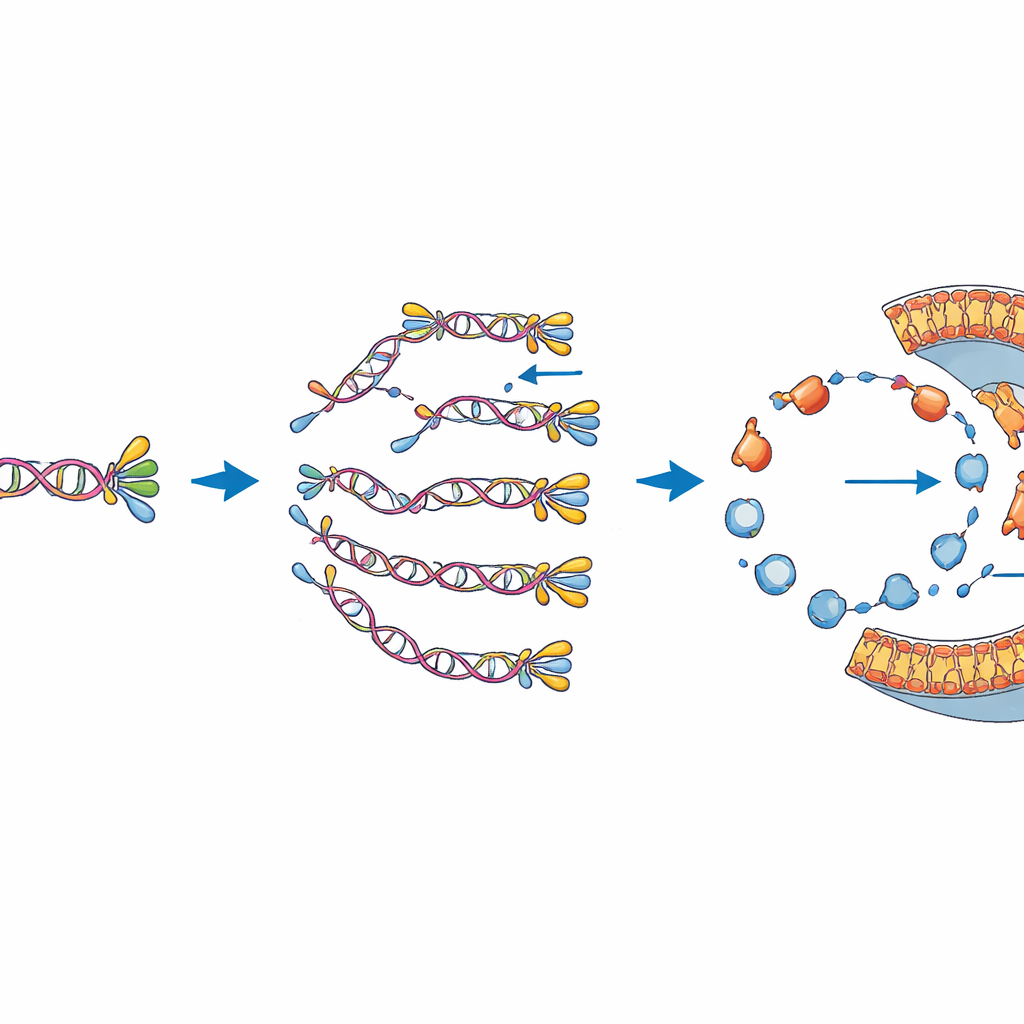
Equilibrar dos tareas esenciales
Los autores investigan entonces cómo se influyen mutuamente estas dos funciones. Al activar o desactivar la química de copiado de ADN o de fabricación de membrana mediante los ingredientes requeridos, muestran que cada proceso puede operar en gran medida sin perturbar al otro. Sin embargo, cuando ambos módulos están codificados en el mismo ADN, el lado de la síntesis de membrana resulta más frágil: menos vesículas muestran esta actividad en comparación con vesículas que llevan solo los genes relacionados con los lípidos. De manera similar, el genoma combinado no se copia tan eficientemente como una versión más pequeña que contiene únicamente los genes de replicación de ADN. Esto sugiere que incluso en este sistema reducido hay competencia por recursos compartidos y por el espacio físico en el ADN, evocando compensaciones observadas en células reales.
Prepararse para la evolución en el tubo de ensayo
Para avanzar más allá de una demostración única, el equipo diseña su sistema de modo que, en principio, pueda mejorarse mediante evolución. Generan versiones de ADN más limpias y fiables usando plásmidos cultivados en levadura y bacterias, lo que aumenta la fracción de células sintéticas totalmente funcionales. También muestran que es posible encapsular, seleccionar y recuperar genomas de vesículas que realizan tanto el copiado de ADN como la síntesis de membrana. Esto prepara el terreno para futuros ciclos en los que genomas ligeramente diferentes compitan, y aquellos que funcionen mejor sean enriquecidos y replicados.
Por qué esto importa para entender la vida
En términos cotidianos, los investigadores han construido una burbuja microscópica que puede leer su propia receta, hacer más copias de esa receta y usarla para remendar y ampliar su piel exterior. Aunque estas células sintéticas aún no pueden crecer mucho o dividirse como los organismos vivos, el trabajo demuestra que rasgos esenciales de la vida—almacenamiento de información, autorreplicación y autoconstrucción básica—pueden combinarse en un paquete simple y controlable. Esto sienta una base importante para explorar cómo pudo empezar la vida a partir de química no viva y para diseñar células artificiales que realicen tareas útiles, desde liberación inteligente de fármacos hasta pequeñas fábricas autorrenovables.
Cita: Restrepo Sierra, A.M., Ramirez Gomez, F., van Tongeren, M. et al. A synthetic cell with integrated DNA self-replication and lipid biosynthesis. Nat Commun 17, 2727 (2026). https://doi.org/10.1038/s41467-026-69531-9
Palabras clave: células sintéticas, autorreplicación de ADN, biosíntesis de lípidos, vida artificial, biología de abajo hacia arriba