Clear Sky Science · es
Terapia térmica intersticial con láser y pembrolizumab adyuvante en astrocitoma de alto grado recurrente: ensayo de Fase 1/Fase 2b aleatorizado
Por qué importa este estudio sobre cáncer cerebral
El astrocitoma de alto grado recurrente, incluido el glioblastoma, es uno de los cánceres cerebrales más letales, y los tratamientos actuales rara vez lo controlan durante mucho tiempo. Este estudio prueba una estrategia en dos pasos que utiliza el calor de un láser para destruir tejido tumoral y abrir las defensas del cerebro, seguida de un fármaco inmunológico que ayuda a los linfocitos T del propio organismo a atacar el cáncer que quede. Para pacientes y familias ante este diagnóstico, el trabajo explora si un procedimiento mínimamente invasivo puede convertir un cáncer casi no reactivo en uno que finalmente responda a la inmunoterapia.
Una nueva forma de abordar tumores cerebrales resistentes
Los pacientes de este ensayo presentaban astrocitomas de alto grado que habían recurrido tras la terapia estándar, que suele incluir cirugía, radiación y quimioterapia. Los investigadores se centraron en dos herramientas. La primera, la terapia térmica intersticial con láser (LITT), es un procedimiento por orificio en el que una sonda fina se introduce en el tumor guiada por resonancia magnética y se usa para calentar y destruir tejido canceroso mientras se preserva gran parte del cerebro circundante. La segunda herramienta es pembrolizumab, un fármaco de inmunoterapia muy utilizado que bloquea PD-1, un “freno” molecular que a menudo impide que los linfocitos T ataquen los tumores. Intentos previos de usar estos fármacos por sí solos en estos cánceres cerebrales habían sido decepcionantes. El equipo, por tanto, preguntó si usar primero el láser podría preparar el tumor y el sistema inmune para responder mejor al pembrolizumab. 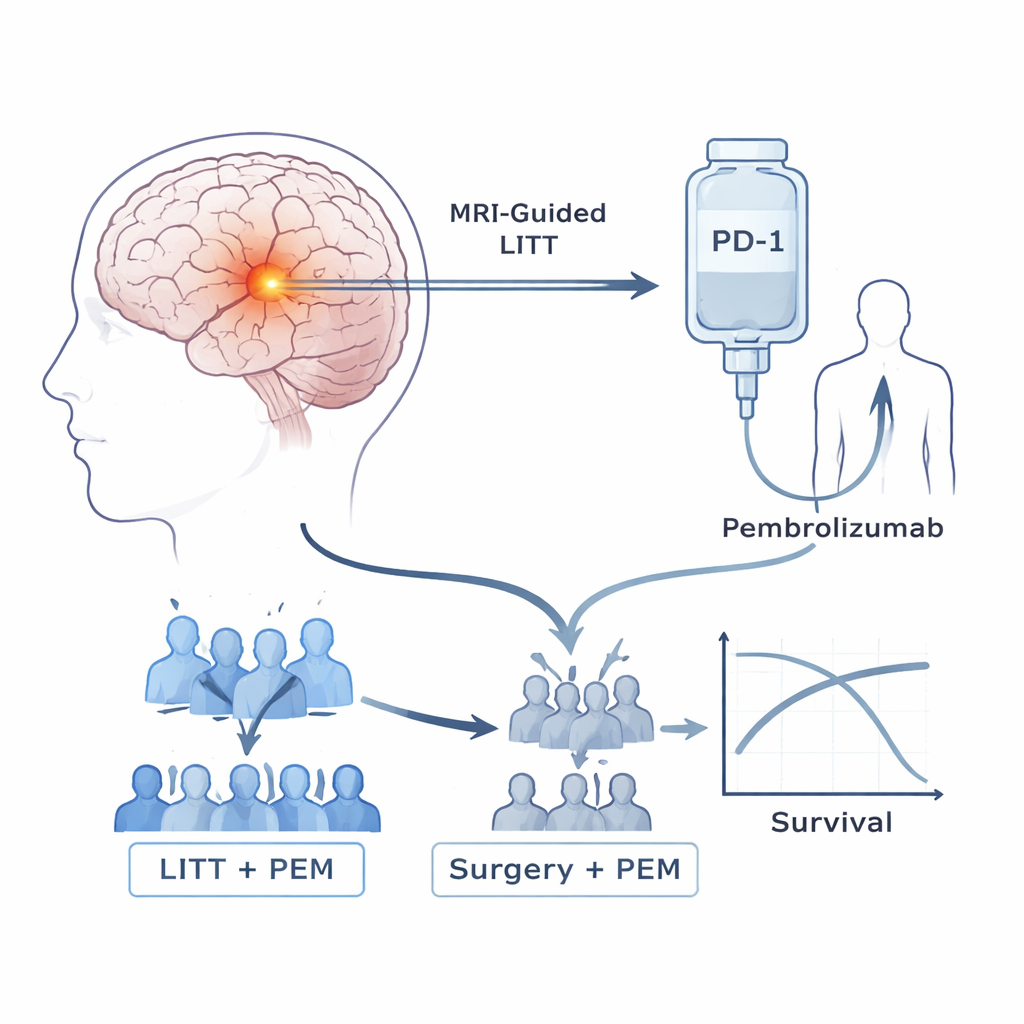
Cómo se condujo el ensayo clínico
El estudio comenzó con una fase pequeña de seguridad, que mostró que los pacientes podían recibir pembrolizumab de forma segura cada tres semanas tras LITT, sin efectos adversos limitantes de la dosis. Luego pasó a un ensayo de Fase 2b. Inicialmente, los pacientes se asignaron aleatoriamente a uno de dos grupos: LITT seguido de pembrolizumab, o una cirugía cerebral repetida convencional sin láser, seguida de pembrolizumab. A medida que la evidencia externa creció indicando que la cirugía más inmunoterapia ofrecía poco beneficio por sí sola, un comité independiente revisó los resultados tempranos de este ensayo. Al ver señales de que el grupo sin láser se comportaba peor mientras que el grupo LITT parecía vivir más, detuvieron la aleatorización y todos los pacientes posteriores recibieron la combinación de láser y fármaco.
Qué ocurrió con la supervivencia y el control tumoral
Entre 39 pacientes que recibieron el tratamiento según lo planeado, los tratados con LITT más pembrolizumab vivieron notablemente más que los que recibieron cirugía más pembrolizumab. La mediana de supervivencia global fue de aproximadamente 11,8 meses con el enfoque combinado LITT, frente a 5,2 meses con cirugía sola, y ninguno de los pacientes del grupo de cirugía estaba vivo a los 18 meses comparado con el 42% de los del grupo LITT. El tiempo hasta que el tumor volvió a crecer también mejoró, de 1,6 meses en el grupo de cirugía a 4,5 meses con LITT. Alrededor del 27% de los pacientes tratados con LITT presentaron una reducción medible de sus tumores y el 70% consiguió al menos un control temporal de la enfermedad, mientras que todos los pacientes sometidos a cirugía no láser más pembrolizumab experimentaron progresión. Los efectos secundarios del tratamiento combinado fueron en su mayoría leves y manejables, con algunos casos de diarrea, debilidad muscular y elevación de enzimas hepáticas, pero no hubo muertes relacionadas con el tratamiento.
Qué hacía el sistema inmune
Para entender por qué la combinación podría funcionar, los científicos examinaron detenidamente las células sanguíneas a lo largo del tiempo usando secuenciación de ARN unicelular y seguimiento de receptores de células T. Tras LITT, observaron que un grupo específico de células inmunitarias innatas, llamadas monocitos no clásicos, pasó a un estado más activo vinculado a migración, inflamación e interacción con linfocitos T—cambios no vistos tras la cirugía estándar. Cuando se inició pembrolizumab, los pacientes que sobrevivieron más mostraron fuertes oleadas de activación y expansión clonal de células T CD8, lo que significa que muchos linfocitos T idénticos dirigidos contra los mismos antígenos se multiplicaron. Estas células T tendieron a pasar a estados de memoria y efector capaces de reconocer y matar células tumorales, en lugar de volverse exhaustas e ineficaces. Los supervivientes a largo plazo también mostraron una disminución de IDO-1, una molécula asociada a la supresión inmune, lo que sugiere que la combinación puede aliviar múltiples capas de frenado inmunitario. 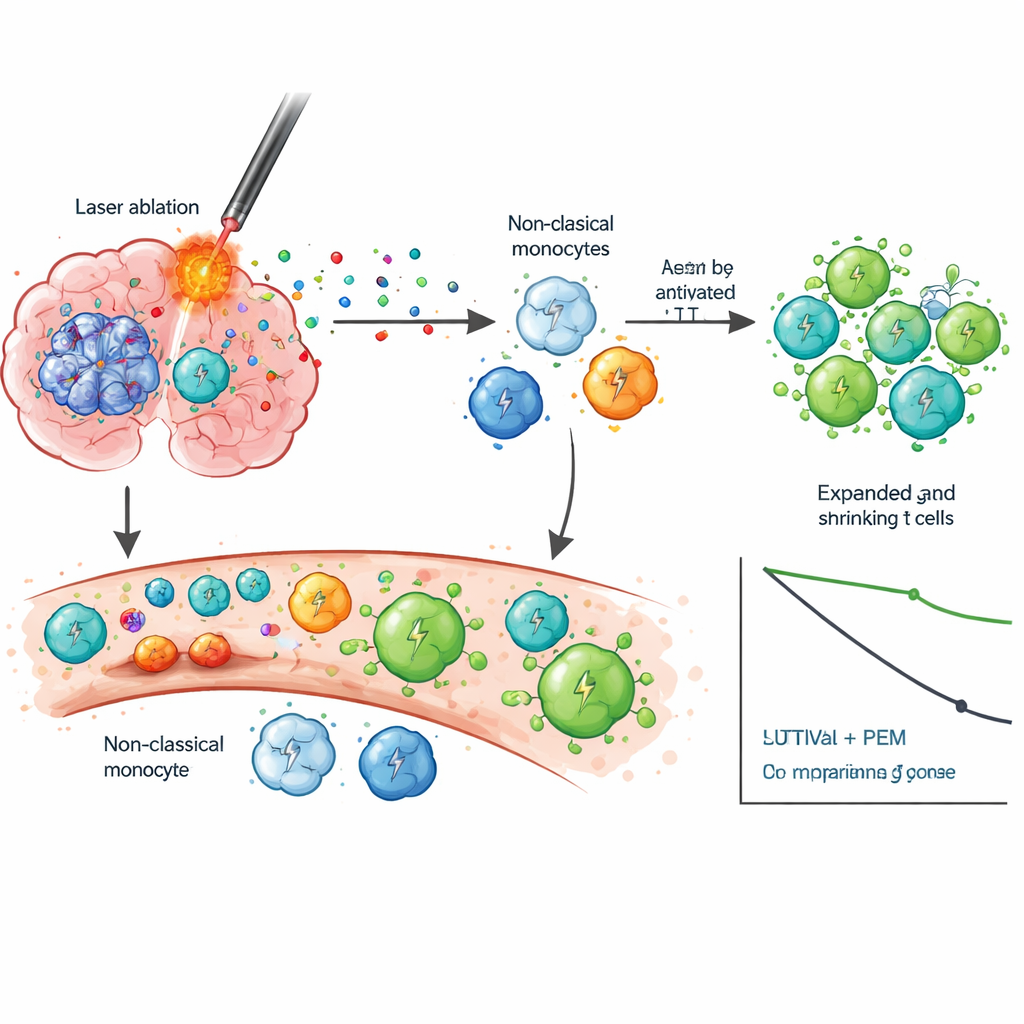
Qué podría significar esto para los pacientes
Para personas con astrocitoma de alto grado recurrente, este trabajo sugiere que usar ablación con láser guiada por RM para reducir la masa tumoral, aflojar brevemente la barrera hematoencefálica y verter fragmentos tumorales a la circulación puede preparar el terreno para que la inmunoterapia funcione donde normalmente fracasa. Al encender una “señal” para el sistema inmune y luego quitar el freno PD-1 con pembrolizumab, la combinación parece generar respuestas de células T más duraderas y prolongar la supervivencia en un cáncer con muy pocas opciones. Dado que el estudio fue relativamente pequeño y la aleatorización terminó pronto, los autores subrayan que aún se necesitan ensayos más amplios y controlados. Aun así, los resultados apuntan a una estrategia prometedora: emparejar la destrucción física del tumor, dirigida con precisión, con fármacos inmunológicos para convertir un tumor cerebral frío y resistente en uno que el cuerpo finalmente pueda reconocer y combatir.
Cita: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Palabras clave: glioblastoma, ablación con láser, pembrolizumab, inmunoterapia, tumor cerebral