Clear Sky Science · es
La señalización excesiva de FGFR3 en la acondroplasia altera el recambio de condrocitos de la zona en reposo mediante la vía CREB
Por qué importa este estudio sobre el crecimiento óseo
La acondroplasia es la causa genética más frecuente de enanismo de extremidades cortas. Afecta no solo la estatura, sino también la salud de la columna, la movilidad y la calidad de vida. Los tratamientos actuales ayudan, pero no restauran por completo el crecimiento óseo. Este estudio emplea un modelo de ratón sofisticado para descubrir una zona del hueso en crecimiento que había pasado desapercibida y señala un nuevo interruptor de señalización, llamado CREB, como un objetivo prometedor para futuras terapias.
Cómo crecen los huesos sanos en longitud
Los huesos largos, como el fémur del muslo, se alargan en las placas de crecimiento situadas cerca de sus extremos. Estas placas de crecimiento están organizadas en tres capas principales de células cartilaginosas. En la parte superior se encuentra la zona en reposo, donde las células actúan como un reservorio de tipo células madre, dividiéndose lentamente y enviando células hijas hacia abajo. Debajo, la zona proliferativa contiene células que se dividen rápidamente y se apilan en columnas ordenadas que impulsan el alargamiento. Más adelante, la zona hipertrófica alberga células maduras y agrandadas que ayudan a guiar la formación de nuevo hueso. El equilibrio entre estas zonas mantiene el crecimiento óseo a la velocidad y forma adecuadas.
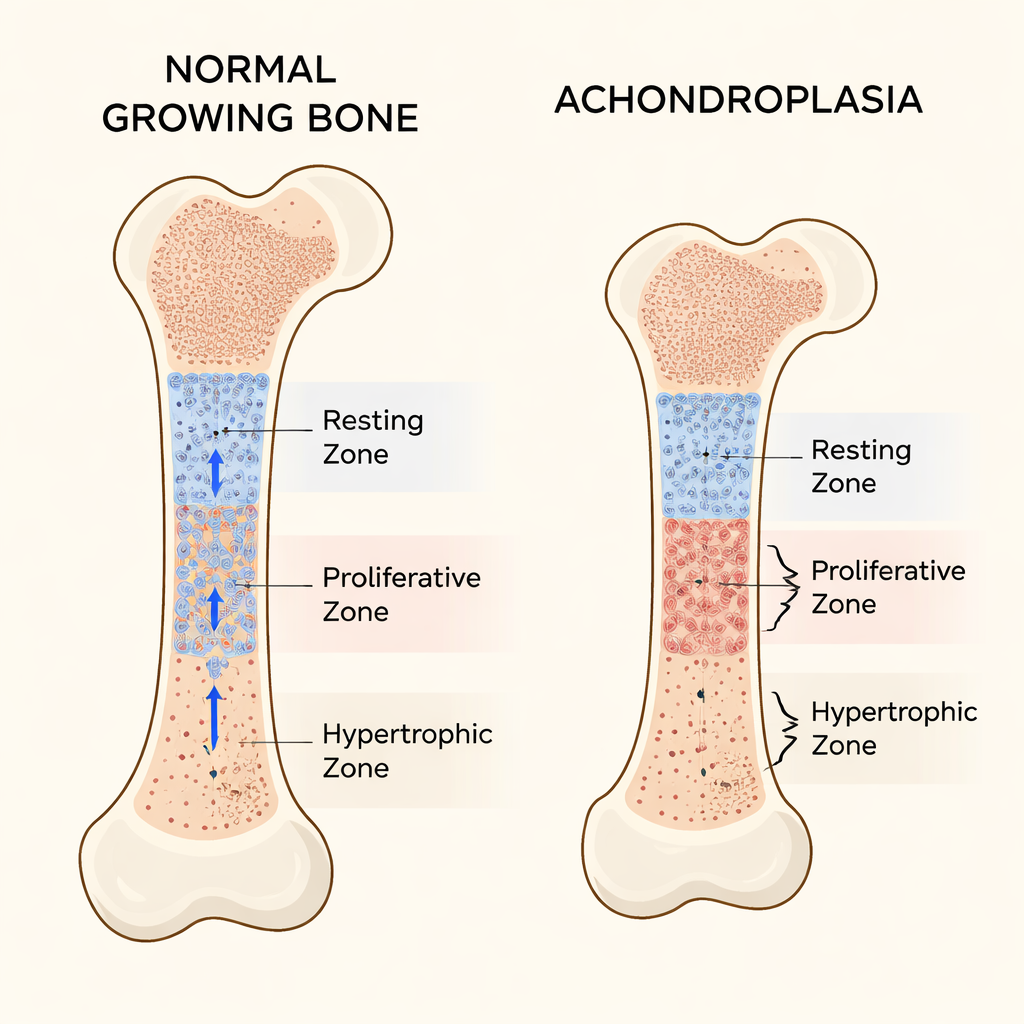
Qué falla en la acondroplasia
En la mayoría de las personas con acondroplasia, una única mutación en el gen FGFR3 vuelve su receptor hiperactivo, poniendo freno al crecimiento óseo. Trabajos previos mostraron que esta señalización ralentiza la división celular en la zona proliferativa y bloquea la ampliación final de las células en la zona hipertrófica. Usando ratones diseñados para portar la mutación humana de la acondroplasia, los autores confirmaron extremidades severamente cortas y placas de crecimiento acortadas. Pero mediciones detalladas revelaron algo que había sido en gran parte pasado por alto: la propia zona en reposo se volvía inusualmente gruesa. En lugar de comportarse como un reservorio estable y bien regulado de células madre, esta región se expandió y contenía células pobres en la matriz cartilaginosa normal.
Las células de la zona en reposo pierden su comportamiento “tipo madre”
Para entender esta expansión, el equipo siguió cómo se dividían y desplazaban las células de la placa de crecimiento a lo largo del tiempo. En ratones normales, las células de la zona en reposo se dividían rara vez y sus descendientes migraban hacia abajo en columnas rectas para rellenar la zona proliferativa. En los ratones mutantes, muchas más células de la zona en reposo se dividían lentamente y permanecían en su lugar, acumulando una capa congestionada que no alimentaba correctamente las zonas inferiores. El trazado de linaje con etiquetas genéticas multicolores mostró que las columnas clonales eran cortas y desorganizadas, con células hijas que se dispersaban en direcciones aleatorias en lugar de formar pilas ordenadas. Marcadores de identidad tipo célula madre, como la proteína CD73, se perdieron en la zona en reposo expandida, lo que sugiere que la hiperactividad de FGFR3 había corrompido el nicho normal de células madre.
Un nuevo culpable en la señalización: CREB
Luego, los investigadores utilizaron secuenciación de ARN a nivel de célula única para perfilar miles de células individuales de la placa de crecimiento. Identificaron un grupo distinto que coincidía con la zona en reposo expandida y que era rico en un gen llamado Spon1, entre otros. El análisis de vías destacó la activación de CREB, una proteína que activa genes cuando se fosforila. La microscopía mostró que las células de la zona en reposo en los ratones mutantes expresaban fuertemente CREB activado y su coactivador CBP, junto con altos niveles de FGFR3 y moléculas aguas abajo como STAT5. En cultivo celular, estimular la vía FGFR3 aumentó la actividad de CREB y elevó SPONDIN1 (la proteína SPON1), mientras que bloquear FGFR3 o CREB redujo esas señales. Esto sitúa a CREB como un relevo clave entre el receptor hiperactivo en la superficie celular y el comportamiento defectuoso de las células de la zona en reposo.
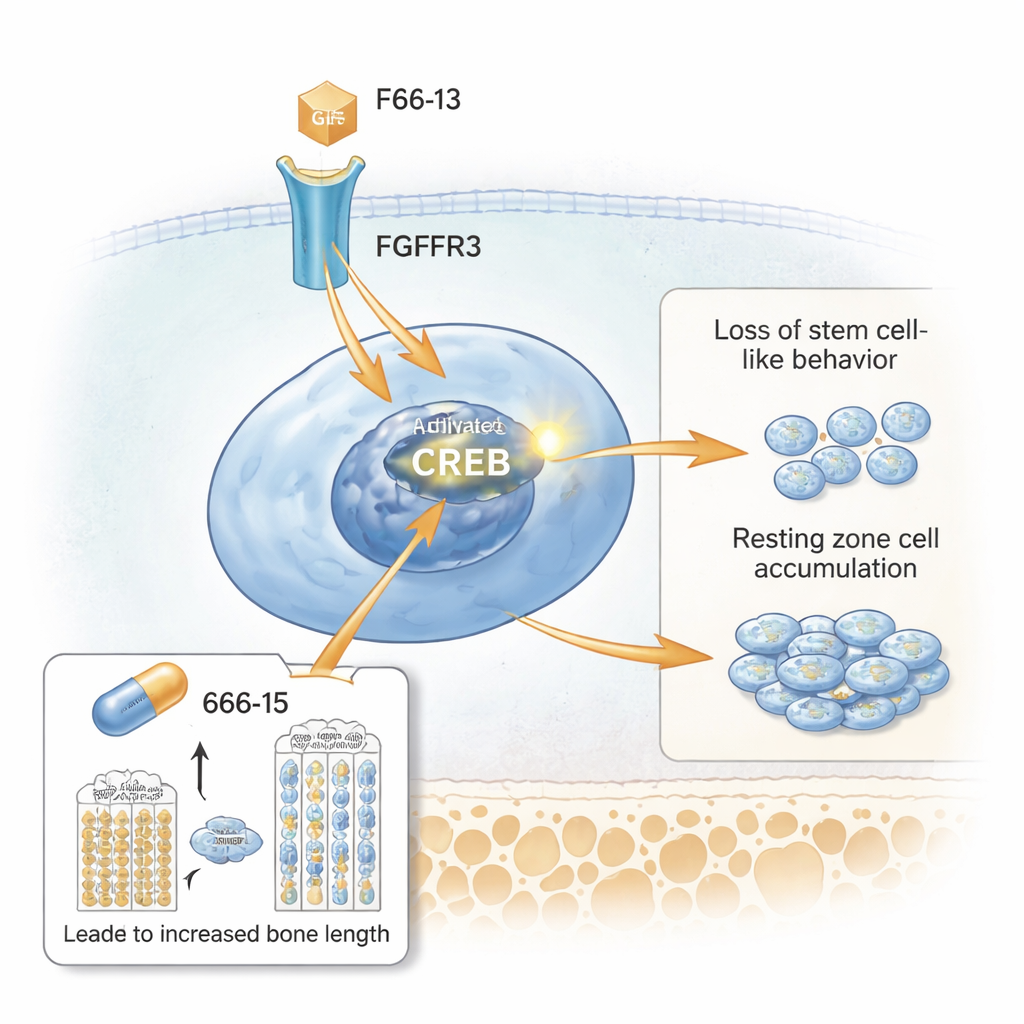
Poniendo a prueba un fármaco que reduce CREB
Finalmente, el equipo planteó si atenuar CREB podría aliviar los problemas de crecimiento. Trataron a ratones modelo de acondroplasia con un inhibidor de CREB de pequeña molécula, llamado 666-15, durante el periodo de crecimiento rápido postnatal. En comparación con los ratones mutantes no tratados, los que recibieron 666-15 tuvieron mayor peso corporal y fémures más largos. Sus placas de crecimiento se veían más normales: la zona en reposo se adelgazó, las zonas proliferativa e hipertrófica recuperaron altura y reaparecieron proteínas de la matriz cartilaginosa. Los marcadores de señalización CREB hiperactiva, incluyendo fosfo-CREB, SPONDIN1 y STAT5, disminuyeron en la zona en reposo, mientras que el marcador tipo célula madre CD73 reapareció. Es importante que el mismo fármaco tuvo poco efecto en ratones control sanos a la dosis probada, lo que sugiere que actúa principalmente cuando CREB está anormalmente elevado.
Qué significa esto para tratamientos futuros
El estudio muestra que en la acondroplasia, la FGFR3 hiperactiva hace más que frenar la división y el agrandamiento celular; también descarrila la silenciosa zona en reposo, de tipo célula madre, activando CREB. Esta alteración priva a las capas inferiores de la placa de crecimiento de nuevas células y contribuye a la acortación ósea. Fármacos existentes como el vosoritide actúan principalmente sobre otras vías en las zonas proliferativa e hipertrófica y solo restauran parcialmente la longitud ósea. Al añadir a CREB a la lista de dianas —especialmente en la zona en reposo—, futuras terapias combinadas podrían normalizar con más amplitud el crecimiento en niños con acondroplasia.
Cita: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Palabras clave: acondroplasia, FGFR3, placa de crecimiento, células madre del cartílago, señalización CREB