Clear Sky Science · es
Densidad de carga del metal hidratado como descriptor universal que explica variaciones mecanísticas en la activación de periodato para la degradación de contaminantes
Limpiar el agua con química inteligente
Muchos medicamentos y productos químicos industriales pasan por alto las plantas convencionales de tratamiento de agua y acaban en ríos y en el agua potable. Este estudio explora una vía prometedora para descomponer esos contaminantes persistentes usando un agente oxidante común, el periodato, y muestra que una propiedad sencilla de los iones metálicos en agua puede predecir cuánto —y con qué seguridad— funcionará esta química. Comprender esta regla podría ayudar a los ingenieros a diseñar sistemas de tratamiento más limpios y eficientes para aguas reales y diversas.
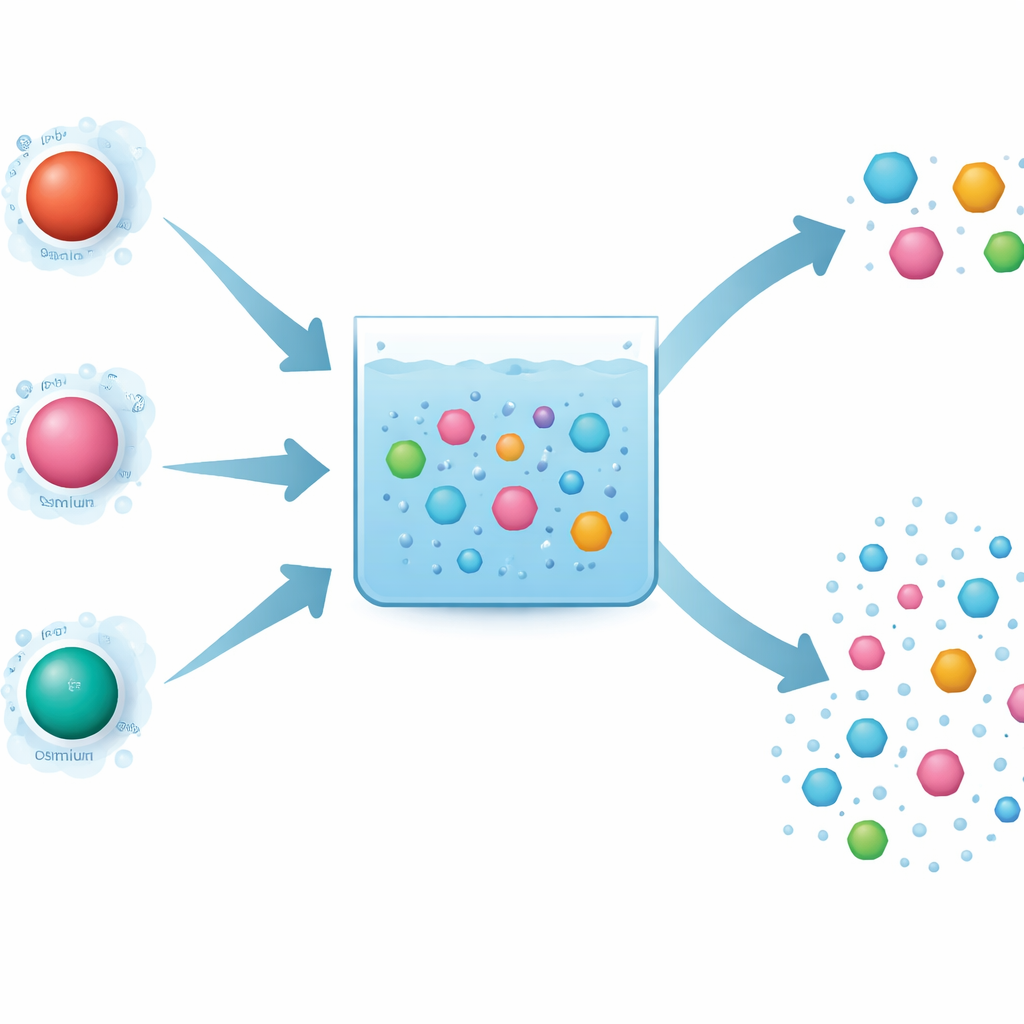
Por qué la elección del metal importa para la degradación de contaminantes
Los procesos avanzados de oxidación emplean especies reactivas potentes para descomponer moléculas orgánicas. El periodato es uno de estos oxidantes y puede “activarse” mediante iones metálicos disueltos. Los autores compararon tres metales estrechamente relacionados —hierro, rutenio y osmio— que pertenecen a la misma columna de la tabla periódica y podrían esperarse que se comporten de forma similar. Los tres pueden activar el periodato y ayudar a destruir un contaminante de prueba, la carbamazepina. Sin embargo, los experimentos mostraron diferencias llamativas: el rutenio actuó extremadamente rápido, el hierro fue más lento y el osmio quedó en un punto intermedio. Más sorprendente aún, el osmio eliminó una amplia variedad de contaminantes con poca preferencia, mientras que el hierro y el rutenio fueron selectivos, atacando algunas moléculas mucho más fácilmente que otras.
Dos vías químicas muy distintas
Para desentrañar el origen de estas diferencias, el equipo siguió qué especies oxidantes de vida corta aparecían en cada sistema metal–periodato. Con hierro y rutenio, los protagonistas dominantes fueron unidades “metal–oxígeno” que actúan como herramientas de precisión, transfiriendo un átomo de oxígeno directamente a sitios específicos de un contaminante. Estas vías tendían a formar productos epóxido —estructuras cíclicas que incorporan un solo átomo de oxígeno—, lo que indica que la reacción es bastante selectiva. En el sistema con osmio, sin embargo, los actores principales fueron radicales hidroxilo, fragmentos extremadamente reactivos que atacan casi cualquier molécula orgánica cercana, dando lugar a productos hidroxilados y pequeños fragmentos con anillos abiertos. Ensayos con sondas químicas y espectroscopía de captura de espines confirmaron que los radicales hidroxilo y especies reactivas de oxígeno relacionadas, no unidades osmio–oxígeno de alto estado de oxidación, impulsan la mayor parte de la destrucción de contaminantes cuando está presente el osmio.
Cómo las condiciones del agua moldean las reacciones
El equipo también examinó cómo el pH y los componentes naturales del agua influyen en estos procesos. Para el osmio, la eliminación de contaminantes se fortaleció a medida que el agua se volvía más alcalina, donde la coordinación de iones hidroxilo adicionales alrededor del metal facilita el movimiento de electrones y la formación de radicales. Sin embargo, a dosis altas de metal u oxidante, el sistema con osmio se “autoapaga” porque los radicales recién formados son consumidos por el exceso de reactivos en lugar de por los contaminantes. La materia orgánica natural, que a menudo interfiere con las reacciones de oxidación, tuvo sorprendentemente poco impacto en la degradación impulsada por osmio, lo que sugiere que la vía radicalaria sigue siendo robusta en aguas realistas. En contraste, el hierro y el rutenio funcionaron mejor en condiciones ácidas, y la materia orgánica natural suprimió fuertemente su actividad al atrapar las oxidantes clave metal–oxígeno.
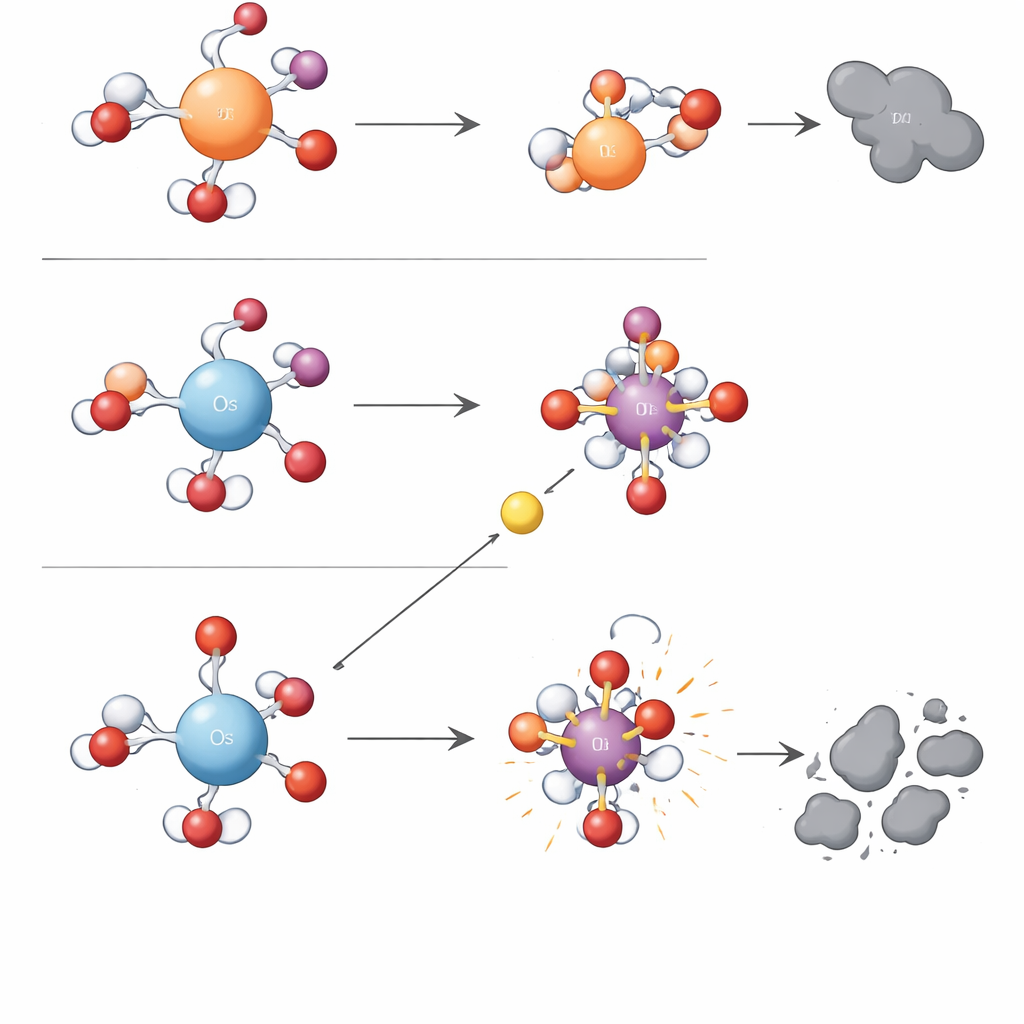
Una regla simple de carga detrás de una química compleja
Para ir más allá del ensayo y error, los investigadores recurrieron a cálculos cuántico‑químicos. Encontraron que una sola característica electrónica —la densidad de carga positiva en el centro metálico hidratado— podía explicar la división entre los dos tipos de reacción. El osmio en agua presenta una densidad de carga positiva más concentrada que el hierro o el rutenio. Este centro fuertemente positivo se aferra con fuerza a su átomo de oxígeno ligado, haciendo que la unidad metal–oxígeno sea estable pero poco reactiva hacia la transferencia directa de oxígeno. Al mismo tiempo, la fuerte atracción sobre el agua y los iones cercanos reduce la barrera energética para pasos de un solo electrón que, en última instancia, rompen un enlace de oxígeno en el periodato y liberan radicales hidroxilo. Metales con menor densidad de carga, como el hierro y el rutenio, retienen los electrones de forma diferente, favoreciendo la formación y el uso de oxidantes metal–oxígeno selectivos en lugar de radicales libres. Los autores denominan a esta idea organizadora el “Mecanismo de Control por Densidad de Carga” y muestran que también racionaliza tendencias informadas para otros metales, como el manganeso.
Diseñar mejor el tratamiento de aguas a partir de una sola perilla
Al vincular un conjunto difícil de observaciones con un descriptor simple —la densidad de carga de un metal rodeado de agua— este trabajo ofrece una hoja de ruta para adaptar procesos avanzados de oxidación. Los metales de alta densidad de carga deberían favorecer la degradación amplia basada en radicales de mezclas complejas de contaminantes, especialmente en aguas alcalinas o ricas en materia orgánica. Los metales de menor densidad de carga son más adecuados cuando se desea una oxidación selectiva y más suave, por ejemplo para transformar contaminantes específicos sin reaccionar en exceso con todo lo demás presente. En términos prácticos, esto significa que químicos e ingenieros pueden evaluar o diseñar catalizadores para la purificación del agua ajustando cuán fuertemente los centros metálicos retienen carga en su entorno acuoso, en lugar de optimizar cada sistema por ensayo y error.
Cita: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Palabras clave: procesos avanzados de oxidación, activación del periodato, tratamiento de aguas, catálisis con metales de transición, radicales hidroxilo