Clear Sky Science · es
Flujo de trabajo de proteómica química de alto rendimiento para perfilar la dinámica de la citrulinación proteica
Por qué importa cambiar los componentes de las proteínas
Nuestras células ajustan constantemente el comportamiento de las proteínas añadiendo pequeñas modificaciones químicas después de su síntesis. Una de esas modificaciones, llamada citrulinación, cambia sutilmente la carga de un aminoácido común y puede remodelar el plegamiento de las proteínas, su unión al ADN o sus interacciones con otras moléculas. Estos pequeños retoques se asocian cada vez más con enfermedades autoinmunes, infecciones, cáncer y funciones cerebrales, pero son notoriamente difíciles de detectar. Este estudio presenta un procedimiento de laboratorio de alto rendimiento que por fin permite cartografiar la citrulinación en miles de proteínas, revelando cuándo y dónde aparece en tejidos y células inmunitarias.
Un interruptor oculto en las proteínas
La citrulinación ocurre cuando enzimas llamadas PADs modifican químicamente la arginina, eliminando su carga positiva. Ese cambio aparentemente pequeño puede aflojar el empaquetamiento del ADN, alterar la rigidez de proteínas estructurales o modificar el reconocimiento de nuestros tejidos por el sistema inmune. La citrulinación anómala se ha implicado en artritis reumatoide, trastornos neurodegenerativos, infecciones virales y cáncer. Sin embargo, las proteínas citrulinadas son poco abundantes y pueden confundirse fácilmente con otras modificaciones más comunes, por lo que los métodos estándar de espectrometría de masas a menudo no las detectan. El resultado es que los investigadores solo disponían de una visión fragmentada del “citrulinoma” del organismo: el conjunto completo de proteínas citrulinadas.
Una estrategia de etiquetado y captura en dos pasos
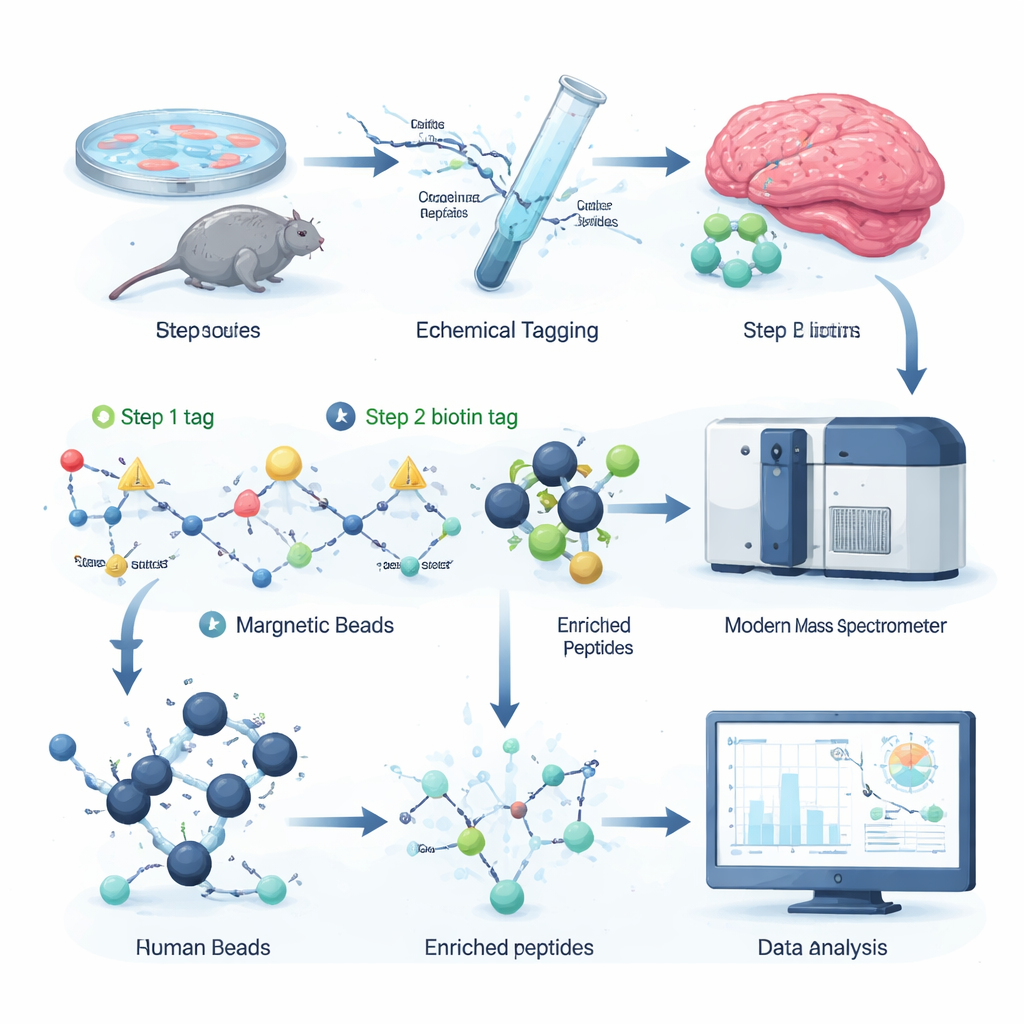
Los autores idearon una estrategia de etiquetado químico que une selectivamente un “asa” removible a los sitios citrulinados en péptidos, los fragmentos de proteínas que analiza la espectrometría de masas. En el primer paso, una pequeña molécula reactiva reconoce la citrulina e instala una etiqueta diminuta. En el segundo, se añade por 'click' una etiqueta más grande con biotina, lo que permite extraer los péptidos etiquetados de una mezcla compleja con perlas de estreptavidina, una herramienta bioquímica habitual. Un tratamiento químico suave corta la parte voluminosa de la etiqueta, dejando un pequeño desplazamiento de masa bien definido que el espectrómetro de masas puede detectar con facilidad. Dado que todos los reactivos están disponibles comercialmente y el protocolo cabe en placas de 96 pocillos, el flujo de trabajo es rápido, escalable y compatible con los montajes proteómicos existentes.
Viendo más del citrulinoma
Al añadir péptidos citrulinados conocidos a extractos celulares y diluirlos sistemáticamente, el equipo demostró que su estrategia de enriquecimiento aumenta la señal de los péptidos citrulinados más de diez veces, incluso cuando representan menos de uno de cada mil moléculas. En muestras complejas, el número de sitios citrulinados detectados y sus intensidades medidas aumentaron de forma drástica tras el enriquecimiento. Al aplicar el método a tejido cerebral de ratón se identificaron entre dos y tres veces más sitios de citrulinación distintos que con un enfoque previo de última generación, incluidos muchos en la proteína básica de la mielina, que aísla las fibras nerviosas, y en proteínas implicadas en la comunicación sináptica. Esto sugiere que la citrulinación puede influir tanto en la señalización de las neuronas como en el mantenimiento del cableado cerebral.
Células inmunitarias que lanzan redes proteicas pegajosas
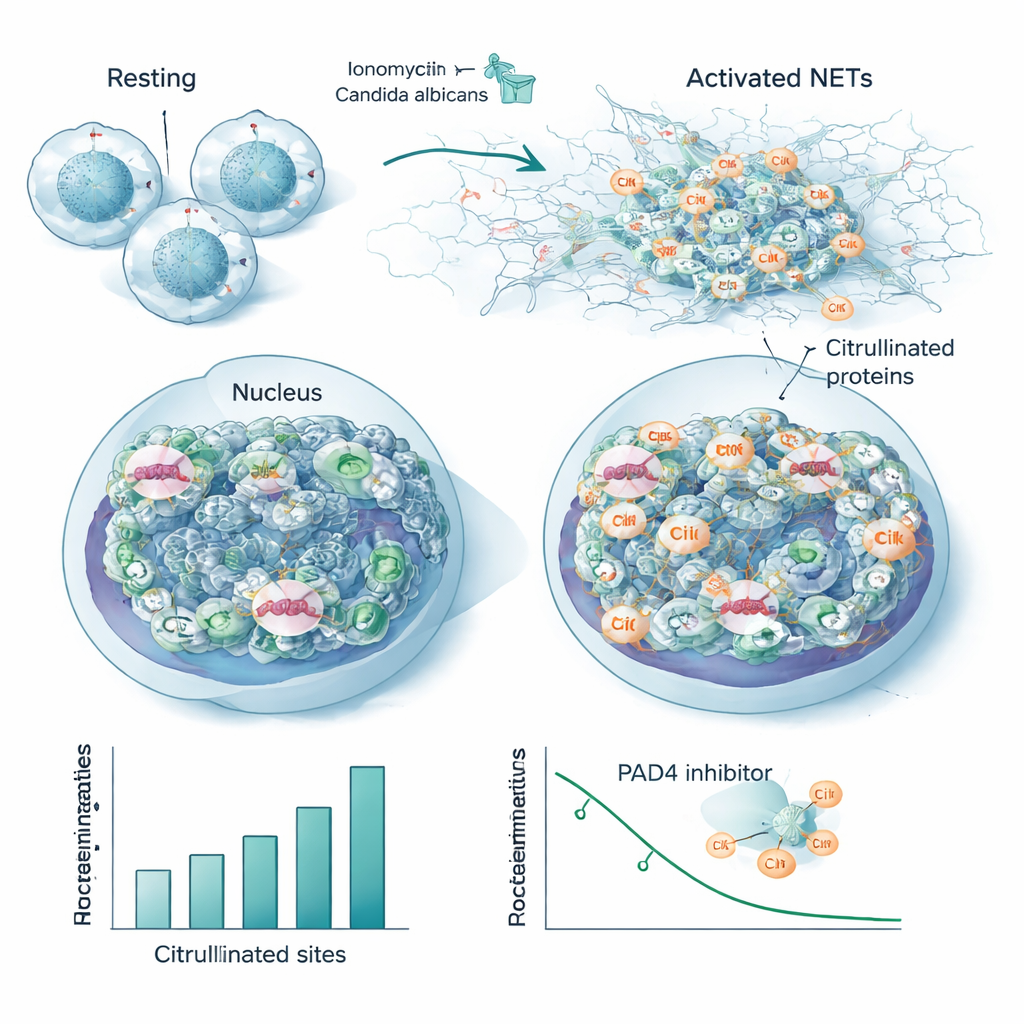
Los neutrófilos, un tipo de glóbulo blanco de primera línea, pueden combatir invasores liberando redes pegajosas de ADN y proteínas llamadas trampas extracelulares de neutrófilos, o NETs. La formación de NETs depende de PAD4, una enzima citrulinante que afloja la chromatina para que el ADN pueda salir al exterior. Utilizando su nuevo flujo de trabajo, los investigadores siguieron cómo cambiaba la citrulinación en neutrófilos humanos expuestos a dosis crecientes de un activador químico. Detectaron hasta 1.700 fragmentos peptídicos citrulinados repartidos en 580 proteínas, con cientos de sitios que aumentaban o disminuían de forma dependiente de la dosis mientras los niveles globales de proteínas permanecían constantes. Las histonas—las proteínas que empaquetan el ADN—presentaron citrulinación generalizada, no solo en unos pocos sitios clásicos, y las variantes de la histona de enlace H1 se modificaron especialmente. Proteínas estructurales como reguladores de la actina y la lamina B, que da forma a la envoltura nuclear, también se volvieron fuertemente citrulinadas, apuntando a un ablandamiento coordinado tanto de la cromatina como de los andamiajes celulares durante la liberación de NETs.
Una firma central de citrulinación en la infección
Para imitar una infección real, el equipo estimuló neutrófilos con Candida albicans muerto por calor, un patógeno fúngico común. Aunque esto produjo menos sitios modificados en conjunto que el fuerte activador químico, la gran mayoría de las proteínas y posiciones citrulinadas se solaparon entre ambos desencadenantes. Este solapamiento define un “citrulinoma” central conservado asociado con la formación de NETs, que incluye muchas proteínas nucleares y del citoesqueleto y varios autoantígenos conocidos—los mismos dianas de los anticuerpos en enfermedades autoinmunes. Cuando los investigadores añadieron un fármaco bloqueador de PAD4, muchos de esos mismos sitios perdieron su citrulinación de manera dependiente de la dosis, vinculándolos directamente con la actividad de la enzima y sugiriendo que podrían servir como lecturas sensibles de la inhibición de PAD4.
Qué significa esto para la salud y la enfermedad
Al convertir una modificación elusiva en una señal medible, este flujo de trabajo permite trazar dónde y cuándo ocurre la citrulinación en tejidos, respuestas inmunitarias y modelos de enfermedad. Para el público general, el mensaje clave es que la citrulinación actúa como un atenuador molecular sutil sobre las proteínas, y poder observar sus patrones con gran detalle podría ayudar a explicar cómo se inician las enfermedades autoinmunes, cómo las infecciones remodelan las células inmunitarias y cómo cambian las proteínas cerebrales con el tiempo. La escalabilidad del método y su dependencia de equipo de laboratorio estándar hacen que pueda adoptarse ampliamente, abriendo la puerta al descubrimiento de nuevas dianas terapéuticas, diagnósticos de precisión y una comprensión más profunda de cómo pequeños retoques químicos pueden tener grandes consecuencias biológicas.
Cita: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Palabras clave: citrulinación, enfermedad autoinmune, trampas extracelulares de neutrófilos, espectrometría de masas, modificación postraduccional