Clear Sky Science · es
Significado fisiopatológico de la alteración de la acetilación de histona H3K14 dependiente de KAT7 durante la deficiencia de zinc
Por qué nutríentes minúsculos importan para nuestra salud
El zinc es un metal traza que nuestro cuerpo necesita en pequeñas cantidades, pero que silenciosamente sostiene a cientos de proteínas que mantienen las células en funcionamiento. Cuando falta zinc —por dieta, enfermedad o envejecimiento— se ha relacionado con problemas que van desde un crecimiento deficiente hasta inmunidad debilitada y enfermedad hepática graso. Este estudio plantea una pregunta más profunda: ¿cómo detectan las células que el zinc escasea y cómo se traduce esa carencia en cambios duraderos en la actividad génica y la salud de los órganos?
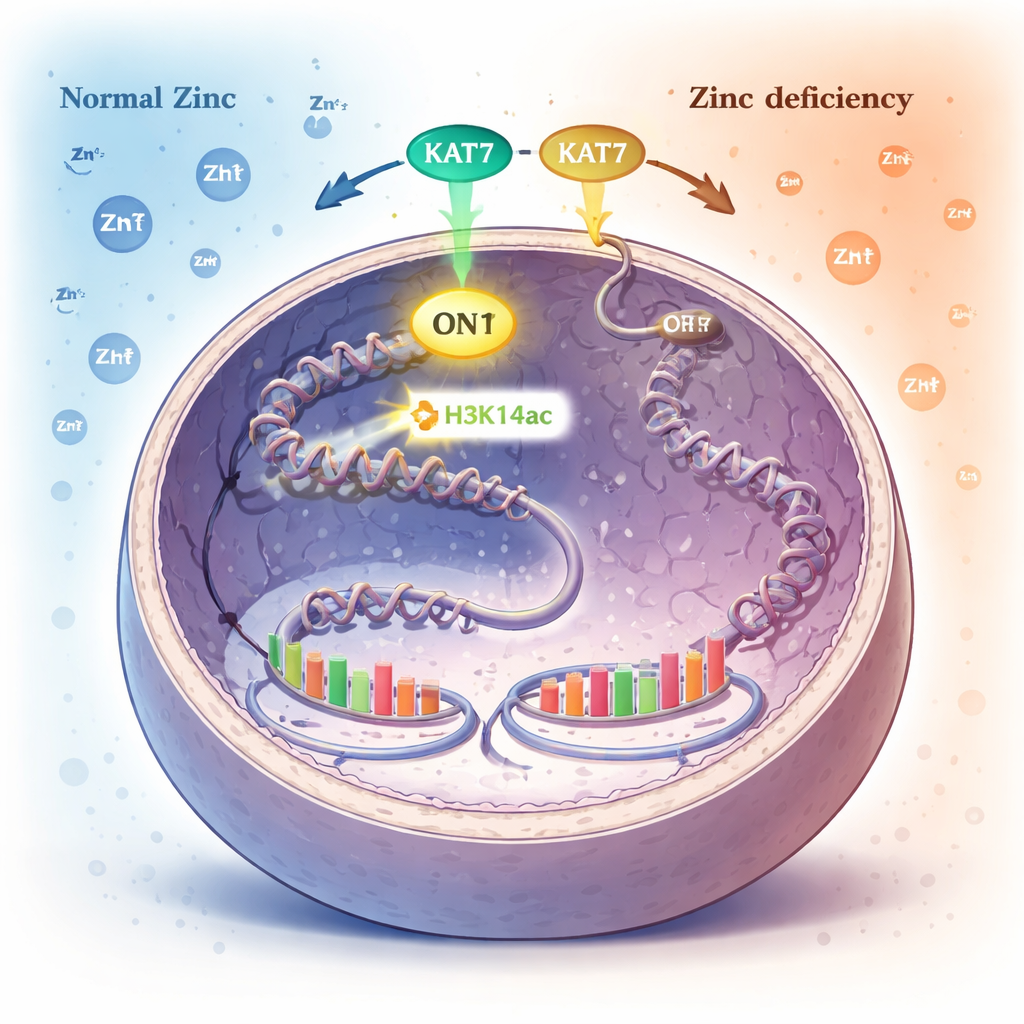
Una etiqueta química en el empaquetado del ADN como alarma interna del zinc
Dentro del núcleo, el ADN se enrolla alrededor de carretes proteicos llamados histonas. Las células controlan qué genes están activos añadiendo o quitando pequeñas etiquetas químicas a estas histonas. Una de esas etiquetas, denominada acetilación en un punto específico de la histona H3 (H3K14ac), la añade una enzima llamada KAT7. Los autores descubrieron que cuando el zinc escasea, los niveles de esta etiqueta H3K14ac caen drásticamente, mientras que muchas otras marcas comunes de histonas permanecen sin cambios. Esto señaló a H3K14ac, y a la enzima KAT7 que la genera, como un sensor clave del estado del zinc.
Cómo el zinc mantiene activada una enzima clave
Al desactivar sistemáticamente distintas enzimas, los investigadores mostraron que KAT7 es la fuente principal de H3K14ac en células humanas. KAT7 contiene una pequeña estructura que une zinc dentro de su centro activo. Cuando las células se sometieron a deficiencia de zinc, la capacidad de KAT7 para colocar la marca H3K14ac disminuyó, aunque la proteína permaneció en el núcleo y siguió asociada con sus socios auxiliares. Ensayos detallados con fragmentos purificados de KAT7 revelaron que el zinc correctamente ligado en esta región es esencial para su actividad; alterar la unión al zinc apagó la enzima, y añadir zinc cuidadosamente la restauró. En esencia, KAT7 actúa como un interruptor dependiente de zinc que controla una marca histónica específica.
Convertir la pérdida de zinc en cambios génicos que restauran el zinc
¿Qué hace realmente la pérdida de esta marca histónica? Mediante mapeo a escala del genoma, el equipo mostró que H3K14ac está especialmente enriquecida en regiones enhancers —fragmentos reguladores de ADN que afinan la expresión de genes vecinos. En condiciones de deficiencia de zinc, H3K14ac fue retirada de muchos enhancers, y cuanto mayor fue la pérdida, más pronunciado fue el cambio en la actividad de los genes próximos. Un gen destacado fue ZIP10, que codifica una proteína en la superficie celular que importa zinc. Cuando H3K14ac descendió en el enhancer de ZIP10, los niveles de ZIP10 en la membrana aumentaron, permitiendo que fluya más zinc hacia la célula. Bloquear KAT7 o impedir la pérdida de H3K14ac interfirió con esta respuesta y redujo la captación de zinc, incluso después de reponer zinc. Esto muestra que las células convierten la escasez de zinc en una señal epigenética que refuerza la maquinaria de importación de zinc para restaurar el equilibrio.
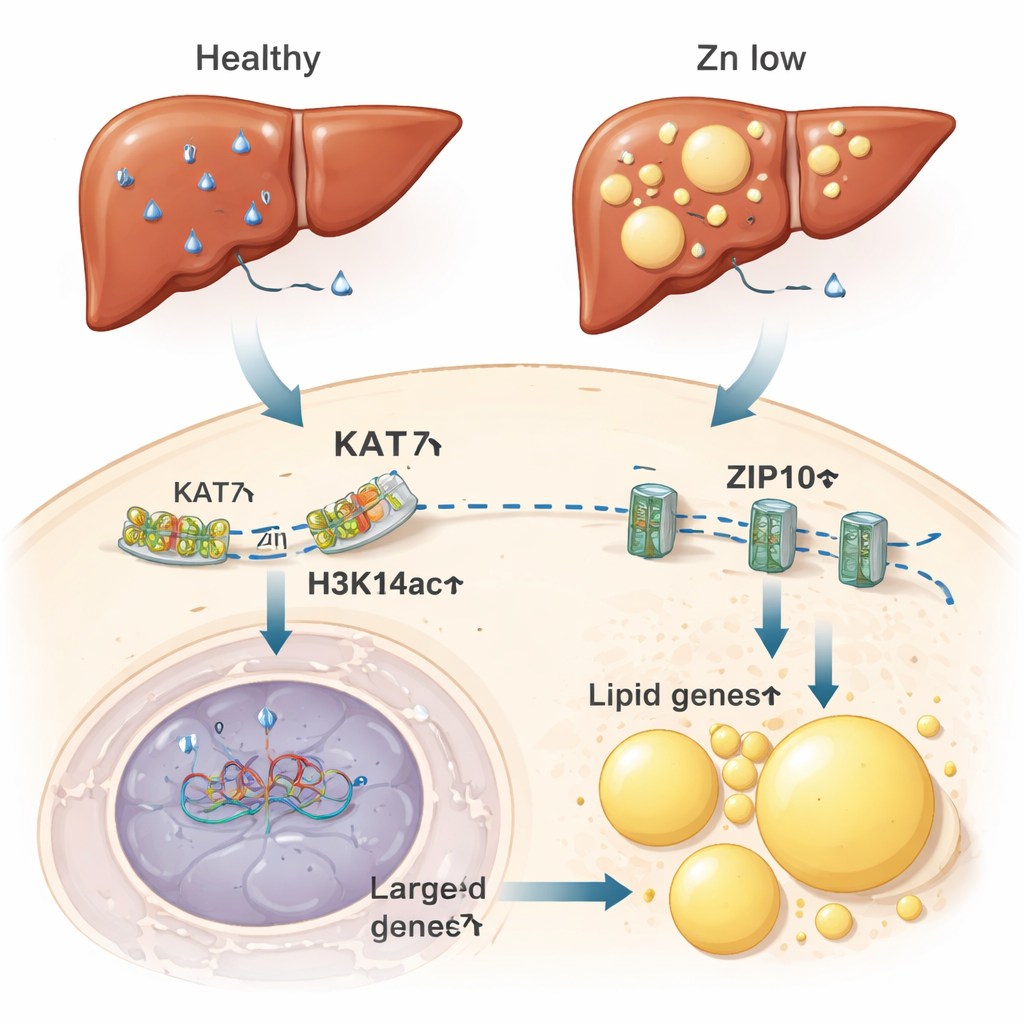
De células privadas de zinc a hígados grasos
Los autores preguntaron después si este interruptor sensible al zinc tiene consecuencias en animales completos. En ratones alimentados con una dieta deficiente en zinc, el hígado —un centro clave del metabolismo del zinc y de las grasas— mostró niveles reducidos de zinc, menor H3K14ac y actividad debilitada de KAT7. Estos cambios coincidieron con una mayor expresión de genes que impulsan el almacenamiento de grasa y la formación de gotas lipídicas, los paque tes microscópicos de grasa dentro de las células. Los hígados de los ratones con deficiencia de zinc acumularon grasa en un grado comparable al observado en animales con dieta alta en grasas. De manera notable, simplemente reducir la actividad de KAT7 con un fármaco, sin cambiar la ingesta dietética de zinc, fue suficiente para promover la acumulación de grasa en células hepáticas. Por el contrario, proporcionar zinc extra redujo la acumulación de grasa causada por una dieta alta en grasas.
Qué significa esto para el riesgo de enfermedad humana
Para poner sus hallazgos en contexto clínico, los investigadores revisaron estudios humanos que midieron niveles de zinc en tejido hepático. En múltiples reportes, las personas con hígado graso y trastornos relacionados tenían significativamente menos zinc en el hígado que los controles sanos. Junto con los experimentos en ratones, esto sugiere que la deficiencia crónica de zinc puede favorecer la enfermedad hepática grasa al silenciar KAT7, borrar la marca H3K14ac y activar de forma persistente genes que promueven el almacenamiento de grasa. En términos sencillos, el trabajo revela un circuito interno “zinc a epigenética”: cuando el zinc cae, una enzima dependiente de zinc pierde potencia, alterando el empaquetado del ADN de maneras que primero ayudan a las células a captar más zinc, pero con el tiempo también pueden empujar al hígado hacia una acumulación de grasa perjudicial.
Cita: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Palabras clave: deficiencia de zinc, epigenética, grasa hepática, acetilación de histonas, transportadores de zinc