Clear Sky Science · es
Perspectivas mecanicistas sobre la termodinámica fuera del equilibrio de la fijación de nitrógeno mediante cavitación acústica
Convertir el aire en fertilizante útil con sonido
El nitrógeno del aire es esencial para los fertilizantes y la producción de alimentos, pero convertir este gas resistente en formas útiles suele exigir fábricas enormes, calor extremo y alta presión. Este estudio explora un enfoque muy distinto: usar ondas sonoras intensas para crear diminutas burbujas explosivas en el agua que pueden "fijar" el nitrógeno bajo condiciones muy alejadas del equilibrio. Observando y modelando lo que ocurre dentro de estos puntos calientes efímeros, los investigadores muestran cómo las burbujas impulsadas por sonido podrían ofrecer una vía nueva para fabricar compuestos nitrogenados sin los catalizadores tradicionales ni reactores gigantes.
Por qué es tan difícil fijar el nitrógeno
Nuestra atmósfera es mayoritariamente gas nitrógeno, pero sus átomos están unidos por uno de los enlaces químicos más fuertes de la naturaleza. Romper ese enlace de forma eficiente es la razón por la que el proceso de Haber–Bosch depende de equipos potentes y consume grandes cantidades de energía a escala mundial. Los métodos convencionales deben encontrar un equilibrio incómodo: temperaturas lo bastante altas para activar el nitrógeno, pero no tanto como para que los productos deseados se descompongan o el equilibrio haga retroceder la reacción. Este artículo sostiene que, en lugar de mantener una temperatura constante, puede ser más eficaz sobrepasarla brevemente —usando ráfagas ultrarrápidas de calor— y luego enfriar tan deprisa que los productos útiles queden atrapados antes de descomponerse.
Usar ultrasonidos para crear cámaras reaccionales diminutas
Cuando ultrasonidos potentes atraviesan el agua, generan burbujas microscópicas que crecen y luego colapsan violentamente, un fenómeno conocido como cavitación acústica. Cada burbuja en colapso se comporta como un reactor en miniatura y de corta vida. En billonésimas de segundo, el gas en su interior se comprime hasta temperaturas superiores a 5000 kelvin y luego se enfría de nuevo a velocidades cercanas a 1012 kelvin por segundo. Bajo estas condiciones, las moléculas de nitrógeno en la burbuja pueden romperse en fragmentos reactivos, que luego se combinan con fragmentos procedentes del oxígeno, el hidrógeno o el agua para formar nitrito, nitrato o amonio. Los nuevos productos son expulsados al líquido circundante, donde se acumulan con el tiempo mientras una nueva generación de burbujas se forma y colapsa. 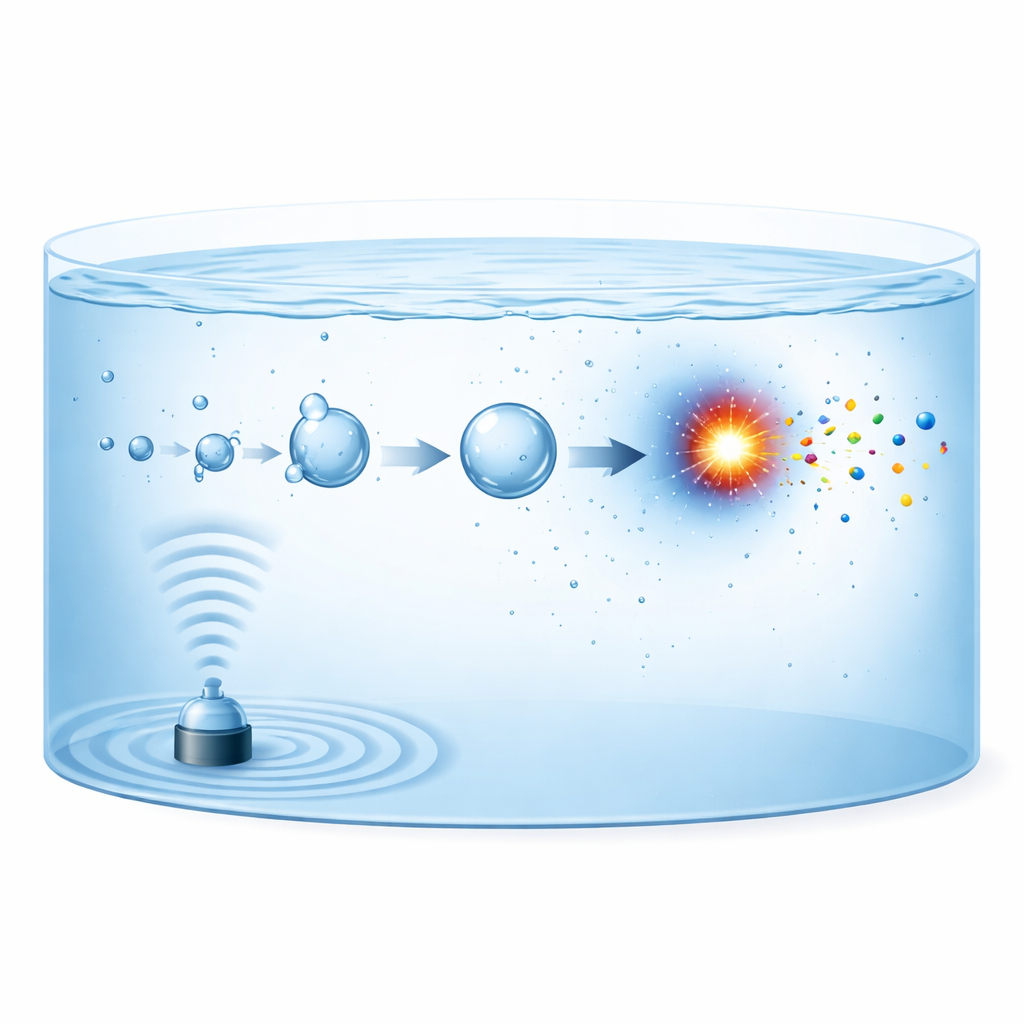
Regular las burbujas para elegir entre distintos productos
El equipo varió sistemáticamente los gases que alimentan las burbujas (nitrógeno más oxígeno o hidrógeno), la intensidad y la frecuencia de los ultrasonidos, y la presencia de partículas sólidas que facilitan la formación de burbujas. Con mezclas nitrógeno–oxígeno, el sistema produjo principalmente productos oxidados como nitrito y nitrato; con mezclas nitrógeno–hidrógeno, se favoreció el amonio. Pequeñas cantidades de partículas de talco actuaron como "semillas" de las burbujas, reduciendo el umbral de cavitación y haciendo las reacciones más reproducibles. Ajustando la presión sonora y el tiempo de reacción, los investigadores pudieron desplazar el equilibrio entre nitrito y nitrato, mostrando que parte de la química ocurre dentro de la burbuja en colapso y parte continúa en el agua circundante mientras los fragmentos reactivos convierten lentamente nitrito en nitrato más oxidado.
Escudriñar el pulso térmico a nanoescala
Para entender por qué condiciones tan extremas y fugaces aún producen compuestos estables, los autores combinaron medidas con simulaciones detalladas y cálculos cuántico-químicos. Estos muestran que, a temperaturas muy altas, el nitrógeno puede romperse directamente en fase gaseosa, abriendo rutas que habitualmente son inaccesibles. Pero los mismos cálculos también revelan que mantener el gas caliente volvería inestables los productos finales. La clave es el enfriamiento rápido: el pico de temperatura de la burbuja activa el nitrógeno y luego el enfriamiento casi instantáneo estabiliza fragmentos intermedios y moléculas terminadas como la amoníaco y el ácido nitroso antes de que puedan descomponerse o revertir a nitrógeno. Modelar burbujas individuales, especialmente cuando se dopan con argón para elevar las temperaturas de colapso, confirmó que mayores temperaturas pico desplazan la mezcla de productos y aumentan las tasas globales de fijación. 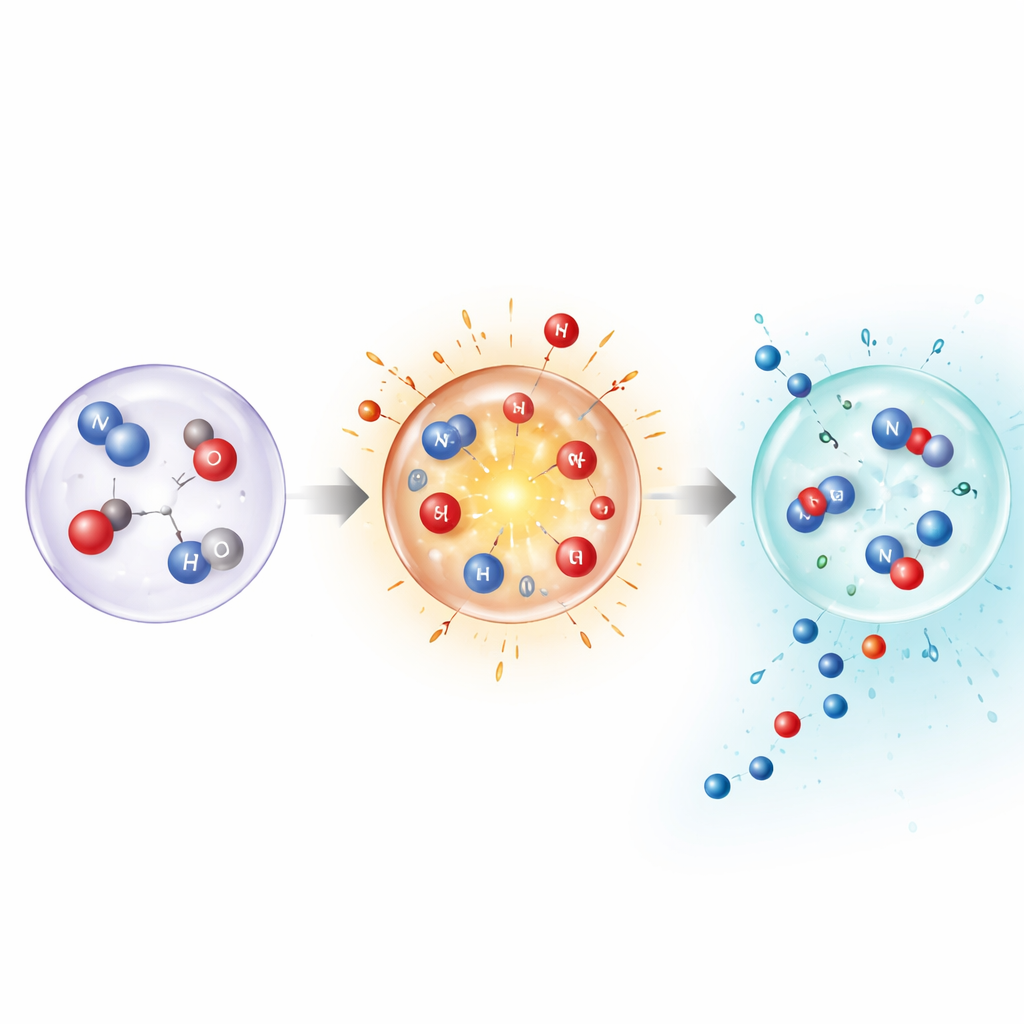
Consumo de energía y posibilidades futuras
Aunque este método impulsado por sonido aún no es tan eficiente energéticamente como los mejores procesos industriales, su rendimiento ya rivaliza con enfoques históricos de arco eléctrico y con algunos sistemas modernos de plasma, todo ello operando en condiciones ambientales generales y sin catalizadores sólidos. Es importante destacar que los mismos eventos de cavitación también rompen el agua, liberando hidrógeno, oxígeno y peróxido de hidrógeno —subproductos ricos en energía que podrían recuperarse junto con el nitrógeno fijado. Los autores enfatizan que su montaje está diseñado para revelar mecanismos más que para maximizar la producción, pero el trabajo establece la cavitación acústica como una vía distinta para fijar el nitrógeno explotando ciclos térmicos extremadamente rápidos en burbujas microscópicas. Para el lector general, la conclusión es que el sonido cuidadosamente controlado puede convertir agua y aire ordinarios en ingredientes de fertilizantes mediante una secuencia de pequeñas explosiones invisibles, apuntando a rutas más verdes y flexibles para producir en el futuro compuestos nitrogenados vitales.
Cita: Pan, X., Preso, D.B., Liu, Q. et al. Mechanistic insights into the non-equilibrium thermodynamics of nitrogen fixation via acoustic cavitation. Nat Commun 17, 2682 (2026). https://doi.org/10.1038/s41467-026-69466-1
Palabras clave: fijación de nitrógeno, cavitación acústica, sonquímica, producción de fertilizantes, química por ultrasonidos