Clear Sky Science · es
Triple diana contra STING, TGF-β y PD-L1 potencia la señalización CXCL16–CXCR6 para una potente respuesta antitumoral
Convertir tumores fríos en calientes
La inmunoterapia contra el cáncer ha transformado el tratamiento de algunos pacientes, pero muchos tumores siguen resistiéndose a estos potentes fármacos. Este estudio explora por qué ciertos cánceres son refractarios a los modernos inhibidores de puntos de control inmunitario y propone un ataque más inteligente y triple que despierta las defensas del organismo, atrae a células T citotóxicas de élite y las mantiene activas dentro del tumor.
Por qué los fármacos inmunitarios actuales no bastan
La mayoría de las inmunoterapias aprobadas se dirigen a un único freno de las células inmunitarias, como la vía PD-1/PD-L1. Una clase más nueva de fármacos intenta ir más allá bloqueando también la TGF-β, una molécula que suprime con fuerza la inmunidad en cánceres avanzados. Un fármaco de este tipo, YM101, combina el bloqueo de TGF-β y PD-L1 en un solo anticuerpo y mostró resultados prometedores en ratones. Pero incluso en animales genéticamente idénticos, algunos tumores apenas se redujeron. Al comparar tumores sensibles y resistentes, los investigadores hallaron que el éxito del tratamiento iba de la mano con una fuerte activación inmune “innata”, en particular la señalización a través de una vía llamada STING, que detecta ADN anómalo y desencadena señales de alarma similares a las antivirales.
Añadir una tercera palanca: la vía STING
Sospechando que la débil activación innata era la pieza que faltaba, el equipo combinó YM101 con un agonista de STING en forma de pastilla llamado MSA-2 en varios modelos tumorales de ratón, incluidos tumores “fríos” normalmente difíciles de tratar. El enfoque triple —activación de STING más bloqueo de TGF-β y PD-L1— redujo tumores de forma más eficaz, prolongó la supervivencia y con frecuencia protegió a los ratones frente a la reaparición tumoral tras un re‑desafío, lo que indica memoria inmune duradera. Esto superó a la combinación más convencional de un agonista de STING con bloqueo de PD-L1 solamente, e incluso potenció la terapia con agonista de STING cuando solo se bloqueó TGF-β, revelando que la TGF-β actúa como un freno importante sobre la inmunidad impulsada por STING. 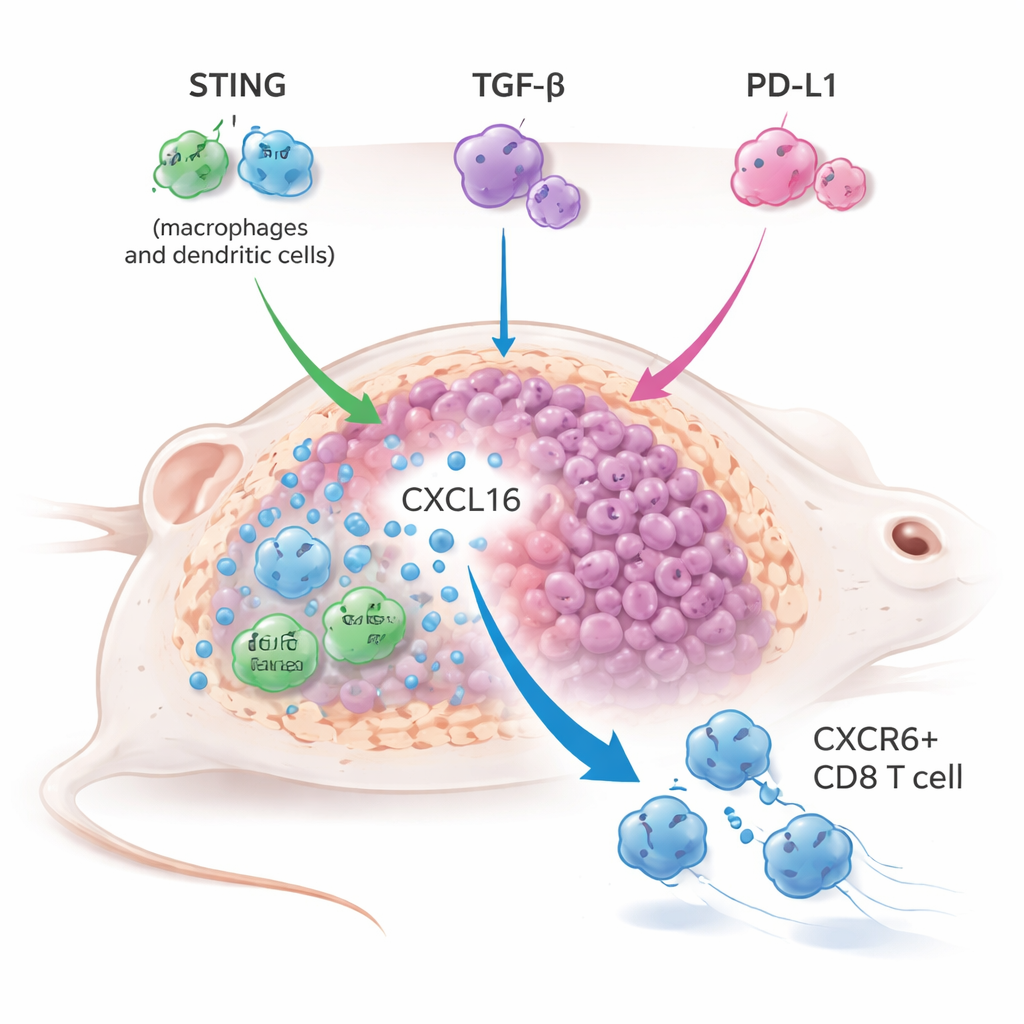
Reclutar un escuadrón especialista de asesinos
Para entender cómo funcionaba esta estrategia triple, los investigadores usaron secuenciación de ARN unicelular y un perfil inmunitario detallado de los tumores tratados. Descubrieron una expansión llamativa de un subconjunto particular de células T citotóxicas marcado por el receptor CXCR6. Estas células T CD8+ CXCR6+ estaban altamente equipadas, expresando altos niveles de granzimas, perforina y moléculas inflamatorias, y mostraban señales claras de activación y proliferación. Al mismo tiempo, los macrófagos y las células dendríticas asociadas al tumor aumentaron la producción de una quimiocina llamada CXCL16, que se une a CXCR6 y ayuda a retener estas células T en el tumor. Cuando el vínculo CXCL16–CXCR6 se interrumpió —ya sea bloqueando CXCL16 o eliminando genéticamente CXCR6 en las células T— el tratamiento combinado perdió en gran medida su potencia antitumoral, demostrando que este eje es central para el éxito de la terapia.
Cómo se activa la cascada de señales
Al profundizar, el equipo preguntó cómo la activación de STING y el bloqueo de TGF-β aumentan conjuntamente CXCL16. En células inmunitarias humanas y de ratón, los agonistas de STING incrementaron con fuerza CXCL16 y la citocina antiviral IFN‑β, mientras que la TGF-β añadida redujo drásticamente ambos. Los investigadores demostraron que STING desencadena la señalización IFN‑I, que activa el factor de transcripción STAT1; STAT1 se une luego directamente a la región de control del gen CXCL16, activándolo. La TGF-β interrumpe esta cadena interfiriendo con un paso clave de la señalización STING, probablemente vía una proteína llamada HDAC4 y especies reactivas de oxígeno, atenuando la activación de IRF3 y la producción posterior de IFN‑β y CXCL16. Bloquear TGF-β elimina este freno, permitiendo que los agonistas de STING enciendan plenamente la vía STAT1–CXCL16 en células mieloides y así proporcionen a las células T CXCR6+ las señales necesarias para permanecer y combatir en el tumor.
Construir un único fármaco de precisión
Para hacer este régimen complejo más práctico y centrado en el tumor, los investigadores diseñaron un único "conjugado anticuerpo‑estimulador inmune" llamado Y101S. Esta molécula combina el anticuerpo que bloquea TGF-β/PD-L1 con un agonista de STING enlazado mediante un conector clivable. Y101S se dirige a las células mieloides PD-L1–positivas en el tumor, es internalizado y libera entonces el fármaco STING dentro de estas células. En varios cánceres de ratón, Y101S igualó o superó la eficacia de administrar YM101 más una alta dosis de agonista de STING libre, a pesar de transportar solo una fracción minúscula de esa dosis de STING. Aumentó macrófagos y células dendríticas CXCL16+, expandió células T CD8+ CXCR6+, indujo memoria inmune duradera y concentró señales inflamatorias en los tumores mientras protegía órganos sanos, con un perfil de seguridad favorable en ratones. 
Qué supone esto para el tratamiento futuro del cáncer
Para los no especialistas, el mensaje clave es que atacar el cáncer con solo uno o dos interruptores inmunitarios puede no ser suficiente, especialmente cuando los tumores silencian activamente los sistemas de alarma temprana. Este trabajo muestra que combinar la activación de STING con el bloqueo de TGF-β y PD-L1 puede reconfigurar el microambiente tumoral, atraer y mantener de forma potente a un grupo especializado de células T citotóxicas y lograr respuestas más profundas y duraderas en modelos preclínicos. El anticuerpo‑fármaco de triple diana Y101S encarna esta estrategia en un único medicamento dirigido y ofrece una hoja de ruta para inmunoterapias de nueva generación dirigidas a tumores que actualmente resisten los fármacos checkpoint estándar.
Cita: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Palabras clave: inmunoterapia contra el cáncer, vía STING, bloqueo de TGF-beta, anticuerpo anti‑PD-L1, CXCL16 CXCR6 células T