Clear Sky Science · es
Una subpoblación de células mesenquimales inducida por macrófagos que expresa Fcer1g contribuye a la fibrosis inducida por heridas
Por qué algunas heridas dejan cicatrices duraderas
La mayoría de nosotros llevamos cicatrices de cortes, cirugías o accidentes, pero por qué unas heridas sanan sin problemas y otras dejan marcas gruesas y elevadas sigue siendo un enigma. Este estudio aborda la cuestión enfocándose en las células que reconstruyen la piel dañada. Los investigadores descubren un grupo hasta ahora no reconocido de células formadoras de cicatriz que se activan de forma temprana tras la lesión, bajo la influencia de células inmunitarias llamadas macrófagos. Entender esta asociación oculta podría señalar vías para tratamientos que permitan que la piel sane con menos cicatrices sin dejar de cerrar las heridas de forma eficaz. 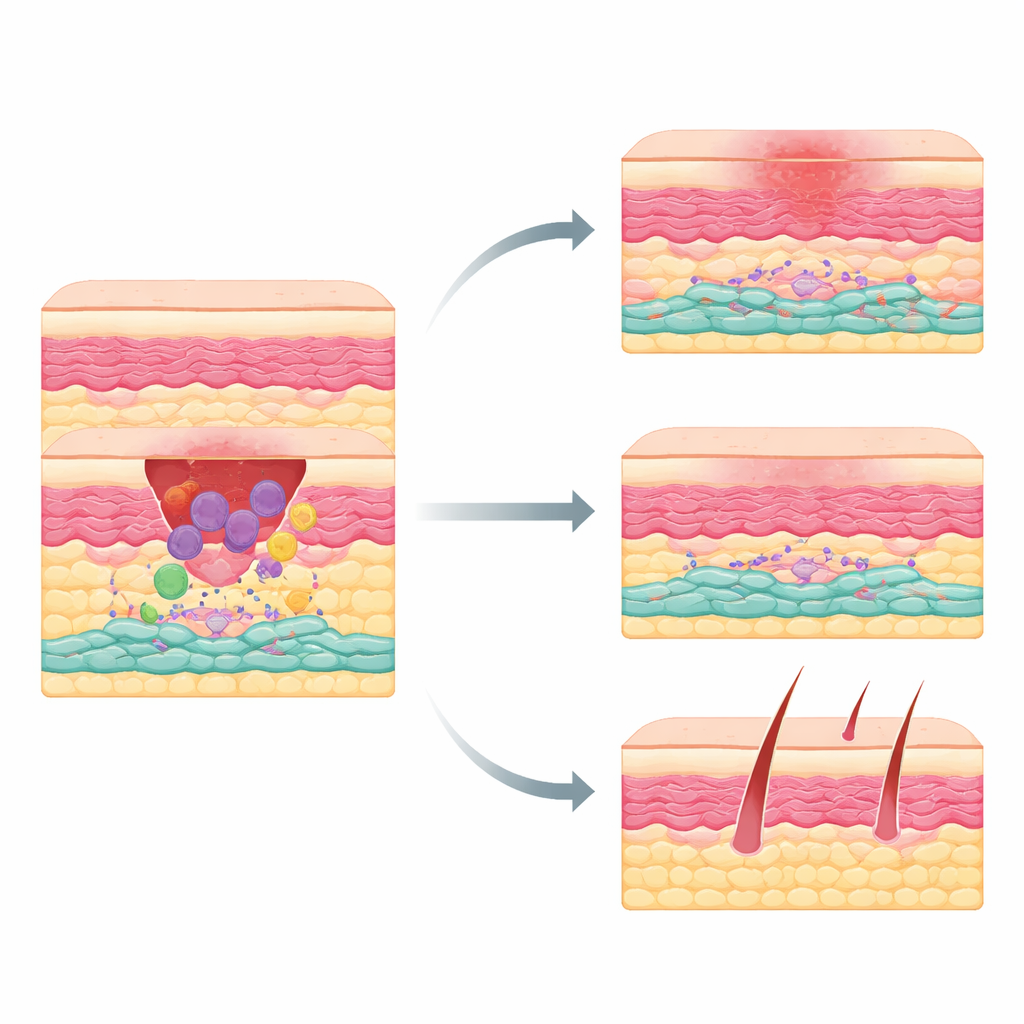
Los actores ocultos dentro de la piel en curación
Cuando la piel se corta, el cuerpo sigue una secuencia coreografiada: primero inflamación para limpiar el daño, luego crecimiento tisular y, finalmente, remodelación. Los macrófagos llegan pronto para eliminar restos y enviar señales químicas que movilizan a otras células. Entre las respondedoras están las células mesenquimales —constructores con aspecto de fibroblastos que depositan colágeno y otros materiales de sostén. Estos constructores no son todos iguales: algunos favorecen la regeneración, mientras que otros tienden a producir en exceso tejido cicatricial. Hasta ahora, los científicos no habían identificado con claridad qué células mesenquimales de la piel adulta eran las principales responsables de las cicatrices gruesas.
Células inmunitarias que silenciosamente preparan el terreno para la cicatrización
Para explorar cómo los macrófagos influyen en la formación de cicatrices, el equipo usó ratones en los que los macrófagos pueden eliminarse de forma selectiva durante los primeros días tras la lesión. Cuando se eliminaron estos macrófagos tempranos, las heridas todavía se cerraron, pero formaron cicatrices mucho más pequeñas, con colágeno menos denso. La secuenciación de ARN de una sola célula —una forma de perfilar la actividad génica célula por célula— mostró que la mayoría de los subgrupos mesenquimales no cambiaron al perder macrófagos. Una excepción destacó: un subconjunto distinto de células mesenquimales PDGFRα‑positivas que activaron un gen llamado Fcer1g. Este subconjunto casi desapareció cuando faltaban macrófagos, lo que sugiere que los macrófagos son necesarios para crear o mantener estas células.
Una población celular de rápido crecimiento que impulsa la cicatriz
Experimentos adicionales mapearon dónde y cuándo aparecen estas células mesenquimales positivas para Fcer1g. En piel no lesionada eran raras, pero tras la lesión se expandieron rápidamente, primero alrededor de los bordes de la herida y luego concentrándose en el lecho de la misma, donde constituían la mayor parte de las células PDGFRα‑positivas a los siete días. Estas células se dividían más rápido que otras mesenquimales y mostraron baja migración, lo que indica que su aumento se debe a la proliferación local. Cuando los investigadores usaron un ingenioso sistema genético para eliminar selectivamente las células que expresaban tanto PDGFRα como Fcer1g, el cierre de la herida transcurrió con normalidad —pero las cicatrices se redujeron en más del 20 por ciento, el contenido de colágeno cayó alrededor de un 30 por ciento y la red de colágeno de la piel reparada se pareció más a la de la piel no lesionada. Los folículos pilosos fueron más abundantes en estas heridas con depleción, lo que sugiere una curación más regenerativa. 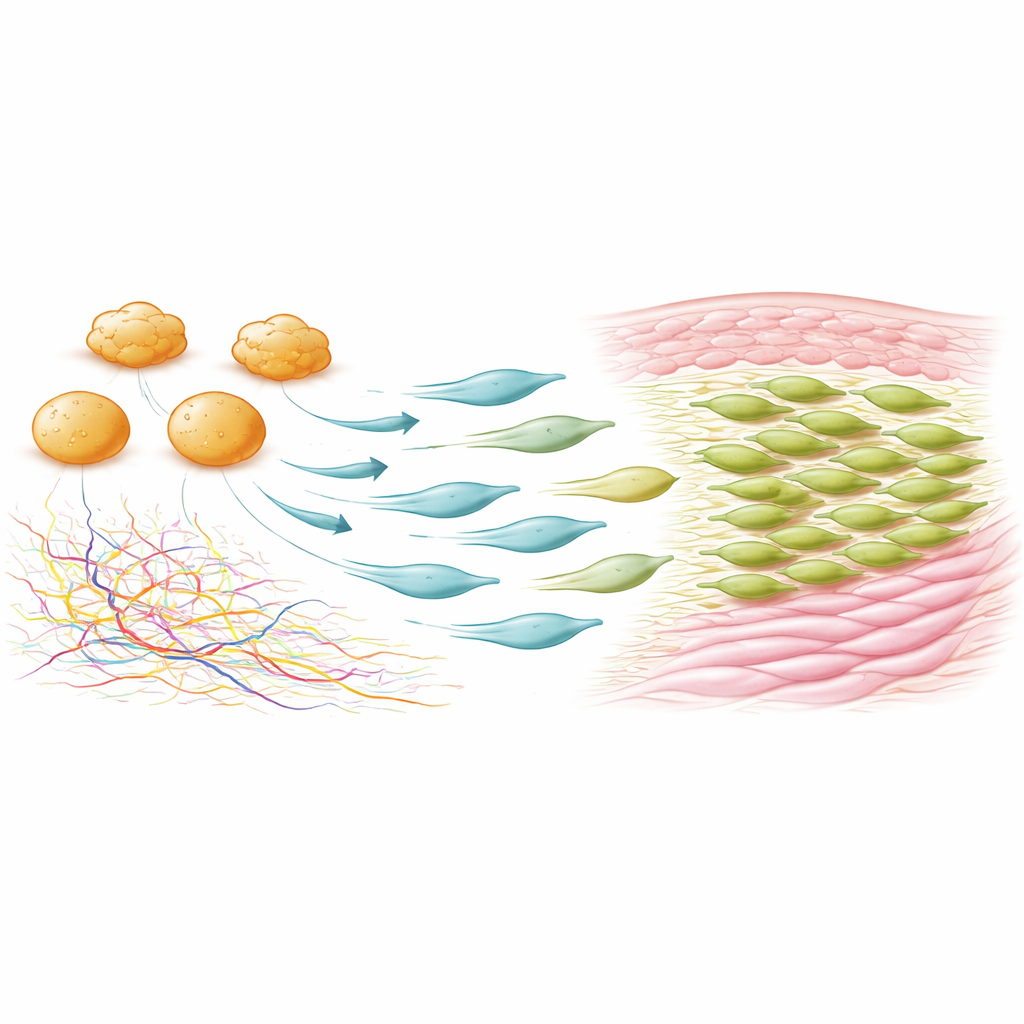
Cómo los macrófagos señalan a los constructores para producir más cicatriz
Para entender cómo los macrófagos desencadenan este estado proclive a la cicatriz, el equipo analizó las rutas de comunicación probables entre tipos celulares. Un candidato principal fue la fibronectina, una proteína adhesiva que forma parte de la matriz temporal en heridas recientes. Los macrófagos en heridas tempranas fueron una fuente mayor de fibronectina, y sus niveles cayeron drásticamente cuando se eliminaron los macrófagos. En ratones diseñados para carecer de una versión asociada a heridas de la fibronectina (la forma EDA), las células mesenquimales Fcer1g‑positivas se redujeron considerablemente y las cicatrices fueron más leves. En cultivo, el contacto directo con macrófagos fue suficiente para convertir fibroblastos dérmicos ordinarios en células positivas para Fcer1g y PDGFRα, lo que subraya que los macrófagos pueden inducir directamente este estado.
Un programa compartido de cicatrización en ratones y humanos
Para ver si este tipo celular importa en humanos, los investigadores reexaminaron conjuntos de datos existentes sobre heridas cutáneas humanas a resolución de célula única y de tejido completo. Encontraron un subgrupo mesenquimal coincidente en heridas humanas que expresaba FCER1G y un perfil génico similar, con un pico alrededor de una semana tras la lesión —el mismo momento observado en ratones. En más de cien muestras humanas que incluían piel normal, heridas agudas, heridas crónicas y cicatrices elevadas, el programa génico vinculado a FCER1G separó claramente el tejido lesionado y cicatrizado de la piel no lesionada y fue más fuerte al inicio tras la lesión. Esta similitud entre especies sugiere que el estado celular recién definido es un impulsor evolutivamente conservado de la reparación fibrótica.
Hacia una curación más suave con menos cicatrices
En conjunto, los hallazgos revelan una cadena de eventos hasta ahora poco apreciada: los macrófagos que llegan temprano enriquecen la fibronectina en la herida, la fibronectina ayuda a convertir las células mesenquimales locales en un estado de rápida proliferación positivo para FCER1G, y este subconjunto especializado luego deposita colágeno en exceso que se convierte en tejido cicatricial. Dado que la eliminación de estas células en ratones redujo la formación de cicatrices sin ralentizar el cierre de la herida, representan un objetivo atractivo para futuras terapias. Fármacos o biológicos que interrumpan las señales que crean o sostienen este estado celular —quizá modulando el comportamiento de los macrófagos o el entorno de fibronectina— podrían algún día ayudar a los pacientes a sanar lesiones cutáneas con cicatrices mínimas y menos visibles.
Cita: Ma, X., Wang, E., Puviindran, V. et al. A macrophage-induced subpopulation of mesenchymal cells expressing Fcer1g contributes to wound-induced fibrosis. Nat Commun 17, 2686 (2026). https://doi.org/10.1038/s41467-026-69449-2
Palabras clave: cicatrización de heridas, fibrosis cutánea, macrófagos, fibroblastos, formación de cicatrices