Clear Sky Science · es
Cooperatividad positiva entre los dominios de unión a RAS y ricos en cisteína regula la cinética de unión de RAF a la membrana mediante reanudación lateral
Por qué importa esta pequeña danza molecular
En el interior de nuestras células, las decisiones de vida o muerte sobre crecimiento, división y supervivencia se toman a menudo en la superficie de la membrana celular. Un actor clave en estas decisiones es una proteína llamada RAF, que ayuda a transmitir señales de crecimiento y con frecuencia está desregulada en el cáncer. Este estudio descubre, con un detalle cinético sin precedentes, cómo RAF se ancla a las membranas celulares, cuánto tiempo permanece allí y por qué los parches densos de otra proteína, RAS, pueden mantener a RAF activo durante más tiempo del esperado.
Señales que se encuentran en la superficie celular
RAF actúa en una importante vía de señalización conocida como la vía MAPK, que conecta estímulos externos como los factores de crecimiento con cambios en la actividad génica. En su forma inactiva, RAF flota en el interior celular en una conformación plegada y auto-inhibida. Solo se activa cuando encuentra a RAS, un pequeño interruptor molecular anclado a la cara interna de la membrana celular. RAS debe estar en su estado “encendido” y estar incrustado en el tipo adecuado de lípidos para que RAF sea reclutado y activado. Dado que las moléculas de RAF son relativamente escasas en comparación con muchos otros componentes de señalización, la forma exacta en que se acoplan a la membrana y evitan una liberación prematura influye fuertemente en si una célula responderá débil o fuertemente a una señal de crecimiento.
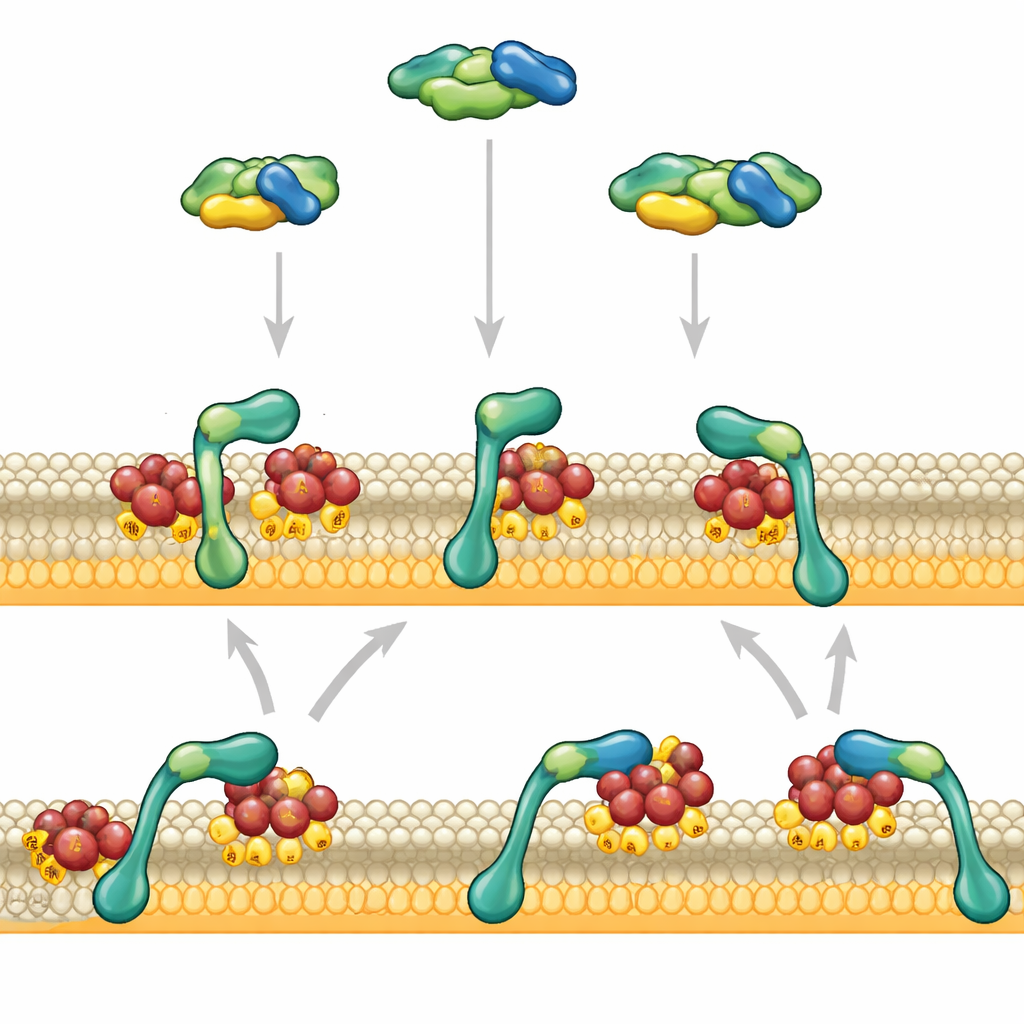
Dos manos para agarrar la membrana
Los autores se centraron en dos regiones en el extremo frontal de RAF: una que se une a RAS y otra que prefiere lípidos de la membrana con carga negativa. Usando membranas artificiales y proteínas purificadas, observaron fragmentos individuales de RAF uniéndose a superficies decoradas con RAS mediante microscopía avanzada. Cuando la región de unión a RAS actuaba sola, tocaba la membrana brevemente y se soltaba en aproximadamente un segundo. La región que prefiere lípidos, por sí sola, apenas se adhería. Pero cuando estas dos regiones estaban conectadas, su comportamiento cambió drásticamente: RAF ahora se unía con firmeza y permanecía en la membrana durante decenas de segundos, especialmente cuando la membrana contenía muchos lípidos cargados negativamente similares a los de las células reales.
Cooperación que ralentiza la salida
Este cambio dramático no se debió a que RAF encontrara la membrana más rápido, sino a que se marchaba más despacio. Primero, el segmento de RAF que une RAS reconoce a RAS activado y ancla a RAF en la membrana. Solo después de este primer apretón la región de unión a lípidos participa por completo con los lípidos circundantes, ralentizando el movimiento lateral de RAF y anclándolo con mayor firmeza. Este segundo contacto, a su vez, estabiliza la interacción original RAS–RAF, creando un bucle de realimentación positiva entre contactos proteína–proteína y proteína–lípido. Experimentos que modificaron el corto enlace que conecta las dos regiones mostraron que su estrecha coordinación espacial es crucial: hacer el enlace más flexible o más largo debilitó la capacidad de RAF para permanecer en la membrana.
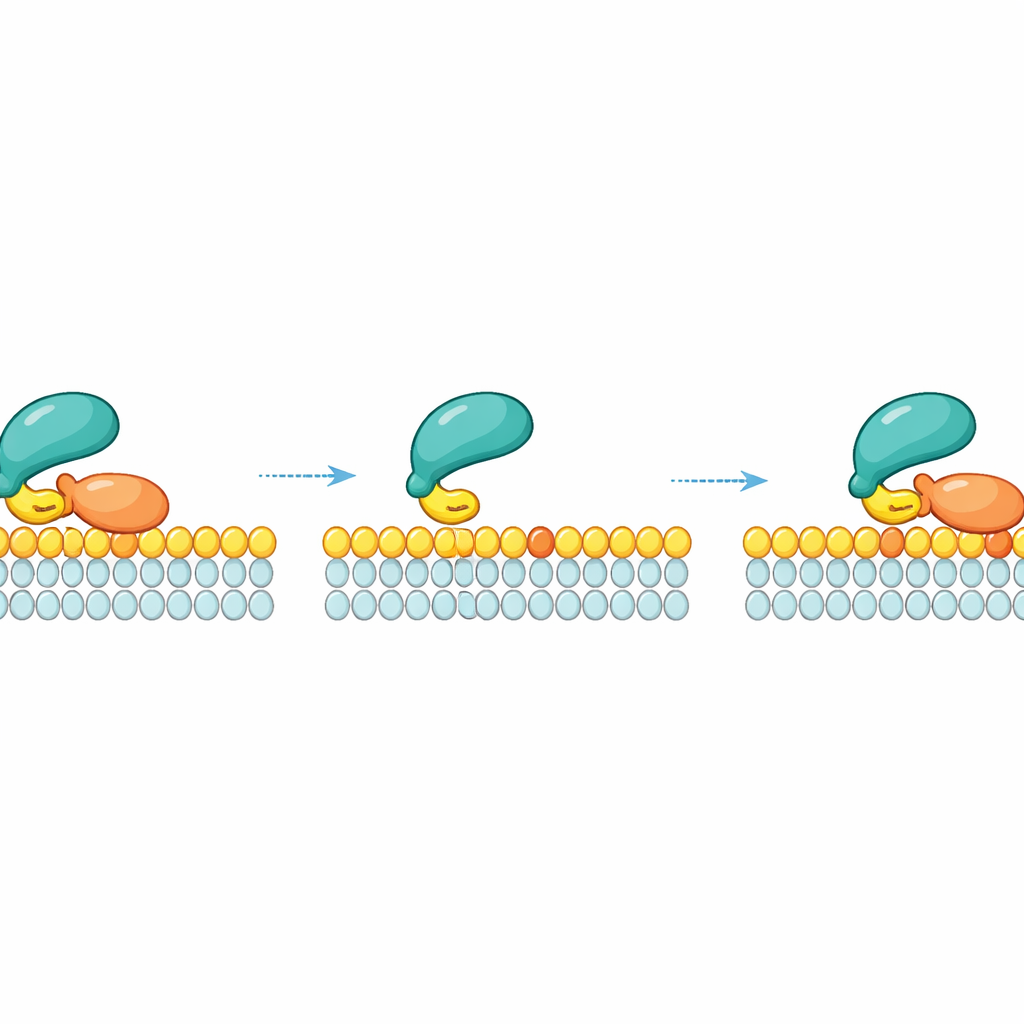
Reanudación lateral: deslizarse en lugar de caerse
Una idea clave del trabajo es que RAF no se desprende simplemente al fluido circundante una vez que suelta a una molécula particular de RAS. En su lugar, tras la liberación de RAS, RAF puede permanecer brevemente sujeto a la membrana mediante su débil contacto con los lípidos y deslizarse lateralmente. Mientras está en este estado transitorio, puede “volver a agarrar” una molécula vecina de RAS en el mismo parche de membrana. Esta reanudación lateral crea una red de seguridad cinética: a alta densidad local de RAS —como en nanocúmulos donde las moléculas de RAS se empaquetan estrechamente— RAF tiene muchas oportunidades de volver a engancharse a RAS antes de derivar. Mediciones y simulaciones mostraron que cuanto mayor es la densidad de RAS activo en la membrana, más tiempo permanece RAF unido a la membrana debido a estas readhesiones locales repetidas.
De visitas prolongadas a activación fiable
El tiempo extendido que RAF pasa en la membrana tiene consecuencias importantes. La activación de RAF no es un evento único sino una secuencia de varios pasos que incluye cambios conformacionales, eliminación de marcas inhibitorias y el emparejamiento de dos moléculas de RAF en un dímero activo. El estudio sugiere que solo las moléculas de RAF que permanecen el tiempo suficiente en la membrana pueden completar esta secuencia, una forma de “comprobación cinética” que ayuda a las células a evitar activaciones accidentales por señales efímeras y débiles. Al revelar cómo la interacción entre la unión a RAS, el compromiso con los lípidos y la reanudación lateral determina la residencia de RAF en la membrana, el trabajo describe una estrategia general mediante la cual las células pueden usar muchas interacciones pequeñas y débiles en membranas para ajustar con precisión vías de señalización potentes.
Cita: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Palabras clave: RAS, quinasa RAF, señalización en la membrana celular, reanudación lateral, comprobación cinética