Clear Sky Science · es
Base estructural y molecular de la regulación alostérica y el acoplamiento catalítico de la fosforribosilformilglicinamida amidina humana
Por qué importa esta enzima para la salud
Cada célula de su cuerpo depende de las purinas, pequeñas moléculas que impulsan reacciones, almacenan energía y transportan información genética. Las células cancerosas, que se dividen rápidamente, son especialmente voraces de purinas y con frecuencia reconfiguran su producción. Este estudio se centra en una enzima humana llamada FGAMS, un actor clave en la síntesis de purinas desde cero. Al revelar la estructura tridimensional de FGAMS y cómo sus partes se mueven y comunican, los autores muestran cómo se enciende y apaga la enzima y cómo podría dirigirse para frenar el crecimiento tumoral.
Los componentes de la vida bajo control
Las células fabrican purinas mediante una cadena de montaje exigente conocida como la vía de novo, que consume energía y emplea varias enzimas para ensamblar un anillo complejo. FGAMS realiza el cuarto paso de esta secuencia y se sitúa en el centro de un ensamblaje enzimático mayor llamado purinosoma, que ayuda a canalizar los sustratos de forma eficiente. Dado que las células tumorales de rápido crecimiento a menudo aumentan esta vía, enzimas como FGAMS son objetivos farmacológicos atractivos: bloquearlas puede privar a los tumores de los nucleótidos que necesitan, mientras que las células sanas recurren a rutas de reciclaje.
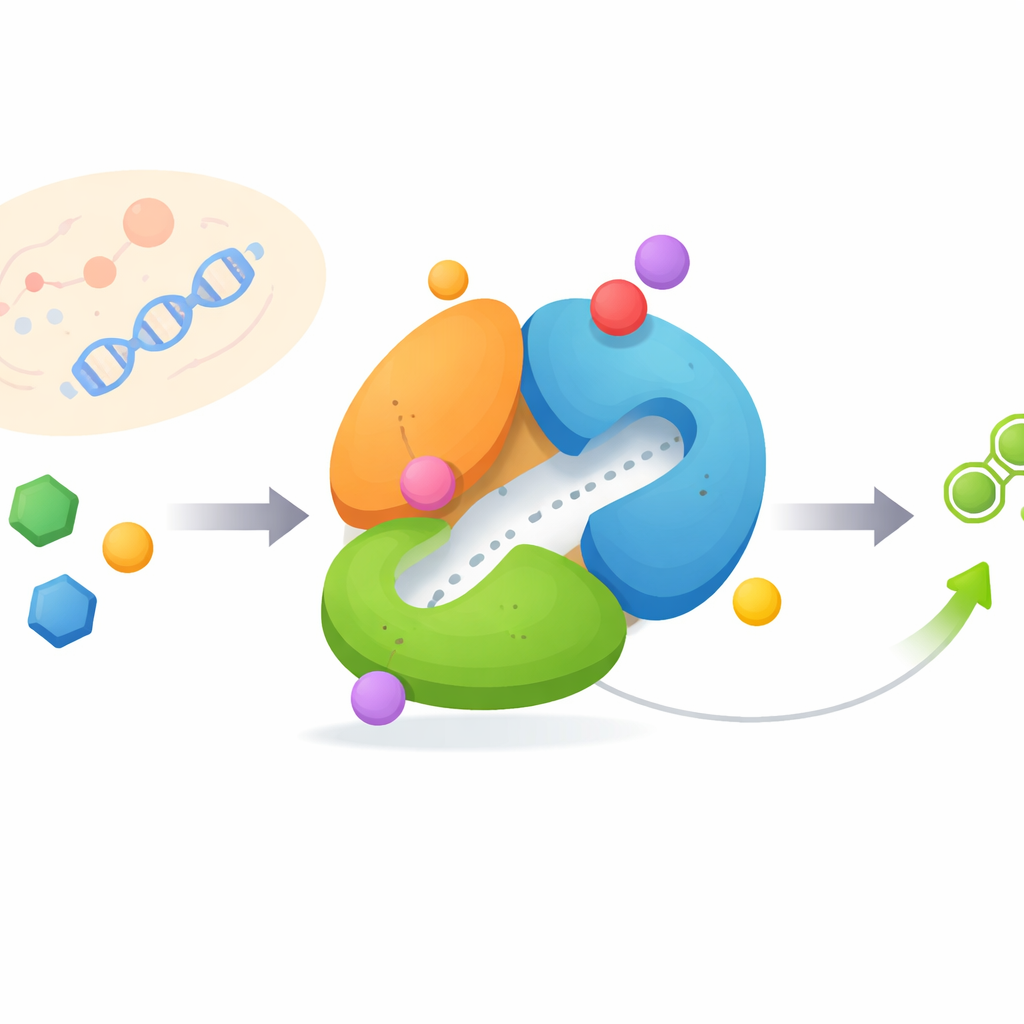
Una máquina molecular que cambia de forma
FGAMS está construida a partir de tres partes conectadas, o dominios, que desempeñan trabajos distintos y deben cooperar en un orden preciso. Un dominio libera amoníaco del aminoácido glutamina, otro emplea ese amoníaco para modificar una pequeña molécula azucarada, y un tercer dominio actúa como centro regulador. Mediante microscopía crioelectrónica de alta resolución, los investigadores capturaron FGAMS en tres estados de trabajo distintos: con una molécula portadora de energía unida, con un intermedio de reacción de corta vida atrapado, y con múltiples sustratos e intermedios presentes a la vez. Comparar estos estados reveló que bucles flexibles y un “brazo” N‑terminal se mueven de forma dramática, reconfigurando la enzima a medida que avanza la química.
Túnel oculto y compuertas moleculares
Un rompecabezas clave ha sido cómo el amoníaco liberado en un dominio viaja de forma segura hasta el sitio distante donde se utiliza, sin difundirse y causar daños. Las nuevas estructuras exponen un túnel interno hasta ahora no visto que conecta los dos sitios, junto con una serie de “compuertas” formadas por aminoácidos específicos. Cuando se unen los sustratos adecuados y se forma el intermedio, un bucle central se ordena bruscamente, tirando del dominio N‑terminal y reordenando bucles cercanos en el dominio catalítico. Esta coreografía abre dos compuertas de entrada para que la glutamina pueda procesarse y remodela brevemente una región que estabiliza el intermedio de alta energía necesario para romper enlaces.
Acoplar la química mediante el movimiento
A medida que la reacción progresa, la enzima no se limita a esperar; emplea cada paso químico como una señal. Una vez que se forma un intermedio tioéster covalente en el dominio que genera amoníaco, los movimientos previos se invierten parcialmente. Esto relaja el bucle central y reposiciona las compuertas para cerrar rutas de escape, mientras que otras dos compuertas en los extremos del túnel se abren. Desplazamientos sutiles en un puñado de residuos “estrecho” ensanchan el pasaje interior, permitiendo que una molécula de amoníaco viaje por el túnel directamente hasta el segundo sitio activo, donde reacciona con el intermedio atrapado para producir el producto final. Mutar los residuos de las compuertas provoca fugas de amoníaco o desacoplamiento de las dos mitades de la reacción, lo que confirma que este sistema de compuertas y canalización es esencial para una catálisis eficiente.
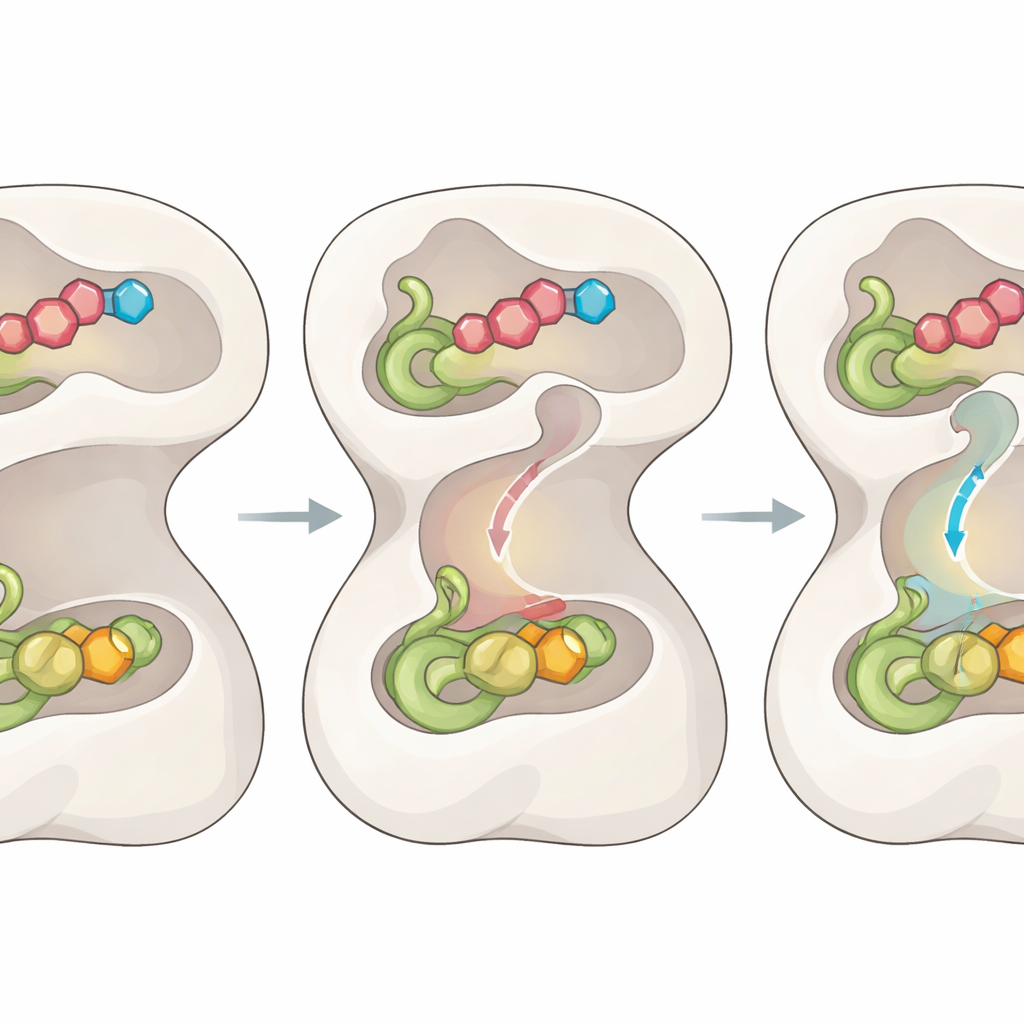
De la visión estructural a vías terapéuticas
Siguiendo a FGAMS a lo largo de su ciclo catalítico, el estudio dibuja un panorama detallado de cómo los movimientos de dominios, los bucles flexibles, las compuertas internas y un túnel transitorio están todos conectados para coordinar la química. Para un público general, la conclusión es que la enzima actúa como una pequeña fábrica programable: solo abre sus puertas y su cinta interna cuando todas las piezas correctas están en su sitio, garantizando rapidez y seguridad. Dado que FGAMS sostiene la producción de purinas en células cancerosas y se asocia con peor supervivencia en tumores hepáticos, los planos estructurales y los puntos de control recién identificados ofrecen múltiples apoyos para diseñar fármacos que bloqueen el túnel, inmovilicen las compuertas o atrapen intermedios clave, lo que podría dar lugar a una nueva clase de terapias anticancerígenas dirigidas.
Cita: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Palabras clave: biosíntesis de purinas, regulación alostérica, canalización de amoníaco, metabolismo del cáncer, estructura por crio‑EM