Clear Sky Science · es
Regulación por retroalimentación negativa de la señalización STING mediante la golgifagia dirigida por TAX1BP1
Cómo las células evitan una sobrerreacción inmune
Nuestro sistema inmunitario debe caminar por una cuerda floja: tiene que reconocer rápidamente los virus invasores y el ADN dañado, pero también necesita desactivar esa alarma antes de que la inflamación descontrolada dañe tejidos sanos. Este estudio revela cómo un ayudante celular poco conocido, TAX1BP1, actúa como un freno integrado sobre una potente vía de alarma llamada cGAS–STING. Al explicar cómo las células desmantelan esta alarma una vez que ha cumplido su función, el trabajo arroja luz sobre las enfermedades autoinmunes, la defensa antiviral y posibles terapias contra el cáncer.
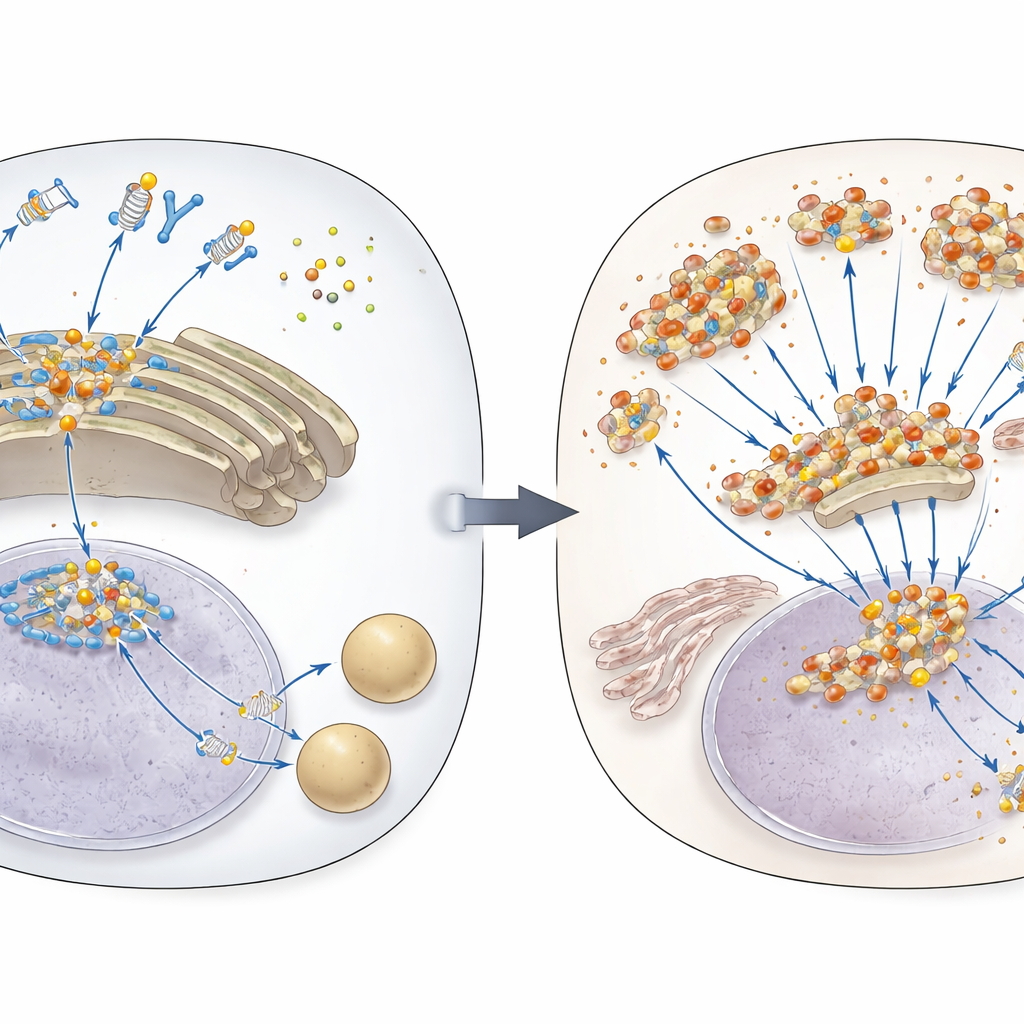
El sistema de alarma de ADN de la célula
Cuando aparece ADN extraño o mal localizado en el interior de las células, una proteína sensor llamada cGAS lo detecta y produce una pequeña molécula mensajera. Esa mensajera activa a STING, una proteína tipo interruptor que vive en membranas internas. STING entonces viaja a un centro de distribución celular llamado Golgi, donde se agrupa y desencadena la producción de moléculas antivirales conocidas como interferones de tipo I, junto con otras señales inflamatorias. Debido a que esta respuesta es muy potente, las células normalmente degradan STING tras un breve estallido de actividad, encaminándolo hacia centros de reciclaje celular llamados lisosomas. Hasta ahora, cómo se dirigía STING hacia este paso de apagado solo se entendía de forma parcial.
Un freno celular con muchas funciones
Se sabía previamente que TAX1BP1 es un multitarea que ayuda al sistema de eliminación de residuos de la célula, la autofagia, a reconocer material no deseado. Puede unirse tanto a la carga marcada para eliminación como a las sacos en formación que la engullirán. Los autores se preguntaron si TAX1BP1 también podría ayudar a contener la alarma cGAS–STING. Utilizando células humanas de tipo inmune y macrófagos de ratón carentes de TAX1BP1, encontraron que al activar cGAS o STING se producían muchos más interferones y citocinas inflamatorias que en células normales. Estas células deficientes en TAX1BP1 también eran más resistentes a la infección por el virus herpes simple, coherente con su señalización antiviral sobreactivada.
Limpieza de STING y un Golgi estresado
Al profundizar, los investigadores mostraron que sin TAX1BP1, STING permanecía activo más tiempo y se degradaba más lentamente. La microscopía y pruebas bioquímicas revelaron que STING activo forma grandes agregados y que esos cúmulos se acumulan cuando falta TAX1BP1. Al mismo tiempo, la estructura del Golgi se hincha y fragmenta en pedazos. El equipo descubrió que TAX1BP1, junto con otro ayudante de reciclaje llamado p62, dirige estos fragmentos del Golgi dañados y los agregados de STING sobre ellos hacia la destrucción en los lisosomas—una forma especializada de limpieza que los autores denominan «golfifagia». Este proceso es distinto de la autofagia clásica y masiva y en su lugar emplea vías más selectivas para capturar las piezas sobrecargadas del Golgi.
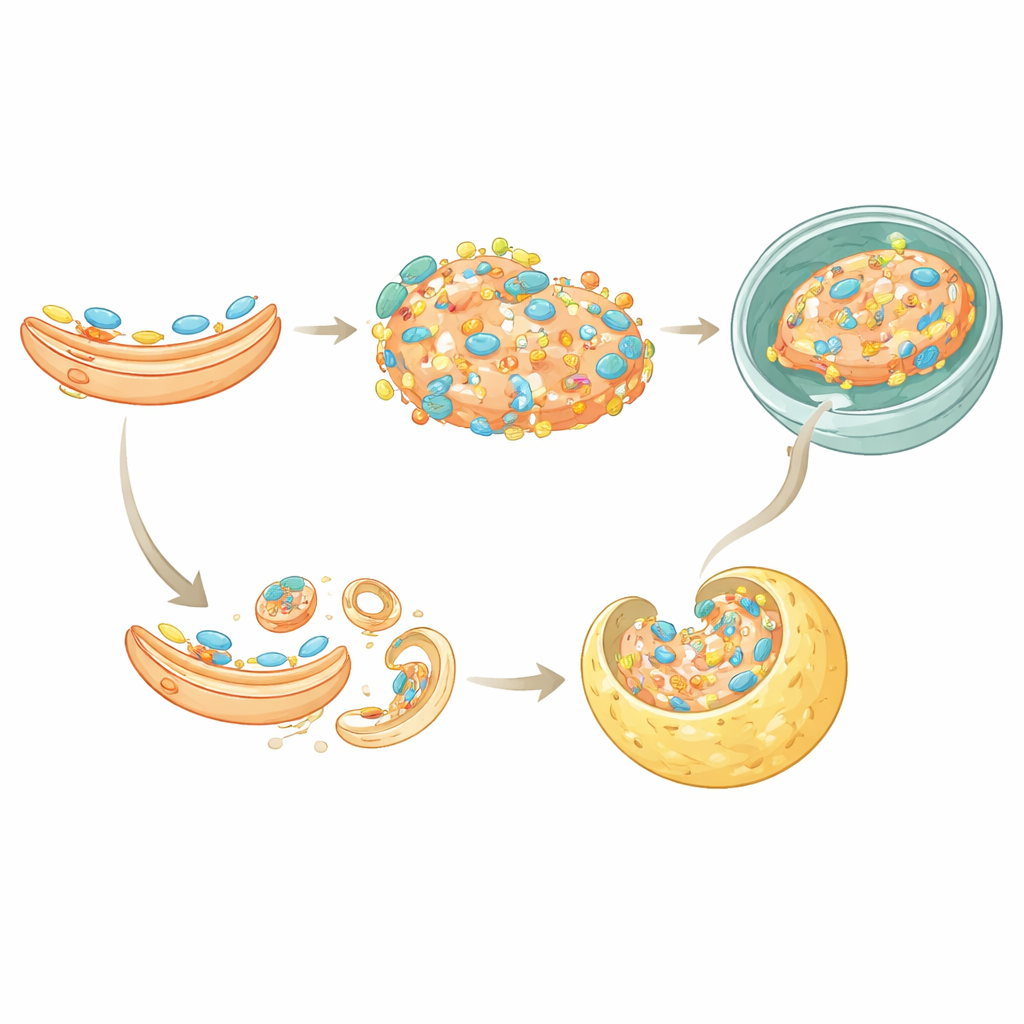
Dos rutas para apagar la alarma
El estudio también descubrió una segunda forma en que TAX1BP1 ayuda a silenciar STING. Normalmente, una vez que STING ha señalado en el Golgi, se empaqueta en pequeñas vesículas que brotan y son reconocidas por un sistema de clasificación de proteínas llamado ESCRT, que a su vez entrega STING a los lisosomas. TAX1BP1 se une directamente a STING y facilita su interacción con un componente clave de ESCRT, HGS. Cuando se eliminó TAX1BP1, la transferencia de STING a esta maquinaria de clasificación fue menos eficiente y su degradación se ralentizó. Sin embargo, parte de su descomposición aún ocurría, lo que indica que TAX1BP1 actúa junto a p62 en esta vía de microautofagia, proporcionando a las células maneras parcialmente redundantes de asegurar que STING no permanezca activo demasiado tiempo.
Por qué esto importa para la salud y la enfermedad
Para probar la importancia de este freno en animales vivos, los investigadores diseñaron ratones carentes de TAX1BP1 específicamente en ciertas células inmunitarias. Cuando se estimularon con un fármaco que activa STING, estos ratones presentaron niveles más altos de interferón y citocinas inflamatorias en sangre que los ratones normales. Al infectarlos con un poxvirus, presentaron menos virus, mostrando una resistencia aumentada. En conjunto, estos hallazgos sugieren que TAX1BP1 conecta el momento de activación de STING en el Golgi con un apagado temporizado mediante la destrucción selectiva tanto de STING como de las membranas del Golgi dañadas. Para un público general, la conclusión es que las células no solo activan una alarma al detectar ADN peligroso, sino que también desmantelan activamente partes de su propio cableado interno para asegurarse de que la alarma se apague. Comprender y, potencialmente, modular este freno interno podría ayudar a diseñar tratamientos para enfermedades inflamatorias crónicas, mejorar las defensas antivirales o ajustar las respuestas inmunitarias en cáncer.
Cita: Suklabaidya, S., Mohanty, S., Reider, I.E. et al. Negative feedback regulation of STING signaling by TAX1BP1-directed Golgiphagy. Nat Commun 17, 2762 (2026). https://doi.org/10.1038/s41467-026-69422-z
Palabras clave: inmunidad innata, vía STING, autofagia, aparato de Golgi, respuesta antiviral