Clear Sky Science · es
La fotoliasa/criptocrómica de Aspergillus nidulans detecta el estrés oxidativo y se desplaza del núcleo a las mitocondrias
Cómo los hongos perciben la luz y el estrés
La luz solar mantiene vivos a las plantas y a los hongos, pero también trae peligros como el daño al ADN y compuestos oxigenados dañinos. Este estudio explora cómo un moho común, Aspergillus nidulans, utiliza una única proteína, llamada CryA, para detectar tanto la luz como el estrés oxidativo y protegerse. Comprender este "sensor dual" no solo amplía nuestro conocimiento sobre cómo los microbios afrontan ambientes hostiles, sino que también puede arrojar luz sobre cómo las células, en general, coordinan señales entre su núcleo y las mitocondrias productoras de energía.
Una enzima reparadora de luz azul con un papel oculto
CryA pertenece a una familia de proteínas conocidas por reparar el daño en el ADN causado por la radiación ultravioleta. Estas proteínas, llamadas fotoliasas y criptocrómicas, usan una molécula que absorbe luz (un flavino) para aprovechar la luz azul y reparar bases de ADN dañadas. Los investigadores confirmaron que CryA tiene la arquitectura clásica de una enzima reparadora del ADN, se une a los cofactors habituales captadores de luz y se agrupa con fotoliasas conocidas en árboles evolutivos. Solo por eso, CryA parecería una herramienta de reparación rutinaria. Sin embargo, trabajos anteriores sugerían que también influye en el desarrollo del hongo, comportándose más como un interruptor regulado por la luz que como una simple máquina molecular.
Un regulador maestro de los genes sensibles a la luz
Para descubrir el lado regulador de CryA, el equipo rastreó su localización en la célula y cómo cambiar su cantidad altera el crecimiento fúngico. Hallaron que en condiciones normales CryA se acumula en el núcleo, donde se almacena el ADN. Cuando eliminaron el gen cryA, el hongo produjo más estructuras sexuales; cuando forzaron la sobreproducción de CryA, casi bloquearon por completo la formación de las esporas asexuales habituales, dejando colonias pálidas y esponjosas. Pruebas de expresión génica mostraron que muchos genes activados por la luz y relacionados con el desarrollo se activaron en exceso sin CryA y quedaron demasiado debilitado cuando CryA se sobreexpresó. En conjunto, estos resultados revelan a CryA como un elemento de retroalimentación negativa: la luz eleva los niveles de cryA, CryA entonces se desplaza al núcleo y modera los genes inducidos por la luz y el desarrollo, evitando que la respuesta se descontrole. 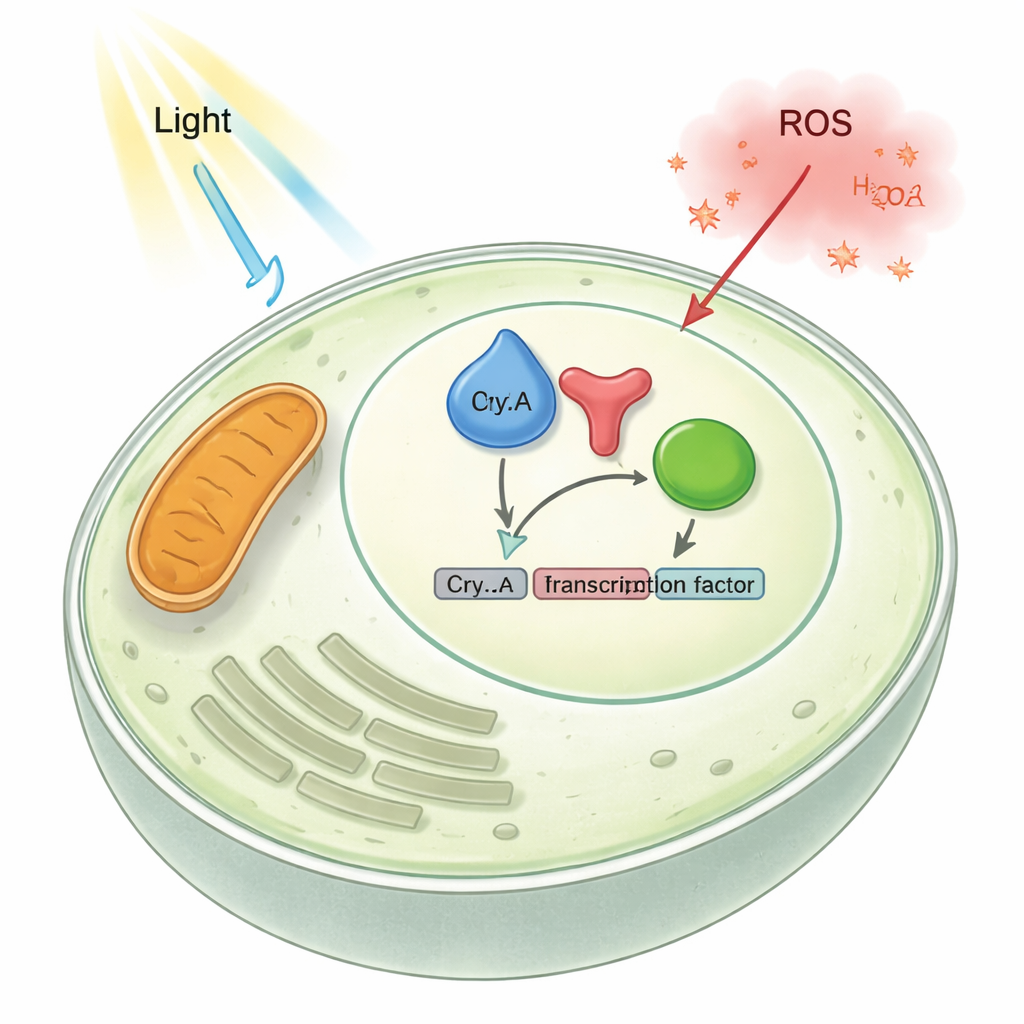
Interacción con las principales vías de luz y estrés
El hongo ya depende de otro fotorreceptor, un sensor de luz roja llamado fitocromo (FphA), y de una vía de estrés que termina en un factor de transcripción denominado AtfA. Usando pruebas de interacción proteína–proteína en células vivas y con proteínas purificadas, los investigadores mostraron que CryA se une físicamente tanto a FphA como a AtfA en el núcleo. Cuando cryA fue eliminado, los genes normalmente activados por la luz roja a través del fitocromo se expresaron con mayor intensidad; cuando cryA se sobreexpresó, resultaron más difíciles de activar. Experimentos de cromatina indicaron que, en ausencia de CryA, un gen clave sensible a la luz presenta más marcas histónicas activadoras, lo que sugiere que CryA normalmente atenúa la actividad de apertura de la cromatina impulsada por el fitocromo. En efecto, CryA frena tanto al sensor de luz como al factor de transcripción aguas abajo, actuando como un freno compartido para la señalización de luz y estrés.
Un sensor rápido de estrés que salta a las mitocondrias
El estrés oxidativo —un exceso de especies reactivas de oxígeno como el peróxido de hidrógeno— supone una amenaza constante para las células. Los autores encontraron que dicho estrés, al igual que la luz, aumenta la expresión de cryA. De manera llamativa, cuando se añadió peróxido de hidrógeno, CryA se trasladó del núcleo a las mitocondrias en menos de un minuto. Este salto requirió una extensión corta y flexible en el extremo N-terminal de la proteína y, en particular, un único aminoácido cisteína dentro de ella. Cuando esa cisteína se cambió por otro residuo, CryA ya no pudo abandonar el núcleo ante el estrés. La eliminación de la cola N-terminal obligó a CryA a ubicarse de forma permanente en las mitocondrias. Estas cepas modificadas respondieron de manera distinta a los oxidantes: las versiones de CryA confinadas solo al núcleo o solo a las mitocondrias alteraron la resistencia del hongo al peróxido de hidrógeno y a la menadiona y remodelaron la expresión de genes antioxidantes. Los hallazgos sugieren que CryA hace más que detectar estrés: puede ayudar a coordinar la comunicación entre mitocondrias y núcleo para que las defensas antioxidantes se ajusten al tipo y nivel de daño. 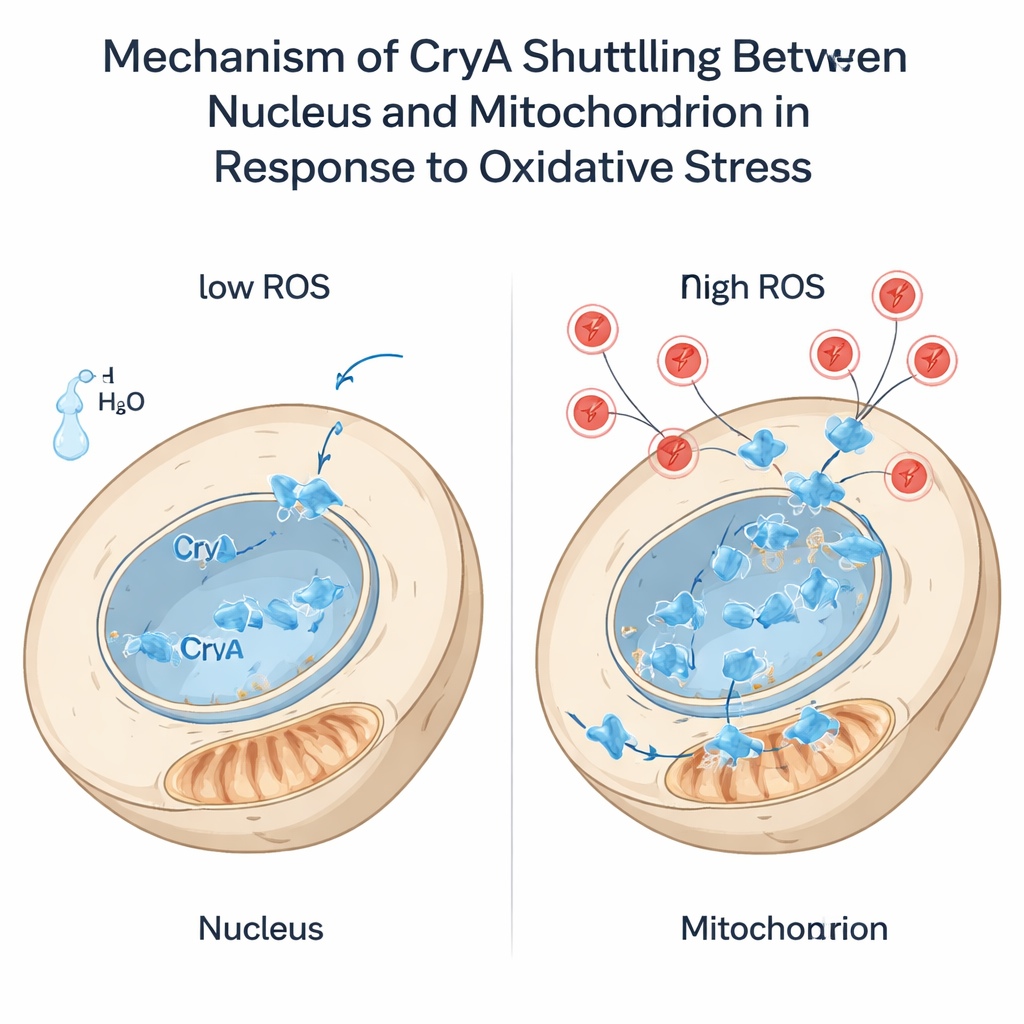
Por qué esto importa
Para un no especialista, CryA puede entenderse como un agente regulador celular que vigila tanto la luz exterior como el estrés oxidativo interior y decide cuándo frenar el crecimiento, el desarrollo y la actividad génica. Al desplazarse entre el núcleo y las mitocondrias y conectarse con rutas de señalización principales, evita que el hongo reaccione en exceso a la luz o al estrés, al mismo tiempo que permite una respuesta protectora rápida. Proteínas y mecanismos similares existen en muchos organismos, por lo que este trabajo ofrece una ventana sobre cómo las células integran las señales ambientales con las señales internas de daño para sobrevivir en un mundo cambiante.
Cita: Landmark, A., Rudolf, T., Hundshammer, K. et al. The photolyase/cryptochrome of Aspergillus nidulans senses oxidative stress and shuttles from nuclei to mitochondria. Nat Commun 17, 1483 (2026). https://doi.org/10.1038/s41467-026-69403-2
Palabras clave: detección de la luz, estrés oxidativo, criptocrómica, mitocondrias, desarrollo fúngico