Clear Sky Science · es
El lactato derivado de macrófagos impulsa la remodelación fenotípica de los fibroblastos dérmicos mediante la lactilación de la lisina 23 de la histona H3 primada por MCT1 en la cicatriz hipertrófica
Por qué algunas cicatrices se engrosan y elevan
La mayoría de los cortes y quemaduras acaban convirtiéndose en cicatrices finas y planas. Pero algunas heridas cicatrizan con bandas de tejido gruesas y elevadas llamadas cicatrices hipertróficas, que pueden picar, doler y limitar el movimiento. Este estudio descubre un impulsor inesperado de esas cicatrices persistentes: un subproducto metabólico común llamado lactato, producido por células inmunes en piel rígida en proceso de curación, que reprogrma a las células reparadoras vecinas para comportarse de forma más agresiva y favorecedora de la formación de cicatriz.
De la reparación normal a la cicatriz problemática
En la cicatrización saludable, las células de la piel colaboran para cerrar la lesión y reconstruir el tejido. Los fibroblastos, las principales células reparadoras de la capa profunda de la piel, pasan brevemente a un estado más activo que produce colágeno, la proteína que sirve como armazón de la piel. Una vez sellada la herida, estas células vuelven a calmarse. En las cicatrices hipertróficas, sin embargo, los fibroblastos permanecen atrapados en este estado sobreactivado, depositando demasiado colágeno en haces gruesos y desorganizados. Los autores empezaron comparando piel normal con tejido de cicatriz hipertrófica y encontraron un cambio metabólico claro: el microambiente de la cicatriz favorecía una química de quema rápida de azúcar que genera grandes cantidades de lactato, junto con altos niveles de una proteína transportadora llamada MCT1 que transporta lactato dentro de las células. 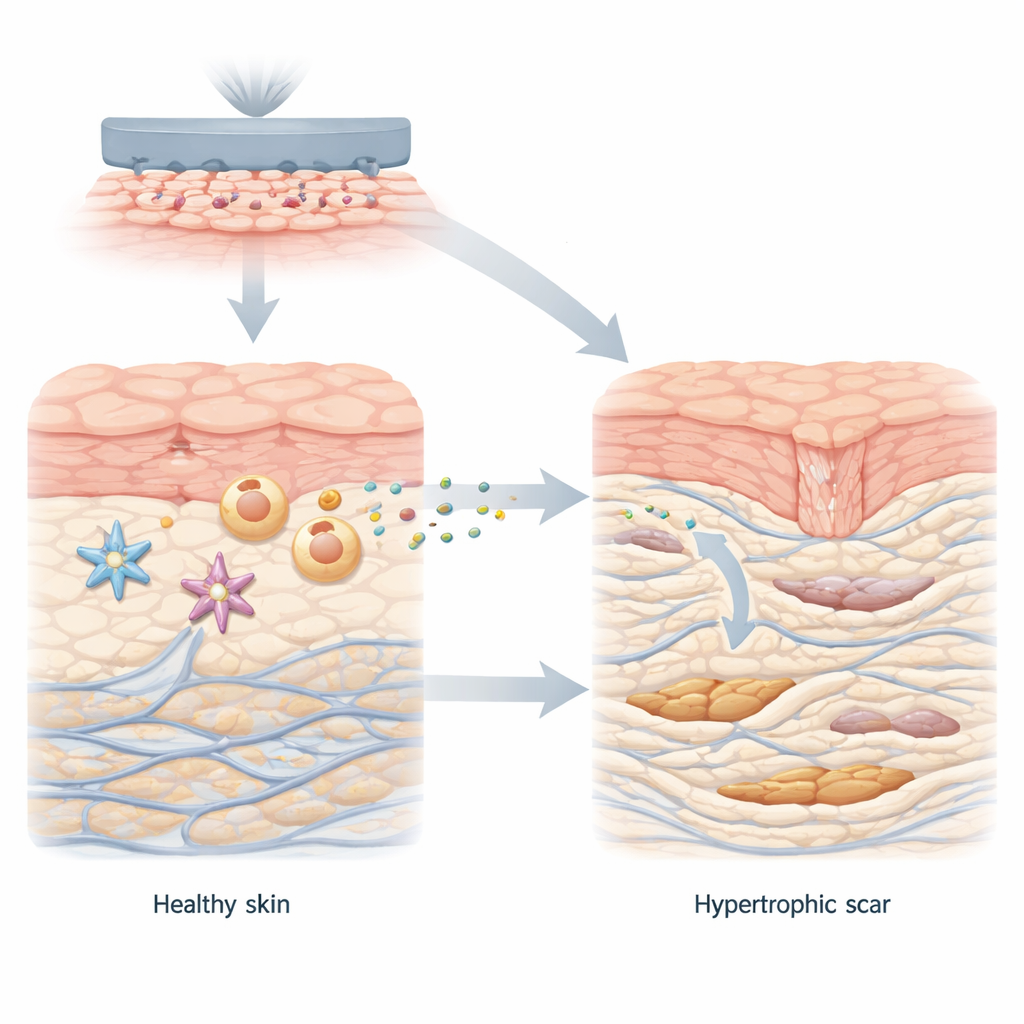
Las células inmunes como fábricas inesperadas de lactato
Para descubrir de dónde procede tanto lactato, el equipo examinó distintos tipos celulares de piel humana y modelos en ratón: macrófagos (células inmunes que limpian restos y coordinan la curación), células de vasos sanguíneos y fibroblastos. Cultivaron estas células sobre materiales suaves o rígidos que imitan la piel normal y la cicatrizada. En superficies rígidas, solo los macrófagos cambiaron a un modo altamente glucolítico, ávido de azúcar, y expulsaron grandes cantidades de lactato, tanto en placas de cultivo como en tejido cicatricial real. Cuando se eliminaron los macrófagos de heridas en ratones, los niveles de lactato tisular disminuyeron y la formación de cicatriz se redujo. Estos resultados señalan a los macrófagos, especialmente los que perciben un entorno rígido, como las principales fábricas de lactato que moldean el microambiente de la cicatriz.
El lactato como señal que reconfigura a los fibroblastos
A continuación, los investigadores preguntaron cómo afecta este exceso de lactato a los fibroblastos. Cuando los fibroblastos se expusieron a un fluido rico en lactato procedente de macrófagos cultivados en condiciones rígidas, se multiplicaron más rápido, se movieron más y produjeron más colágeno, todos rasgos característicos del estado agresivo de los miofibroblastos. Bloquear el transportador MCT1 en los fibroblastos, o reducir la producción de lactato en los macrófagos, redujo drásticamente estos cambios. Dentro de los fibroblastos, el lactato entrante hizo más que servir de combustible: desencadenó una marca química específica en proteínas histonas, que empaquetan el ADN en el núcleo celular. Esta marca, llamada lactilación de H3K23, era mucho más alta en fibroblastos formadores de cicatriz que en los normales y actuaba como un interruptor que activaba dos genes clave, HEY2 y COL11A1, que en conjunto amplifican las señales pro-cicatriz.
Un bucle de cicatrización auto-reforzante
Las proteínas impulsadas por esta modificación de histonas forman un potente circuito de retroalimentación. HEY2 aumenta la actividad de una vía que involucra a YAP1 y SMAD2, conocida por empujar a los fibroblastos hacia un estado más contractil y productor de colágeno. COL11A1, una proteína estructural relacionada con el colágeno, interactúa físicamente con el transportador MCT1 en los fibroblastos, ayudando a estabilizarlo y a hacer más eficiente la captación de lactato. En otras palabras, la entrada de lactato en la célula cambia la regulación génica de un modo que mejora aún más la entrada de lactato y la producción de colágeno, fijando a los fibroblastos en una identidad pro-cicatriz. 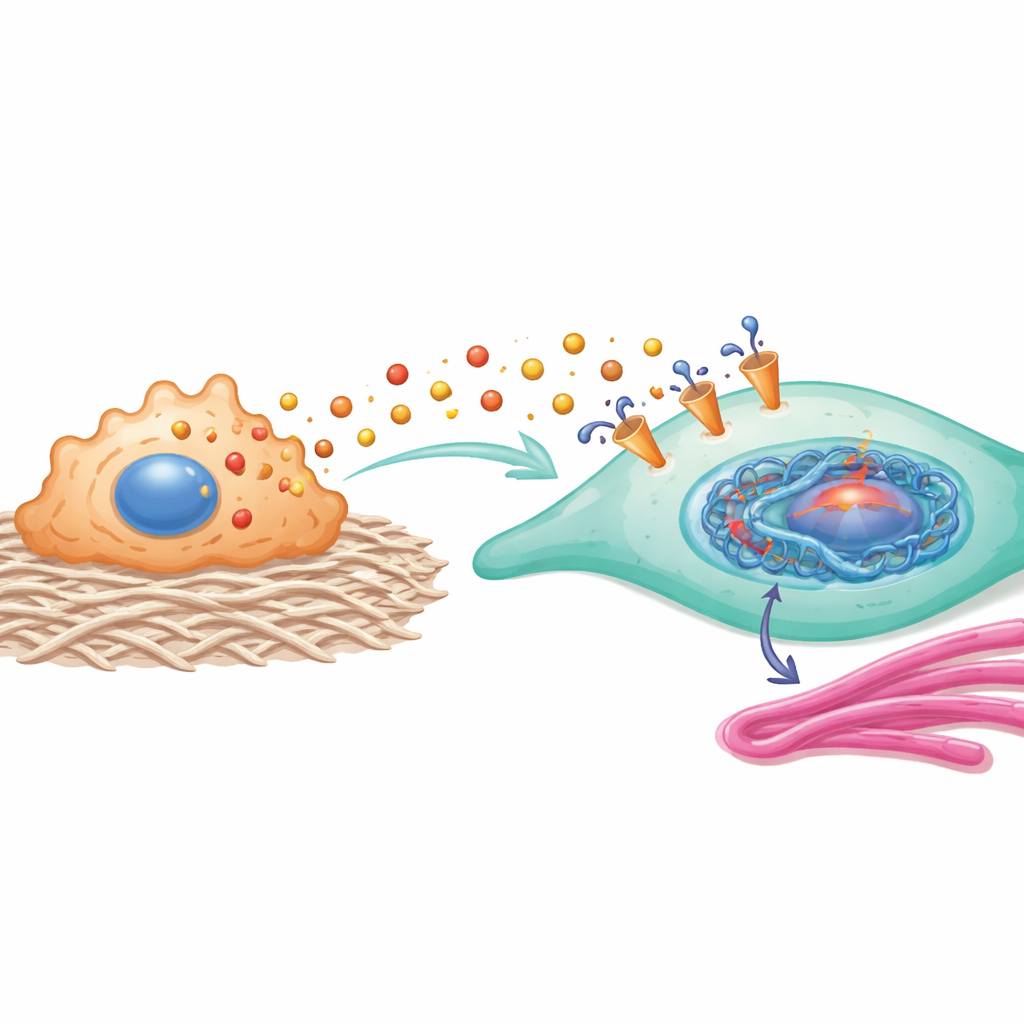
Atenuar el bucle para mejorar la cicatrización
Para comprobar si interrumpir este bucle puede mejorar la cicatrización, el equipo utilizó ratones en los que MCT1 podía eliminarse selectivamente de los fibroblastos, así como un fármaco que bloquea MCT1. En ambos casos, las heridas cerraron más rápido, la piel recién formada se veía más organizada y las fibras de colágeno eran más delgadas y mejor alineadas, con menos rasgos de cicatrización hipertrófica. La marca específica de histona y sus genes diana también disminuyeron. Agotar los macrófagos, la principal fuente de lactato, o reducir químicamente el lactato produjo efectos anti-cicatriz similares. Estos experimentos muestran que la cadena herida rígida–macrófago–lactato–fibroblasto no es solo una correlación, sino un motor clave de la cicatrización patológica.
Qué significa esto para futuros tratamientos de cicatrices
Este trabajo redefine al lactato, de simple residuo metabólico, a mensajero potente que enlaza mecánica, metabolismo y control génico en la cicatrización. Al mostrar cómo el lactato derivado de macrófagos, transportado a través de MCT1, altera histonas y activa un programa de cicatrización auto-reforzante en fibroblastos, el estudio destaca varios objetivos terapéuticos prometedores. Fármacos que modulen la producción de lactato, bloqueen MCT1 o interfieran con la modificación específica de histonas podrían, algún día, ayudar a que las heridas cicatricen más rápido y con cicatrices más planas y menos visibles.
Cita: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Palabras clave: cicatriz hipertrófica, señalización por lactato, interacción macrófago–fibroblasto, lactilación de histonas, terapia de cicatrización de heridas