Clear Sky Science · es
Mioferlina es un componente de las vesículas de tráfico vRNP en fases tardías para virus ARN envueltos
Por qué esto importa para la salud cotidiana
La gripe estacional y otras infecciones respiratorias pueden parecer rutinarias, pero juntas matan a millones de personas en todo el mundo cada año. Muchos de estos virus, incluidos el virus de la influenza A y el virus respiratorio sincitial (VRS), ya eluden vacunas y antivirales al mutar rápidamente. Este estudio se centra en cambio en algo que los virus no pueden cambiar fácilmente: la maquinaria celular humana que secuestran para escapar de las células infectadas. Al descubrir un punto débil compartido en esa maquinaria, el trabajo apunta hacia futuros fármacos que podrían contener de forma simultánea una amplia gama de virus respiratorios.
Una ruta celular de transporte que explotan los virus
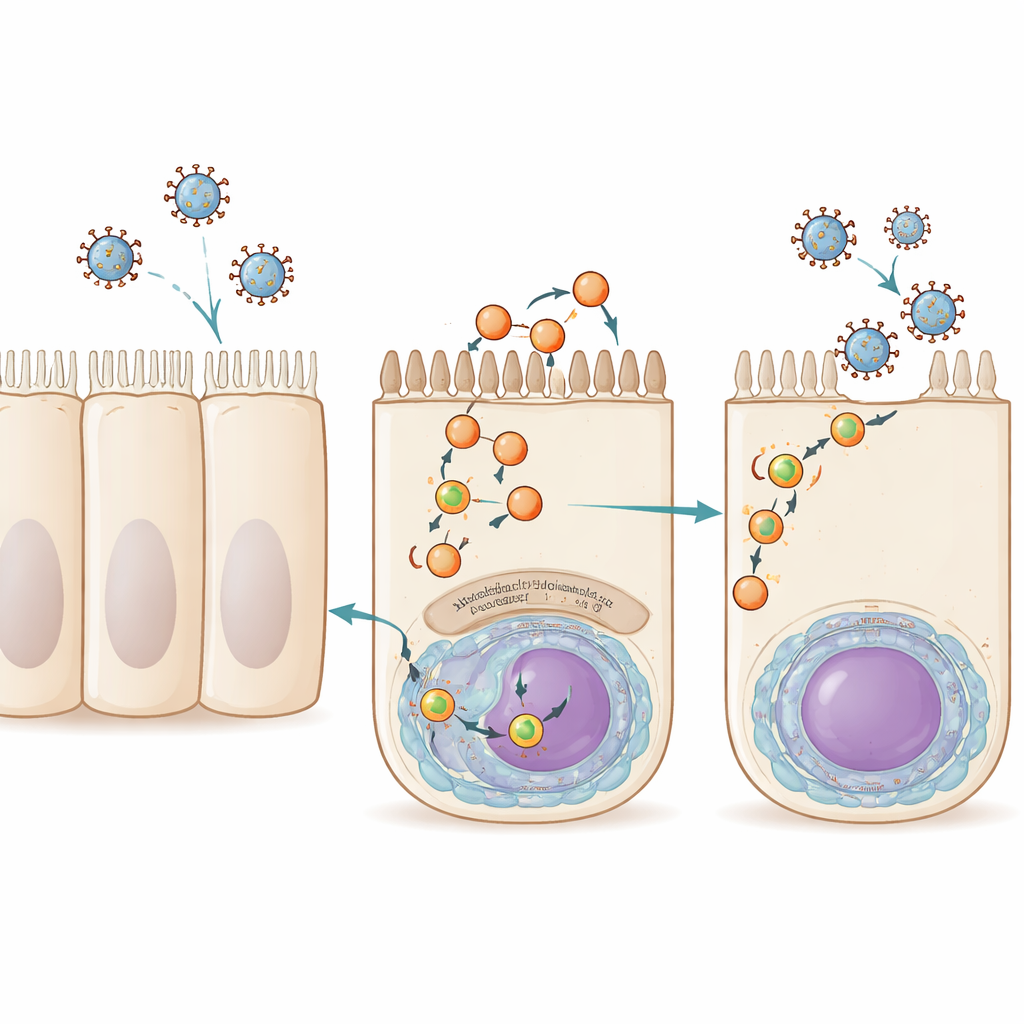
Nuestras células de las vías respiratorias reutilizan constantemente fragmentos de su membrana externa mediante un proceso llamado reciclaje. Pequeñas burbujas membranosas, o vesículas, transportan carga desde el interior de la célula de vuelta a la superficie, guiadas por una familia de proteínas conocidas colectivamente como Rab11. El virus de la influenza A, el VRS y un virus relacionado llamado virus de Sendai explotan esta ruta en la fase tardía de la infección. Cargan su material genético, empaquetado en complejos ribonucleoproteicos, sobre vesículas que contienen Rab11 que los llevan al lado superior (orientado a las vías respiratorias) de la célula, donde nuevas partículas virales brotan y se propagan. Hasta ahora, Rab11 era el único factor del huésped claramente compartido por estas vesículas de tráfico, lo que dejaba una gran laguna en nuestra comprensión de cómo se forman y funcionan.
Encontrando un nuevo actor: la mioferlina
Los investigadores empezaron preguntándose qué proteínas humanas se asocian físicamente con la maquinaria de empaquetamiento genómico de la influenza en distintos momentos de la infección. Diseñaron un virus de influenza A cuya polimerasa llevaba una etiqueta molecular y luego usaron espectrometría de masas para catalogar las proteínas humanas unidas a este complejo al inicio y en fases tardías de la infección. Entre cientos de candidatas, una destacó en los puntos temporales tardíos: la mioferlina, una proteína asociada a membranas de gran tamaño previamente relacionada con el desarrollo muscular, la endocitosis y la reparación de membranas. Cuando el equipo redujo los niveles de mioferlina en células derivadas de pulmón usando ARN pequeños interferentes o la bloqueó con un inhibidor de pequeña molécula, las células seguían produciendo ARN viral y proteínas virales con normalidad, pero liberaban muchas menos partículas infecciosas de influenza. Esto indicó que la mioferlina no es necesaria para copiar el genoma viral, pero sí es crucial para las etapas tardías cuando los nuevos virus se ensamblan y salen de la célula.
La mioferlina viaja con la carga viral
Imágenes de alta resolución revelaron dónde se sitúa la mioferlina durante la infección. En células no infectadas, la mioferlina se solapa en gran medida con las vesículas de reciclaje positivas para Rab11, tanto cerca del núcleo como hacia el borde celular, y la pérdida de cualquiera de las dos proteínas altera la distribución normal de la otra. Durante la infección por influenza, la red de Rab11 se remodela de forma drástica en vesículas agrandadas e irregulares que transportan ribonucleoproteínas virales. La mioferlina se conserva en estas vesículas remodeladas y muestra una fuerte colocalización con el genoma viral y Rab11. Cuando el equipo usó un fármaco que fuerza a los complejos del genoma viral y a sus vesículas transportadoras a agregarse, la mioferlina fue arrastrada a los mismos agregados, confirmando que es un componente integrante de estas estructuras de tráfico en fases tardías y no simplemente una presencia fortuita en las proximidades.
Un centro compartido por múltiples virus respiratorios
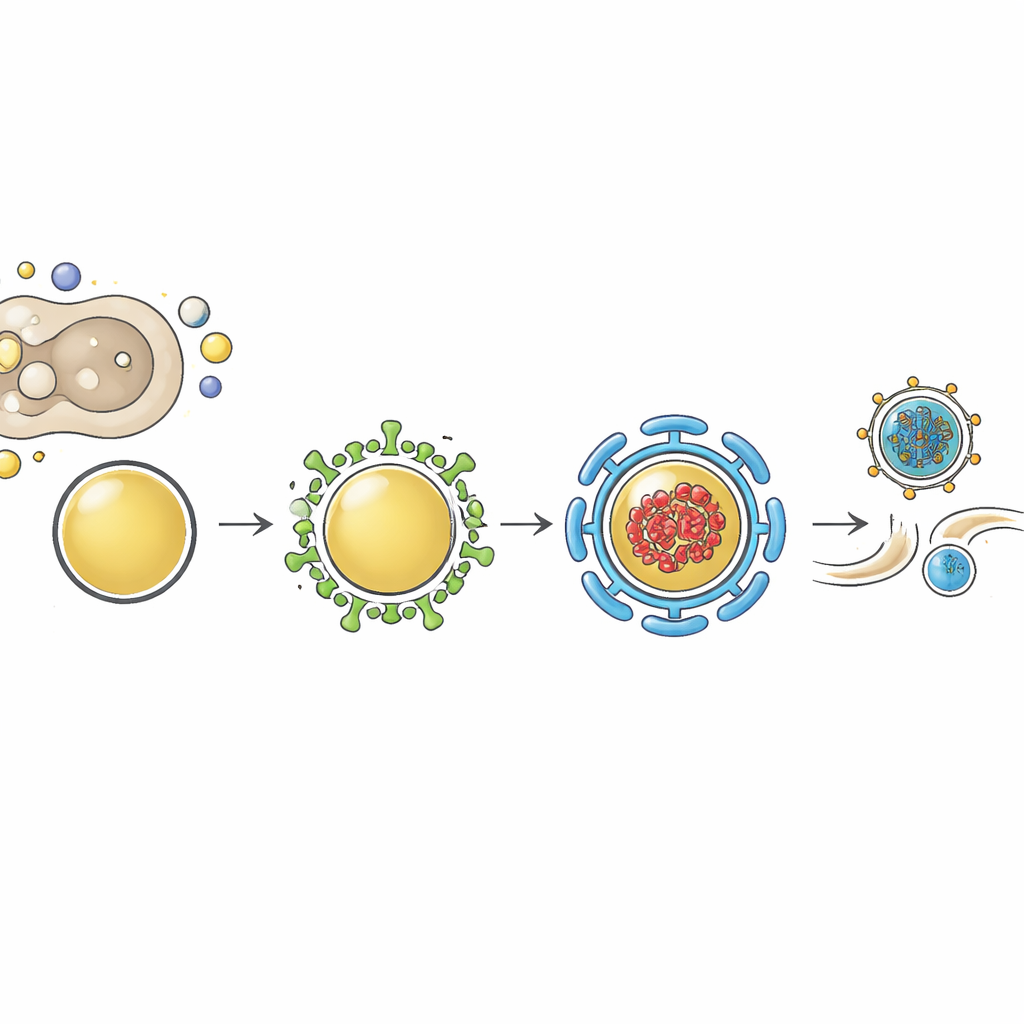
El estudio preguntó luego si esta dependencia de la mioferlina es única de la influenza o si es más ampliamente compartida. La reducción de mioferlina en células pulmonares infectadas con VRS o con el virus de Sendai provocó nuevamente una fuerte caída en el número de virus infecciosos liberados, sin disminuir los niveles de ARN viral. La imagen de una sola molécula mostró los genomas de ambos virus agrupándose junto con la mioferlina y Rab11 en puntos citoplasmáticos que probablemente representan centros de transporte más que fábricas de replicación. Este patrón respalda una imagen unificadora: diferentes virus respiratorios de ARN envueltos, a pesar de sus estilos de vida diversos, convergen en el mismo sistema de vesículas Rab11–mioferlina cuando llega el momento de mover sus genomas completos hacia la superficie celular para su empaquetamiento y salida.
Cómo la mioferlina moldea las vesículas que llevan virus
La mioferlina está formada por múltiples dominios "C2" que pueden unirse a membranas y proteínas asociadas. Trabajos anteriores mostraron que uno de estos dominios interactúa con una familia de proteínas remodeladoras de membrana llamadas EHD. En este estudio, EHD1 y EHD2 etiquetadas con fluorescencia se encontraron dentro de las mismas vesículas remodeladas que transportan genomas de influenza y Rab11, especialmente cuando estas vesículas se agruparon experimentalmente. La reducción de los niveles de EHD2, al igual que la reducción de mioferlina, disminuyó los rendimientos de influenza sin afectar la replicación del genoma. Además, la eliminación de la mioferlina provocó una caída en los niveles de proteína EHD2, lo que sugiere que la mioferlina ayuda a estabilizar o posicionar correctamente a EHD2 en las membranas. Los autores proponen que la mioferlina se asienta en vesículas positivas para Rab11 y recluta proteínas EHD para esculpir sus membranas, completando la formación de "vesículas recubiertas irregularmente" especializadas que están optimizadas para transportar carga viral hacia los sitios de gemación.
Qué significa esto para futuras estrategias antivirales
En conjunto, los hallazgos sitúan a la mioferlina como un organizador central de una ruta de reciclaje del huésped de la que dependen muchos virus respiratorios envueltos en un paso tardío crítico. Dado que dirigirse solo a las proteínas virales a menudo conduce a una resistencia rápida, los factores del huésped reutilizados por múltiples virus son objetivos farmacológicos atractivos. Interferir con la función de la mioferlina, o con su asociación con Rab11 y las proteínas EHD, podría en principio ralentizar o bloquear la propagación de patógenos diversos, desde la influenza y el VRS hasta otros virus dependientes de Rab11, como algunos coronavirus. Aún queda mucho trabajo para traducir este concepto en terapias seguras, pero el estudio ofrece un mapa detallado de una vía de escape viral compartida y destaca a la mioferlina como un prometedor punto de estrangulamiento a lo largo de ese camino.
Cita: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Palabras clave: gripe, virus respiratorios, tráfico vesicular, factores del huésped, mioferlina