Clear Sky Science · es
Nanovesículas exosomales diseñadas para la entrega de anticuerpos en el tratamiento de la enfermedad inflamatoria intestinal
Nueva esperanza para una enfermedad intestinal persistente
La enfermedad inflamatoria intestinal (EII) puede convertir la vida cotidiana en una batalla constante contra el dolor, la diarrea y la fatiga, y además aumenta el riesgo a largo plazo de cáncer de colon. Muchos fármacos actuales calman los brotes pero no restablecen de forma duradera las reacciones inmunitarias defectuosas que impulsan la enfermedad, por lo que los síntomas suelen reaparecer. Este estudio presenta una nanopartícula “inteligente” ingeniosamente diseñada que viaja por el torrente sanguíneo, localiza las zonas inflamadas del intestino y entrega un tratamiento de dos partes concebido tanto para reducir la inflamación dañina como para reconstruir un equilibrio inmunitario duradero.
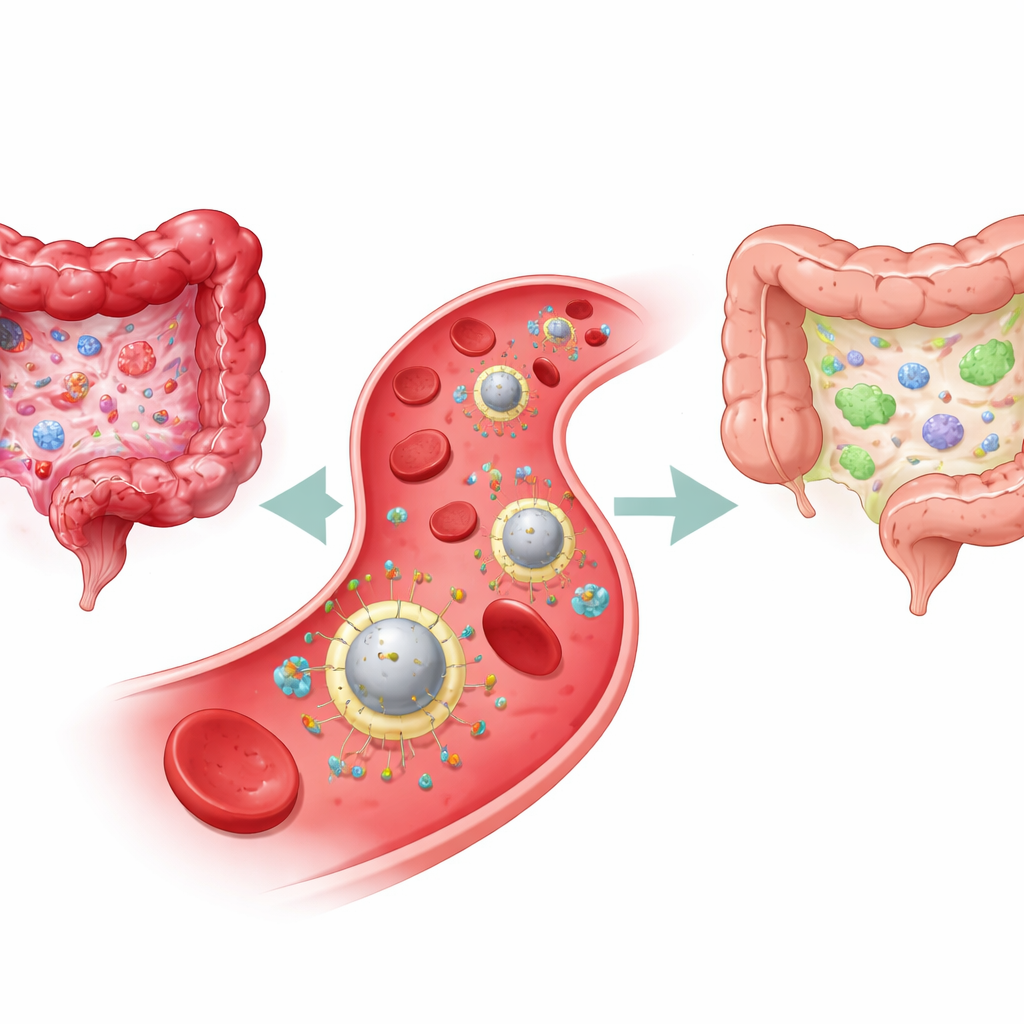
Por qué los tratamientos actuales se quedan cortos
La EII, que incluye la enfermedad de Crohn y la colitis ulcerosa, surge de una lucha crónica en el sistema inmunitario intestinal. Por un lado están las células inmunitarias agresivas y las moléculas inflamatorias que dañan el revestimiento intestinal; por el otro, las células regulatorias que normalmente mantienen esta respuesta bajo control. Las terapias estándar —como los esteroides, los inmunosupresores y los fármacos biológicos— intentan principalmente atenuar la inflamación en todo el cuerpo. Pueden aliviar los síntomas, pero a menudo hacen poco por restaurar el equilibrio inmunitario subyacente, y la supresión inmune generalizada puede aumentar el riesgo de infecciones. Incluso los anticuerpos más modernos que bloquean una señal inflamatoria clave llamada interleucina-23 (IL-23) benefician solo a una parte de los pacientes y siguen circulando ampliamente, no solo donde se necesitan.
Construyendo un medicamento que localiza y cambia de forma
Los investigadores se propusieron diseñar un tratamiento que se comportara más como una célula viva que como un fármaco simple. Partieron de pequeñas burbujas liberadas de forma natural por células T reguladoras —células inmunitarias que fomentan la tolerancia y la pacificación. Estas vesículas, llamadas exosomas, transportan proteínas y material genético que pueden empujar a otras células inmunitarias hacia un modo calmado. El equipo fusionó estos exosomas con fragmentos de membrana plaquetaria, aprovechando la capacidad de las plaquetas para adherirse a los vasos sanguíneos dañados en tejido inflamado. En la superficie de esta envoltura híbrida fijaron anticuerpos bloqueantes de IL-23 mediante una “cuerda” molecular que puede ser cortada por enzimas (metaloproteinasas de matriz) que abundan únicamente en el tejido intestinal inflamado. El resultado, denominado PrEXO-a23, es una nanovesícula que circula en la sangre, se adhiere a los vasos intestinales lesionados y libera su carga de anticuerpos solo donde la enfermedad está activa.
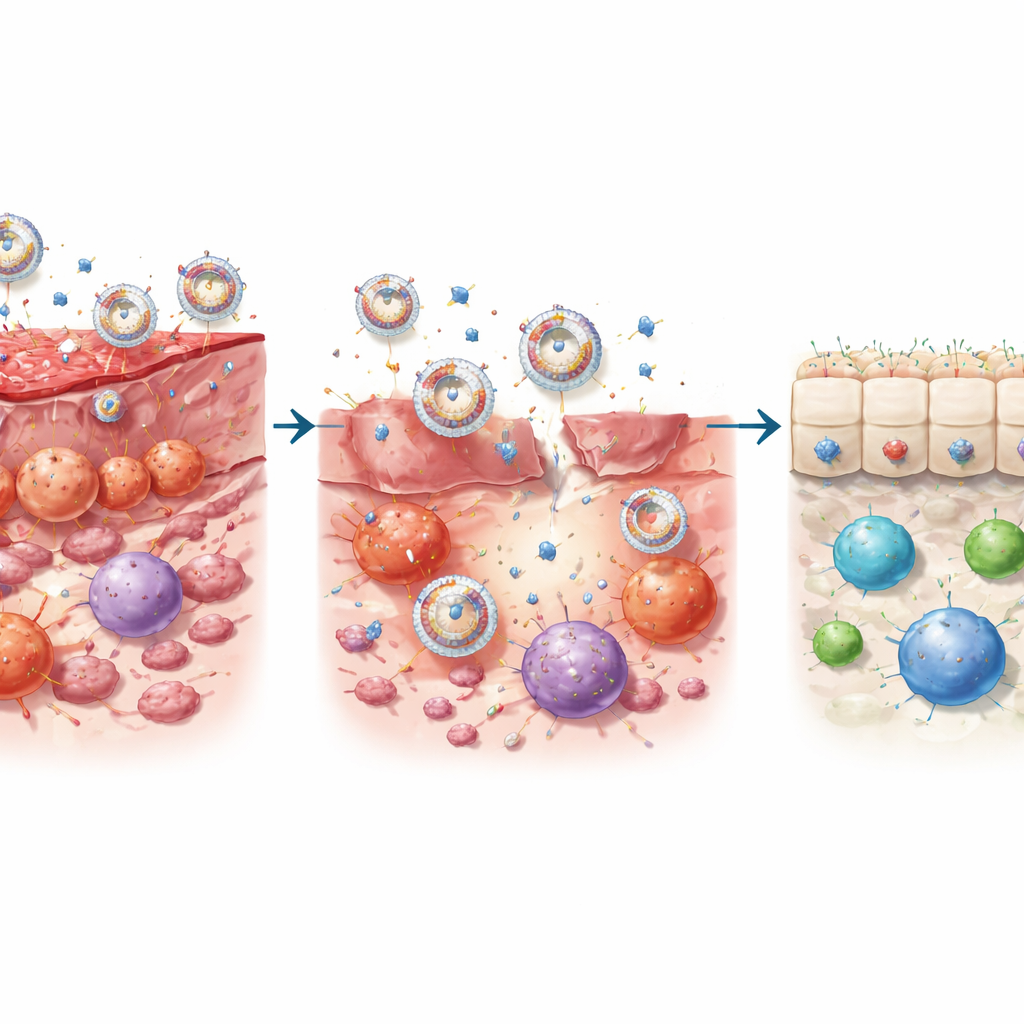
Reeducando el entorno inmunitario intestinal
En estudios celulares, PrEXO-a23 superó tanto al anticuerpo como a los exosomas por separado. Redujo con fuerza la formación de células T helper 17 (Th17) inflamatorias y la liberación de citocinas dañinas que lesionan el revestimiento intestinal, al tiempo que protegía a las células epiteliales intestinales humanas de la muerte. Paralelamente, empujó a las células dendríticas —guardianes que instruyen a las células T— fuera de un estado hostil y activador hacia un estado “tolerante” que fomenta el crecimiento de células T reguladoras. En modelos murinos de colitis, las nanovesículas se dirigieron de forma eficiente al tejido de colon inflamado, fueron absorbidas por múltiples tipos de células inmunitarias y liberaron anticuerpos en respuesta a la actividad enzimática local. Esta acción dual —bloquear la inflamación impulsada por IL-23 y potenciar señales que promueven la tolerancia— llevó los marcadores inflamatorios cerca de niveles normales y restauró una mezcla más saludable de tipos de células T.
Reparación del tejido y prevención del daño a largo plazo
Los ratones con colitis inducida químicamente que recibieron PrEXO-a23 perdieron menos peso, mostraron colones más largos y saludables y un menor agrandamiento del bazo, signo de inflamación sistémica. El examen microscópico reveló una arquitectura intestinal preservada y uniones más estrechas entre células epiteliales, lo que indica una barrera reparada. El tratamiento también ayudó a reequilibrar la microbiota intestinal, aumentando familias bacterianas asociadas con la salud intestinal y reduciendo las vinculadas a la enfermedad. En un modelo más severo que imita la progresión de la colitis crónica al cáncer de colon, PrEXO-a23 no solo alivió la inflamación continua sino que previno por completo el desarrollo de tumores y redujo el engrosamiento y la cicatrización de la pared intestinal característicos de la fibrosis. Los análisis moleculares apuntaron a la restauración de la señalización protectora de p53 —un guardián central contra el cáncer— que resultó importante para el efecto anticancerígeno.
Hacia una atención de la EII más inteligente y duradera
Para un público no especialista, el mensaje clave es que este trabajo va más allá de simplemente “reducir” la inflamación. Al combinar entrega dirigida, liberación local de anticuerpos y carga exosomal con efecto inmunosupresor en un solo paquete diminuto, PrEXO-a23 calma la enfermedad activa y ayuda a reentrenar el sistema inmunitario hacia una tolerancia duradera. En ratones, esto condujo no solo al alivio de los síntomas, sino también a la protección frente a la cicatrización y el cáncer de colon, dos de las complicaciones más temidas de una EII de larga evolución. Aunque quedan muchas pruebas antes de que una terapia así pueda llegar a los pacientes, el estudio muestra cómo las nanomedicinas inspiradas biológicamente podrían algún día ofrecer un control más preciso y duradero de trastornos inmunitarios complejos como la EII.
Cita: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Palabras clave: enfermedad inflamatoria intestinal, nanomedicina, tolerancia inmunitaria, exosomas, prevención del cáncer colorrectal