Clear Sky Science · es
Defectos estructurales en los fibrilos de amyloid-β impulsan la nucleación secundaria
Por qué importan las pequeñas imperfecciones en las proteínas del cerebro
En el Alzheimer y en enfermedades cerebrales relacionadas, ciertas proteínas se agrupan en estructuras largas y filiformes llamadas fibrillas amiloides. Estas fibrillas no solo son un sello de la enfermedad; también contribuyen a generar nuevas partículas proteicas altamente tóxicas que pueden dañar las células cerebrales. Este estudio plantea una pregunta simple pero potente: ¿actúan las raras “fallas” estructurales en el interior de las fibrillas amiloides como los principales puntos calientes que desencadenan un nuevo crecimiento dañino? La respuesta podría indicar nuevas formas de frenar o detener estos trastornos atacando solo unos pocos sitios críticos en lugar de toda la superficie proteica. 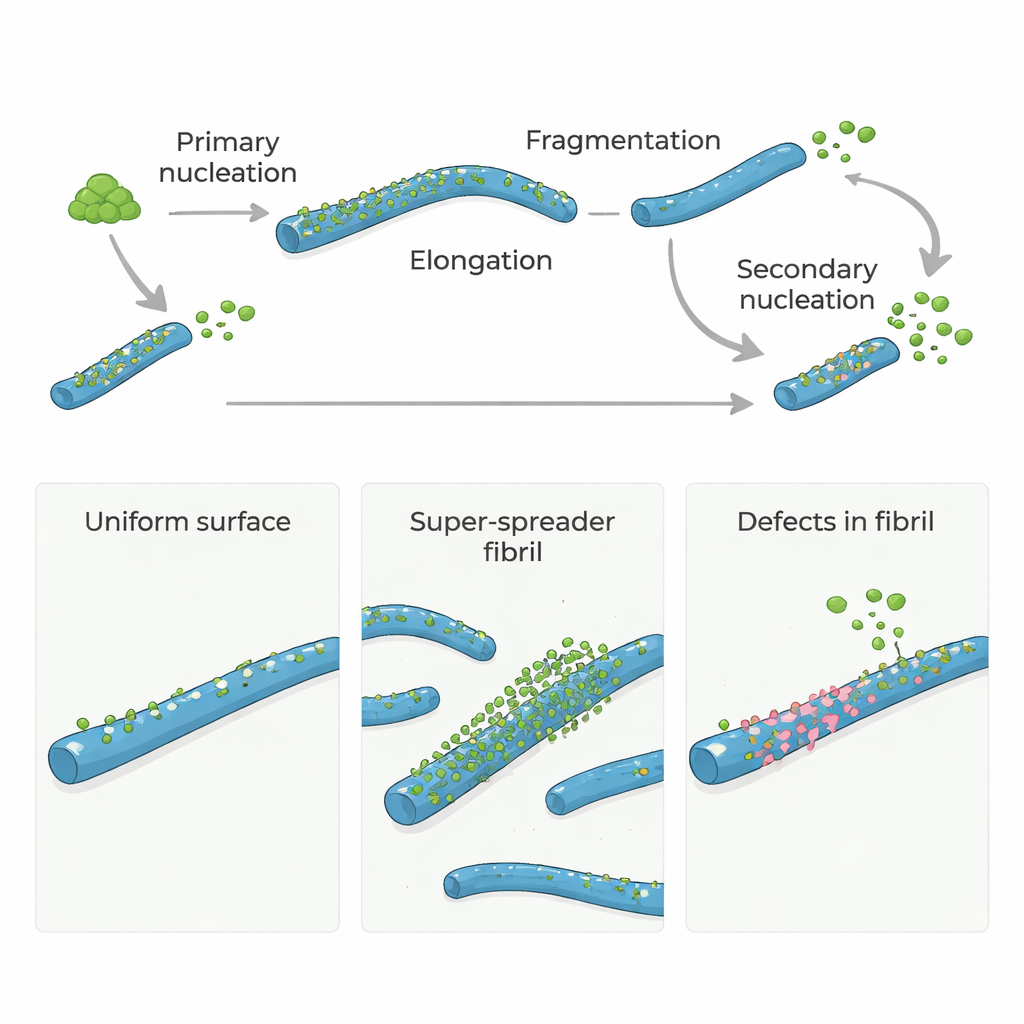
De una proteína tranquila a una reacción en cadena desbocada
Las proteínas amyloid-β (Aβ), centrales en la enfermedad de Alzheimer, no suelen agregarse por sí solas con rapidez. Para empezar, unos pocos monómeros deben ensamblarse lentamente en las primeras fibrillas diminutas, un paso denominado nucleación primaria. Una vez que existen estas fibrillas iniciales, crecen rápidamente a medida que más monómeros se añaden a sus extremos. Aún más importante, las fibrillas existentes pueden provocar la aparición de nuevas fibrillas en sus superficies mediante un proceso conocido como nucleación secundaria. Este paso impulsado por la superficie puede inundar el sistema con nuevas fibrillas y oligómeros pequeños y tóxicos, convirtiendo un goteo lento en una reacción en cadena descontrolada.
¿Son todas las superficies de fibrillas igualmente peligrosas?
Muchos modelos han supuesto que toda la superficie de una fibrilla amiloide es igualmente eficaz para catalizar la nucleación secundaria. Sin embargo, experimentos recientes sugirieron que solo una pequeña fracción de la superficie es realmente activa. Para explorar esto, los autores emplearon una «chaperona» molecular natural llamada Brichos, conocida por bloquear la nucleación secundaria de Aβ40 y Aβ42 (dos formas clave de amyloid-β). Midiendo con cuidado cuánto Brichos marcado fluorescente se adhiere a las fibrillas, hallaron que se une con afinidad pero en números muy bajos: aproximadamente una molécula de Brichos por cada 100–150 moléculas de Aβ en una fibrilla. No obstante, esta cobertura escasa fue suficiente para suprimir más del 90% de la nucleación secundaria, lo que significa que solo sitios raros y localizados —en lugar de toda la superficie— dominan la producción de nuevos ensamblajes tóxicos.
Investigando el papel de los defectos ocultos
Estos hallazgos sugirieron que los sitios de nucleación cruciales podrían ser defectos estructurales: pequeñas irregularidades formadas durante el crecimiento de las fibrillas, como capas desalineadas o núcleos internos parcialmente expuestos. Para probar esta idea de forma directa, los investigadores crecieron fibrillas de Aβ40 bajo dos condiciones diferentes. Un conjunto, las fibrillas «control», se formó en condiciones típicas de fuerte sobresaturación que favorecen el crecimiento rápido y el atrapamiento cinético de defectos. El otro conjunto se creó mediante un protocolo de recocido controlado por temperatura: las fibrillas se crecieron con una fuerza impulsora efectiva muy baja, cercana a su límite de solubilidad, donde las estructuras incorrectas pueden disolverse o repararse antes de quedar fijadas. La criomicroscopía electrónica de alta resolución mostró que ambos conjuntos de fibrillas eran esencialmente idénticos en forma y torsión global, lo que indica que el recocido no cambió la morfología básica. 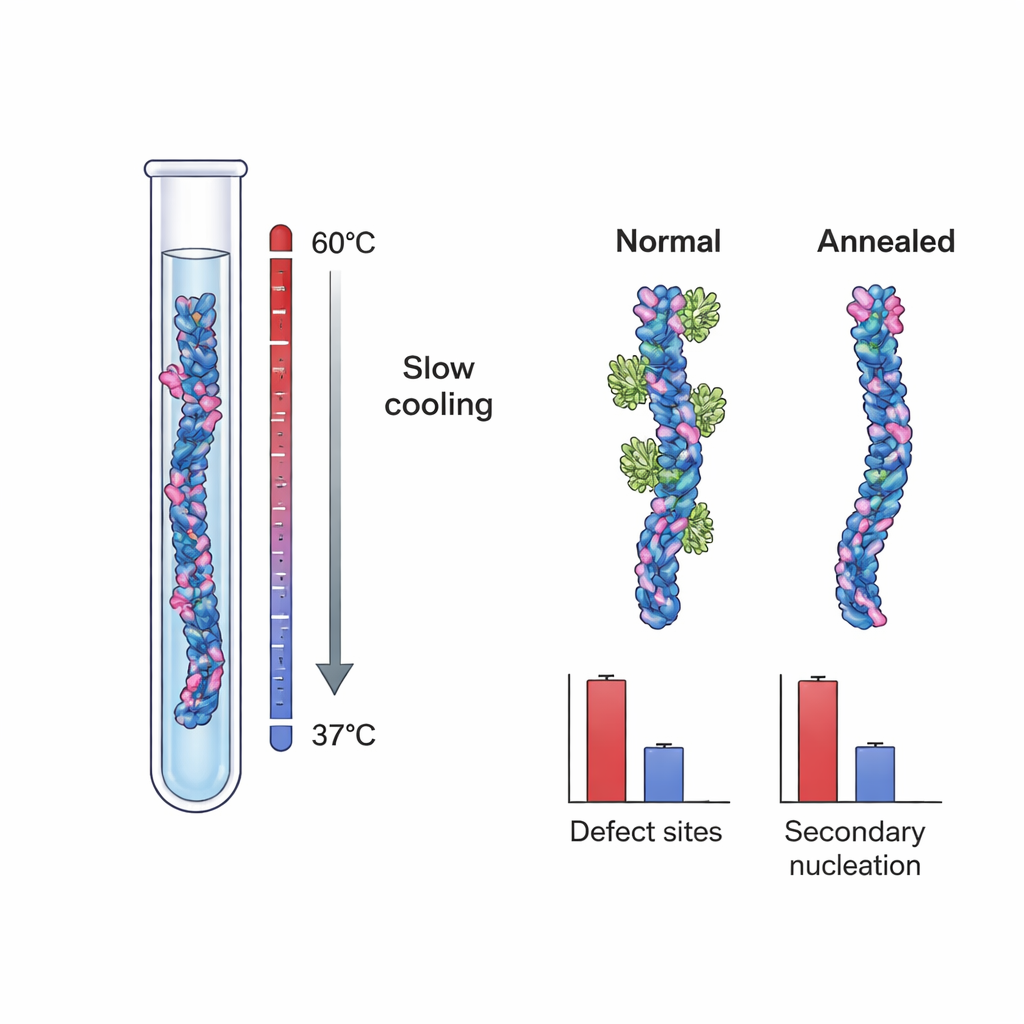
Menos fallas, menos sitios peligrosos de crecimiento
Cuando el equipo midió la unión de Brichos a estos dos tipos de fibrillas, descubrieron una diferencia notable. Las fibrillas control de Aβ40 tenían aproximadamente un sitio de unión a Brichos por ~100 monómeros, lo que de nuevo indica sitios raros pero importantes. Sin embargo, las fibrillas recocidas tenían solo alrededor de un sitio por ~800 monómeros —una reducción de casi el 90% en la frecuencia de sitios. En pruebas separadas donde estas fibrillas se añadieron como “semillas” a soluciones frescas de Aβ40, las fibrillas recocidas fueron mucho menos eficaces para desencadenar nueva agregación, incluso cuando su masa total coincidía con la de las fibrillas control. Un modelado cinético detallado mostró que esta caída en el poder de siembra no podía explicarse simplemente por diferencias en la longitud de las fibrillas. En cambio, se correspondía cuantitativamente con el menor número de sitios de unión a Brichos, apoyando con fuerza la idea de que los defectos de crecimiento actúan como los principales motores de la nucleación secundaria.
Un principio general con promesa terapéutica
Combinando argumentos termodinámicos, un reanálisis de trabajos previos y comparaciones entre varias proteínas formadoras de amiloide, los autores sostienen que los defectos de crecimiento raros probablemente sean centrales en la nucleación secundaria en muchos sistemas, no solo en el Aβ relacionado con el Alzheimer. Estos defectos exponen parcialmente el núcleo interno fuertemente empaquetado de la fibrilla, ofreciendo un andamiaje listo donde nuevos oligómeros y fibrillas pueden formarse con mucha más facilidad que en una superficie lisa. Reconocer estos defectos como los culpables clave abre nuevas vías para el diseño de fármacos. En lugar de intentar bloquear todas las interacciones posibles en la superficie de una fibrilla, las terapias podrían apuntar a proteger o reparar solo estos escasos sitios defectuosos, o a reducir las condiciones que los generan en primer lugar. En términos prácticos, eso podría significar disminuir la concentración efectiva de proteínas formadoras de amiloide en el cerebro o diseñar moléculas, inspiradas en Brichos, que reconozcan y neutralicen los puntos calientes de nucleación impulsados por defectos. Si tienen éxito, tales estrategias podrían cortar la fuente principal de oligómeros tóxicos y ralentizar la progresión de las enfermedades vinculadas al amiloide.
Cita: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Palabras clave: fibrillas amiloides, enfermedad de Alzheimer, nucleación secundaria, agregación proteica, chaperona Brichos