Clear Sky Science · es
El agotamiento de oxígeno en condensados biomoleculares está dominado por la densidad macromolecular
Bolsillos invisibles dentro de las células vivas
Dentro de nuestras células, muchas reacciones químicas dependen de un suministro constante de oxígeno. Pero las células no son bolsas simples de líquido: contienen compartimentos diminutos con aspecto de gotas, llamados condensados biomoleculares, que se forman sin membranas. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones: ¿estos recipientes cambian la disponibilidad de oxígeno en distintas partes de la célula, y si es así, por qué? La respuesta desafía las ideas predominantes sobre el comportamiento de las moléculas pequeñas en estos microambientes congestionados.

Gotas sin paredes
Los condensados biomoleculares son agregados blandos y de tipo líquido de proteínas y ácidos nucleicos que se ensamblan y disuelven según se necesite. Ayudan a organizar la bioquímica concentrando algunas moléculas y excluyendo a otras, a pesar de carecer de una membrana envolvente. Trabajos previos mostraron que muchos metabolitos pequeños y compuestos con carácter farmacológico se acumulan en estas gotas, normalmente porque el interior se comporta algo como un disolvente oleoso en comparación con el fluido acuoso celular. El oxígeno, sin embargo, es un caso especial: es una molécula gaseosa pequeña que impulsa la respiración pero también provoca reacciones secundarias dañinas. Que los condensados enriquezcan o agoten el oxígeno podría, por tanto, influir en la eficiencia de las enzimas y en la cantidad de daño oxidativo que ocurre cerca o dentro de estas gotas.
Midiendo oxígeno en compartimentos diminutos
Para sondear los niveles de oxígeno dentro de los condensados, los investigadores construyeron un sistema modelo sencillo pero ajustable usando proteínas artificialmente diseñadas y flexibles que forman gotas con facilidad en solución salina. Primero crearon fases macroscópicas grandes haciendo girar las muestras en una centrifugadora y luego insertaron microelectrodos electroquímicos finísimos para leer directamente las concentraciones de oxígeno a través del límite entre las capas ricas y pobres en proteína. Estas mediciones revelaron que los niveles de oxígeno bajan cuando la sonda entra en la fase densa en proteínas: las gotas excluyen parcialmente el oxígeno en lugar de absorberlo.
Iluminar el oxígeno con tintes especiales
Puesto que los electrodos alteran las gotas pequeñas, el equipo recurrió a la microscopía de imagen por tiempo de vida de fosforescencia, un método óptico que usa moléculas tintadas especiales cuya emisión dura menos tiempo cuando hay más oxígeno presente. Al seguir el tiempo de la emisión dentro y fuera de gotas individuales, y corrigiendo cuidadosamente cómo el entorno del condensado altera el comportamiento basal del tinte, pudieron inferir las concentraciones de oxígeno sin perturbar físicamente los condensados. En una gama de condiciones, los datos ópticos coincidieron con las mediciones de los electrodos: el oxígeno es consistentemente menor dentro de los condensados que en la solución circundante. Simulaciones por ordenador usando un modelo molecular simplificado respaldaron este panorama, mostrando que el oxígeno pasa relativamente poco tiempo dentro de las regiones densas en proteínas.
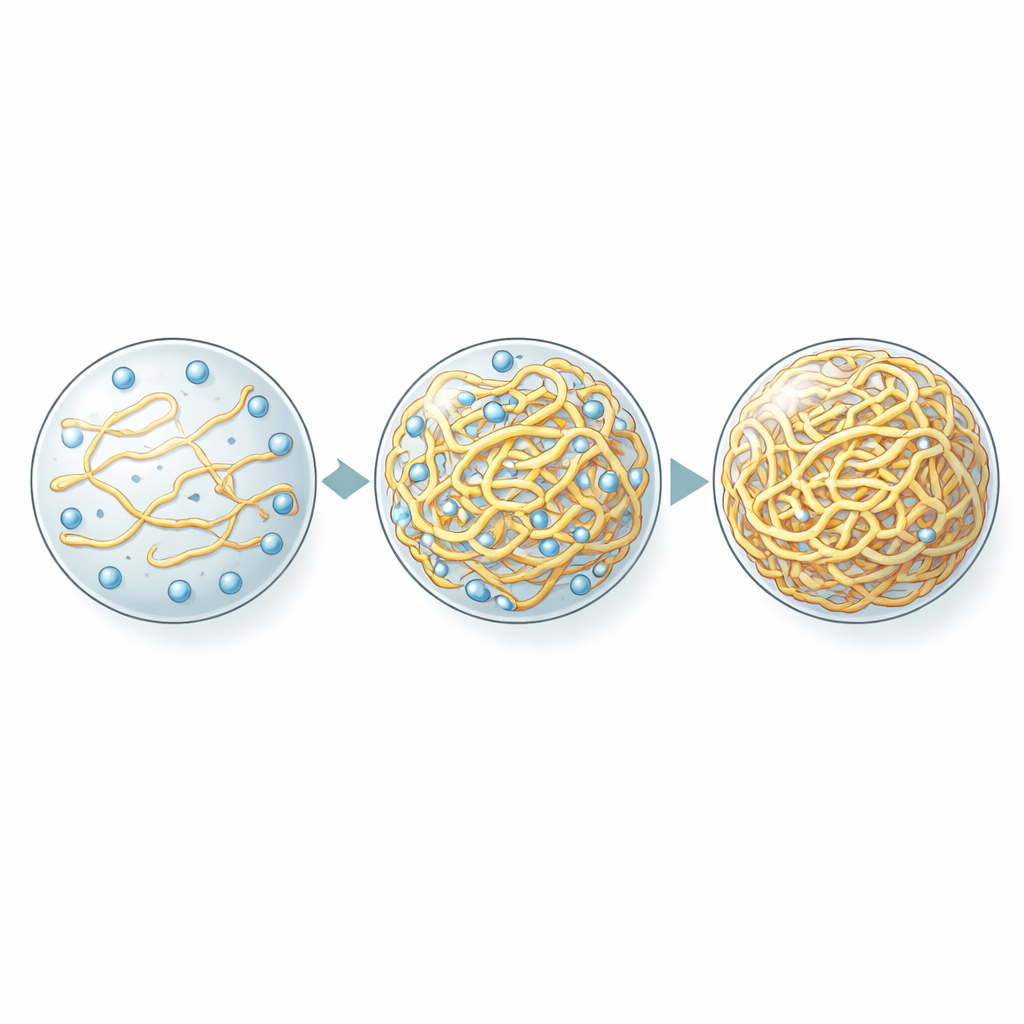
La densidad, no la untuosidad, determina los niveles de oxígeno
El sospechoso obvio para controlar la captación de oxígeno es la hidrofilicidad/hidrofobicidad—la “untuosidad” del interior de la gota—que previamente se había identificado como el factor clave para cómo muchas otras moléculas pequeñas se distribuyen en los condensados. Para poner esto a prueba, los autores alteraron sistemáticamente las secuencias proteicas para cambiar tanto el número de unidades repetidas como su carácter hidrofóbico, y luego midieron el oxígeno dentro de las gotas resultantes. Sorprendentemente, los niveles de oxígeno no siguieron la pista de lo oleoso o acuoso que fueran las gotas. En cambio, se correlacionaron de forma fuerte e inversa con la cantidad de proteína empaquetada en la fase densa. Las variantes que formaban condensados más congestionados retenían menos oxígeno, incluso cuando eran en conjunto menos hidrofóbicas. Otros tintes pequeños y oleosos se comportaron de forma distinta: seguían prefiriendo las gotas más hidrofóbicas, confirmando que el oxígeno rompía las reglas habituales.
Nueva visión de gradientes de oxígeno a nanoescala
Estos hallazgos conducen a una visión revisada de cómo los condensados moldean su entorno químico. Para las moléculas pequeñas que no se adhieren fuertemente a las proteínas andamiaje, la simple densidad de macromoléculas se convierte en el factor dominante: cuanto más volumen ocupan las proteínas, menos espacio queda para el oxígeno disuelto. Esto significa que las células pueden generar gradientes de oxígeno a distancias de nanómetros a micrómetros simplemente formando o disolviendo condensados, o cambiando cuán compactas son estas gotas. En términos prácticos, el trabajo sugiere que los orgánulos sin membrana pueden ajustar sutilmente la disponibilidad de oxígeno para reacciones cercanas—potencialmente acelerando algunas, enlenteciendo otras o protegiendo componentes sensibles—mediante un efecto físico de hacinamiento más que por unión química específica.
Cita: Garg, A., Brasnett, C., Marrink, S.J. et al. Oxygen depletion in biomolecular condensates is dominated by macromolecular density. Nat Commun 17, 2603 (2026). https://doi.org/10.1038/s41467-026-69376-2
Palabras clave: condensados biomoleculares, partición de oxígeno, acolchonamiento macromolecular, separación de fases, microambientes celulares