Clear Sky Science · es
Órdenes competitivos de enlaces de hidrógeno impulsan la anomalía de la tensión superficial del agua
Por qué la superficie del agua es más extraña de lo que parece
La superficie del agua permite que los insectos caminen sobre estanques, da forma a las gotas de lluvia y controla cómo se forman y estallan las burbujas. Sin embargo, cuando los científicos miden cuán “tensa” está esa superficie —la tensión superficial—, descubren que el agua se comporta de manera sorprendentemente extraña al enfriarse, especialmente cuando se la somete a temperaturas por debajo de su punto de congelación normal. Este artículo utiliza simulaciones computacionales avanzadas para revelar cómo la organización oculta de las moléculas de agua en la superficie explica este enigma de larga data.
Dos tipos ocultos de agua líquida
Aunque percibimos el agua como un líquido simple y uniforme, sus moléculas pueden disponerse localmente de dos maneras contrastantes. Una disposición es más densa y desordenada; los autores la denominan estado ρ. La otra es más abierta y simétrica, con cada molécula rodeada en un patrón aproximadamente tetraédrico de cuatro vecinos; a esto lo llaman estado S. Trabajos previos sugerían que el equilibrio entre estos dos patrones locales ayuda a explicar muchas de las propiedades extrañas del agua en volumen. Aquí, los autores se preguntan cómo se manifiesta esa misma visión de dos estados en la interfaz aire–agua, donde nace la tensión superficial.
Cómo la superficie alinea las moléculas
En la frontera entre aire y agua, las moléculas ya no sienten tirones iguales en todas las direcciones. Esa simetría rota favorece a las moléculas del estado ρ, cuyos átomos de hidrógeno y dipolos moleculares pueden inclinarse con facilidad en una dirección preferente. Las simulaciones muestran que cerca de la temperatura ambiente y algo por debajo, la capa más superficial del agua se llena de estas moléculas ρ alineadas, mientras que las moléculas en estado S son más comunes ligeramente bajo la superficie y en el volumen. Debido a que las moléculas en estado ρ se alinean fuertemente, crean un desequilibrio de fuerzas —una anisotropía de tensiones— que genera una tensión superficial relativamente grande en comparación con líquidos ordinarios como el benceno.
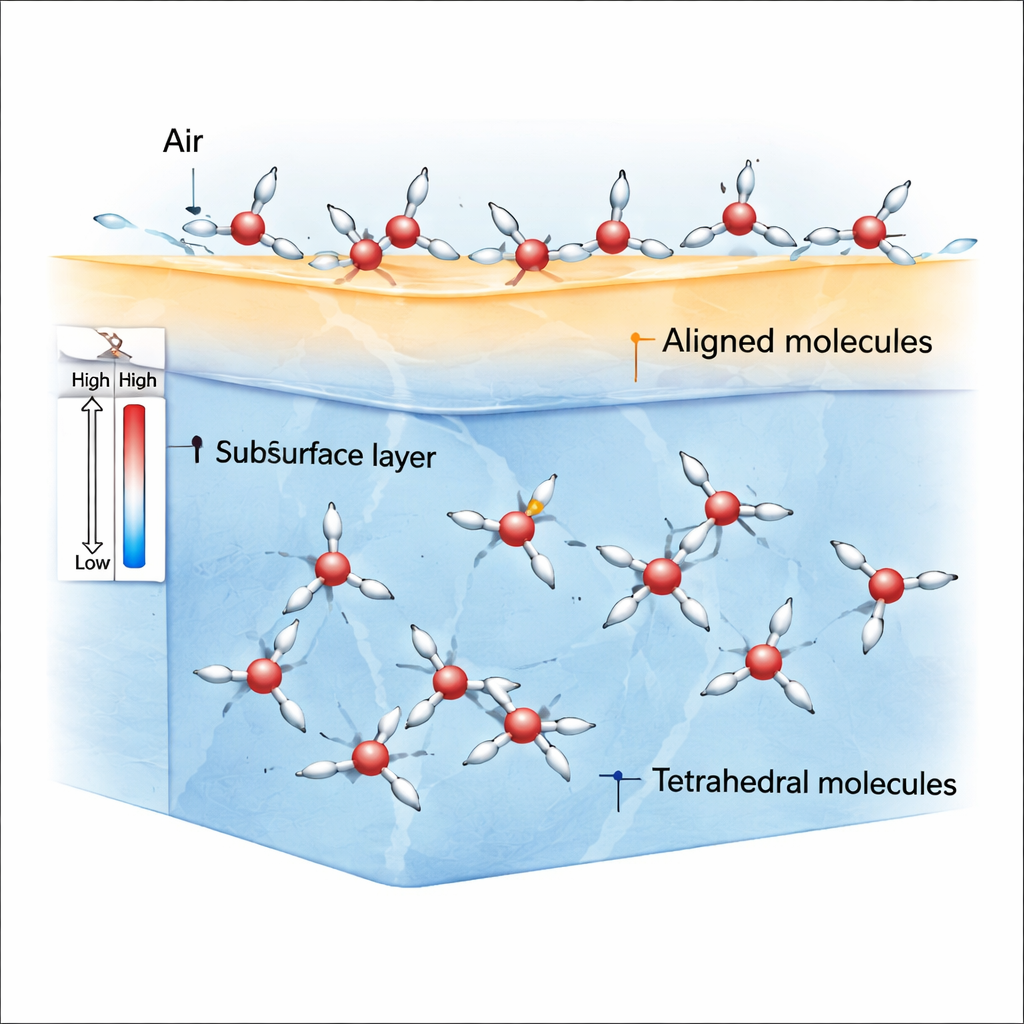
Por qué al enfriarse primero se ralentiza y luego se acelera el tensado superficial
En la mayoría de los líquidos simples, el enfriamiento aprieta la superficie de forma monotónica, haciendo que la tensión superficial aumente casi linealmente. El agua hace esto solo a temperaturas más altas. Al enfriarse hacia aproximadamente −0,15 °C (275 K), el aumento de la tensión superficial empieza a desacelerarse. Las simulaciones muestran que esta desaceleración se debe a que las moléculas en estado ρ de la superficie ya se han alineado tanto como pueden; un enfriamiento adicional apenas cambia su contribución. Al mismo tiempo, las moléculas en estado S en la subsuperficie permanecen mayoritariamente orientadas al azar, por lo que contribuyen poco al aumento de la tensión. El resultado neto es una suerte de meseta: la temperatura sigue bajando, pero la tensión superficial crece solo con lentitud.
El sobreenfriamiento profundo desencadena un segundo apriete
Cuando el agua se enfría mucho más, muy por debajo de su punto de congelación normal, entrando en el régimen de sobreenfriamiento profundo (alrededor de 250 K y menos), su comportamiento cambia de nuevo. La fracción de estructuras tetraédricas del estado S aumenta bruscamente, incluso cerca de la superficie. Crucialmente, estas moléculas en estado S dejan de apuntar en direcciones aleatorias. Sus dipolos comienzan a alinearse a lo largo de la dirección perpendicular a la superficie, impulsados por las interacciones entre dipolos moleculares vecinos y por una región de presión negativa justo bajo la superficie. Cuando eso ocurre, el agua en estado S, que antes ablandaba la tensión superficial, comienza a reforzarla. Esta contribución ordenada adicional produce un nuevo y más rápido aumento —el incremento “reentrante”— en la tensión superficial a bajas temperaturas.
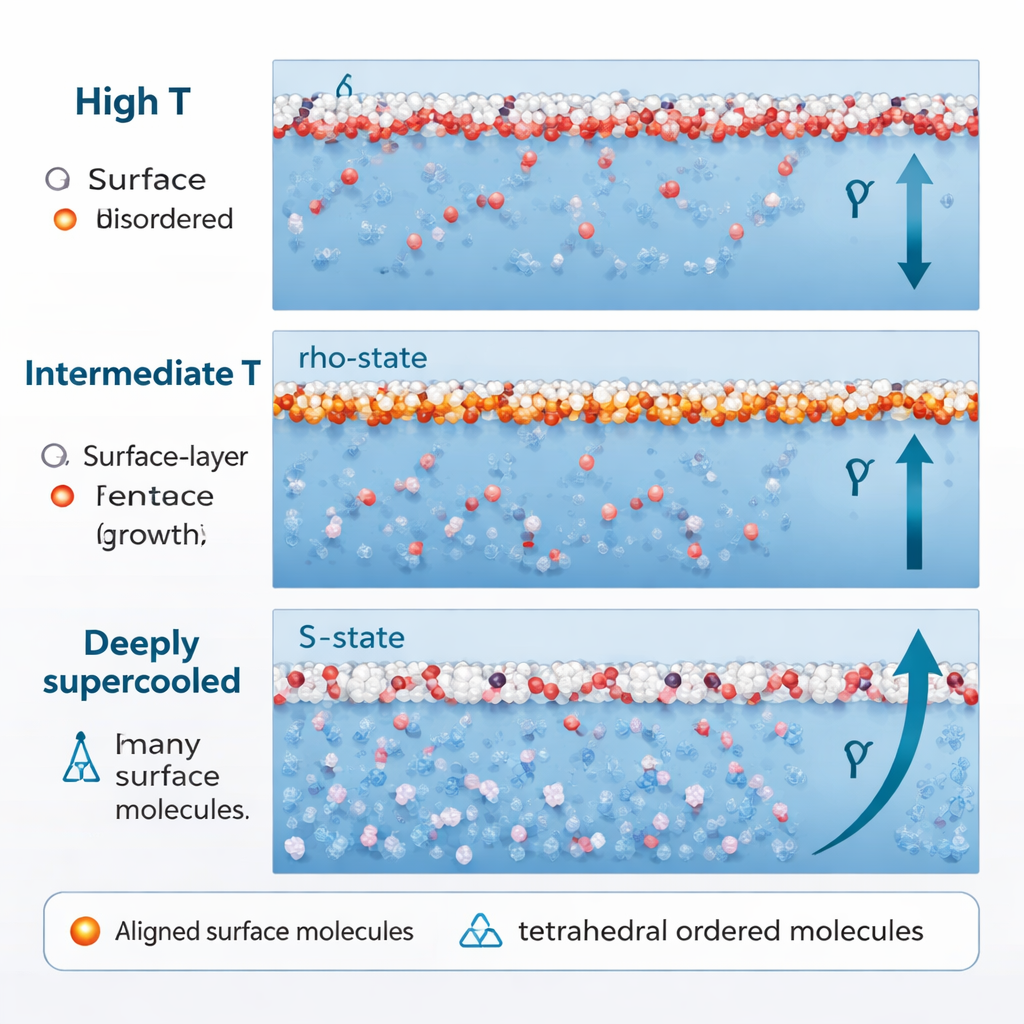
De los rompecabezas superficiales al hielo y más allá
Los mismos cúmulos tetraédricos en estado S que rigidizan la superficie a bajas temperaturas también se parecen a los bloques constructores iniciales de ciertas formas de hielo, y las simulaciones muestran que están enriquecidos cerca de la interfaz. Eso implica que la frontera aire–agua puede actuar como una cuna para la formación del hielo, lo que ayuda a explicar por qué la congelación a menudo comienza en las superficies. En términos más generales, el trabajo ofrece un vínculo concreto a nivel molecular entre cómo las moléculas de agua se organizan y orientan y con qué fuerza la superficie tira hacia adentro. Esta imagen estructural-mecánica no solo resuelve la extraña curva de temperatura de la tensión superficial del agua, sino que también ofrece una hoja de ruta para entender y controlar fenómenos interfaciales en otros líquidos formadores de red, desde el agua sobreenfriada en las nubes hasta materiales usados en tecnología y biología.
Cita: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Palabras clave: tensión superficial del agua, enlaces de hidrógeno, agua sobreenfriada, estructura líquida, nucleación del hielo