Clear Sky Science · es
STING coopera con TOX suprimiendo la expresión de HO-1 para desencadenar ferroptosis en las células CD8+ infiltrantes de tumores y la resistencia a la inmunoterapia
Por qué esta investigación importa para el tratamiento del cáncer
Las inmunoterapias modernas contra el cáncer actúan liberando a las propias células T asesinas del organismo, pero muchos tumores aún encuentran formas de inhabilitar estas células. Este estudio revela un interruptor de autodestrucción oculto dentro de las células T CD8+ que los tumores explotan, y muestra cómo apagar ese interruptor puede hacer que la inmunoterapia sea mucho más eficaz.
Una vía de muerte oculta dentro de las células T que combaten tumores
Dentro de un tumor, las células T CD8+ deberían buscar y destruir células cancerosas. En cambio, con frecuencia escasean, funcionan con lentitud y son de corta duración. Los autores se centraron en dos moléculas dentro de las células T—STING, un sensor de daño en el ADN, y TOX, una proteína asociada con el agotamiento de las células T. Diseñaron ratones cuyas células T CD8+ carecían de STING, de TOX o de ambas, y luego implantaron varios tipos de tumores. Sorprendentemente, los ratones cuyas células T carecían de STING o de TOX eliminaron los tumores con mucha más eficacia. Sus tumores crecieron más despacio, contenían muchas más células T CD8+ y esas células producían mayores cantidades de moléculas citotóxicas como interferón-gamma y granzima B. Esto apuntó a un programa interno que saboteaba silenciosamente a las células T dentro de los tumores.
Cómo la muerte celular impulsada por el hierro debilita la inmunidad
Al examinar la actividad génica en las células T infiltrantes del tumor, los investigadores hallaron que las células T normales dentro de los tumores estaban predispuestas a una forma particular de muerte celular llamada ferroptosis. A diferencia de la apoptosis, la ferroptosis se desencadena por sobrecarga de hierro y la acumulación de lípidos dañados en las membranas celulares. En las células T CD8+ ordinarias expuestas a células tumorales, se activaron genes que promueven la acumulación de hierro y el daño lipídico, mientras que los genes protectores se apagaron. En contraste, las células T deficientes en STING o TOX mostraron el patrón opuesto: expresaron más de las enzimas protectoras HO-1 y GPX4, tenían niveles de hierro más bajos, menos peroxidación lipídica, mitocondrias más sanas y resistieron la muerte por ferroptosis. Pruebas de laboratorio confirmaron que bloquear químicamente la ferroptosis mantenía vivas a las células T normales, mientras que eliminar STING o TOX las hacía naturalmente resistentes.
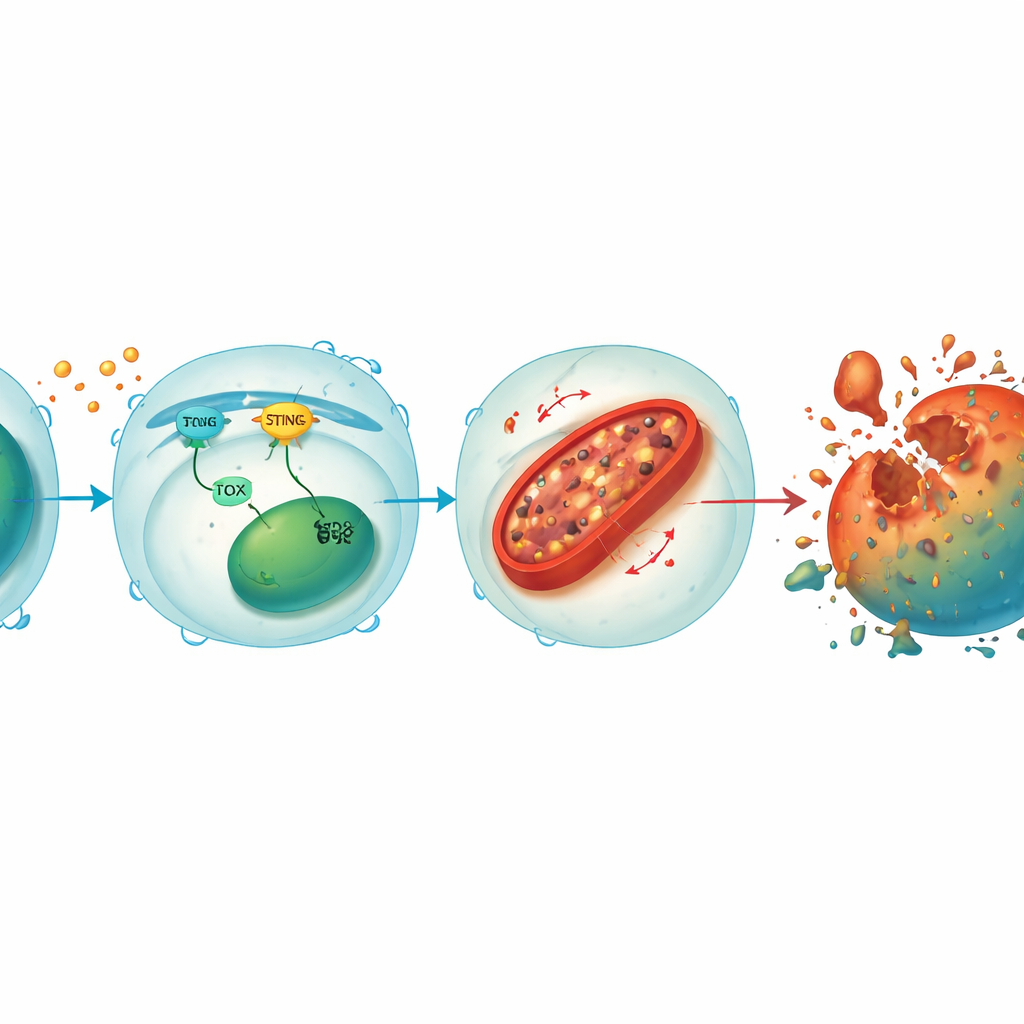
Un circuito que vincula señales de estrés con daño mitocondrial
Profundizando, el equipo descubrió que STING y TOX forman un bucle reforzador dentro de las células T CD8+. Cuando señales tumorales o virales activan STING, se desencadenan factores descendentes que aumentan TOX, y TOX a su vez contribuye a mantener la actividad de STING. Juntos, suprimen HO-1, una enzima que normalmente ayuda a controlar el hierro celular. Con HO-1 reprimida, el hierro se acumula en las mitocondrias—las centrales energéticas de la célula—lo que conduce a elevados niveles de especies reactivas de oxígeno y a la oxidación de los lípidos de las membranas. Este daño mitocondrial agota la producción de energía y, en última instancia, empuja a la célula T hacia la ferroptosis. Restaurar STING o TOX en células T knockout reestableció la sobrecarga de hierro y la muerte celular, mientras que reducir aún más HO-1 volvió vulnerables incluso a las células protegidas, subrayando a HO-1 como un freno central de esta ruta destructiva.
Cómo el lactato producido por el tumor aprieta el gatillo
El microambiente tumoral es rico en lactato, un subproducto del metabolismo alterado del cáncer. El estudio muestra que este lactato no es solo un residuo metabólico: ayuda activamente a activar el interruptor de la ferroptosis en las células T. En comparación con otras células, las células T CD8+ fueron especialmente sensibles al lactato. A medida que el lactato entraba en las células a través de transportadores específicos, provocaba acumulación de hierro, reducción del tamaño mitocondrial, pérdida de ADN mitocondrial y más daño oxidativo. Al mismo tiempo, el lactato aumentó la actividad de STING y TOX y suprimiÓ aún más a HO-1. Las células T que carecían de STING o TOX fueron mucho más resistentes al daño inducido por lactato. Bloquear un transportador clave de lactato con un fármaco (AZD3965) protegió a las células T CD8+ de la ferroptosis en ratones, aumentó su presencia dentro de los tumores y ralentizó el crecimiento tumoral, imitando el beneficio de eliminar genéticamente STING en las células T.
Convertir una vulnerabilidad en una ventaja terapéutica
Estos hallazgos mecanísticos tienen implicaciones prácticas. Cuando los investigadores usaron terapia celular adoptiva—infundiendo en ratones células T activadas en laboratorio—encontraron que las células T diseñadas para carecer de STING o TOX controlaban el tumor con mucha más eficacia que las células T normales. Además, combinar estas células T “resistentes a la ferroptosis” con tratamientos existentes como inhibidores de puntos de control PD-1 o TIM-3, quimioterapia con cisplatino o un fármaco activador de STING produjo una reducción tumoral notablemente mayor que cualquiera de las terapias por separado. Finalmente, en muestras tumorales de pacientes con cáncer de cuello uterino, niveles más altos de TOX y más bajos de HO-1 en los linfocitos infiltrantes se asociaron con peor supervivencia, lo que sugiere que esta vía también condiciona los resultados clínicos en humanos.
Qué significa esto para la atención oncológica futura
En términos sencillos, el estudio revela que los tumores pueden forzar a nuestras mejores células T anticáncer a oxidarse desde dentro al impulsar una forma de muerte celular alimentada por hierro. Un circuito lactato–STING–TOX reduce la protección que ofrece HO-1, daña las mitocondrias y conduce a la ferroptosis, disminuyendo las filas de células T CD8+ efectivas. Interrumpir este circuito—mediante el diseño de células T que carezcan de STING o TOX, potenciando HO-1 o bloqueando la entrada de lactato—mantiene a las células T vivas, enérgicas y listas para atacar. Este trabajo apunta hacia inmunoterapias de nueva generación que combinen ajustes metabólicos y genéticos de las células T con fármacos existentes para superar la resistencia y ofrecer un control tumoral más duradero.
Cita: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Palabras clave: inmunoterapia contra el cáncer, células T CD8, ferroptosis, microambiente tumoral, vía STING TOX HO-1