Clear Sky Science · es
Seq-Scope-eXpanded: ómicas espaciales más allá de la resolución óptica
Ver las células con mayor nitidez
Nuestros cuerpos están constituidos por innumerables células diminutas, cada una llena de actividad que normalmente no podemos ver, ni siquiera con microscopios potentes. Este artículo presenta Seq-Scope-X, una tecnología que permite a los investigadores acercarse a los mecanismos internos de los tejidos con una claridad sin precedentes, cartografiando qué genes y proteínas están activos en puntos precisos dentro y entre células. Ese nivel de detalle podría cambiar la forma en que estudiamos el desarrollo, el sistema inmunitario y enfermedades como el cáncer o las lesiones hepáticas.
¿Por qué mapear las moléculas en su lugar?
Las células no funcionan de forma aislada: viven en vecindarios, forman capas y se especializan según su ubicación. Los métodos tradicionales de secuenciación rompen los tejidos, perdiendo este contexto espacial. Las herramientas más recientes de “ómicas espaciales” mantienen las moléculas en su lugar, pero ha habido una compensación. Los métodos basados en imagen pueden ver detalles muy finos pero, por lo general, detectan solo un conjunto limitado de genes. Los métodos basados en secuenciación pueden leer casi todos los genes a la vez, pero difuminan las características finas, a menudo extendiendo las señales varios micrómetros —mayor que muchas estructuras subcelulares. Los autores se propusieron cerrar esta brecha: conservar la lectura rica e imparcial de la secuenciación, alcanzando o incluso superando la nitidez de los microscopios modernos.
Estirar el tejido para superar los límites ópticos
La idea central de Seq-Scope-X es engañosamente simple: aumentar suavemente el tamaño del propio tejido para que cada nanómetro original de estructura se haga más fácil de resolver. El equipo ancla primero las moléculas de ARN —o etiquetas de ADN especiales unidas a anticuerpos— en un hidrogel blando que se forma alrededor del corte de tejido. Luego digieren el tejido original y hacen hinchar el gel en una solución salina, estirando físicamente todo aproximadamente tres veces mientras mantienen casi intactas las posiciones relativas. Este gel expandido se coloca sobre un chip de secuenciación ultradenso recubierto con sondas de captura. Al calentar cuidadosamente el conjunto, las moléculas ancladas se liberan del gel y se vuelven a unir al chip, que luego puede secuenciarse para revelar qué genes o proteínas estaban presentes en cada minúscula coordenada. 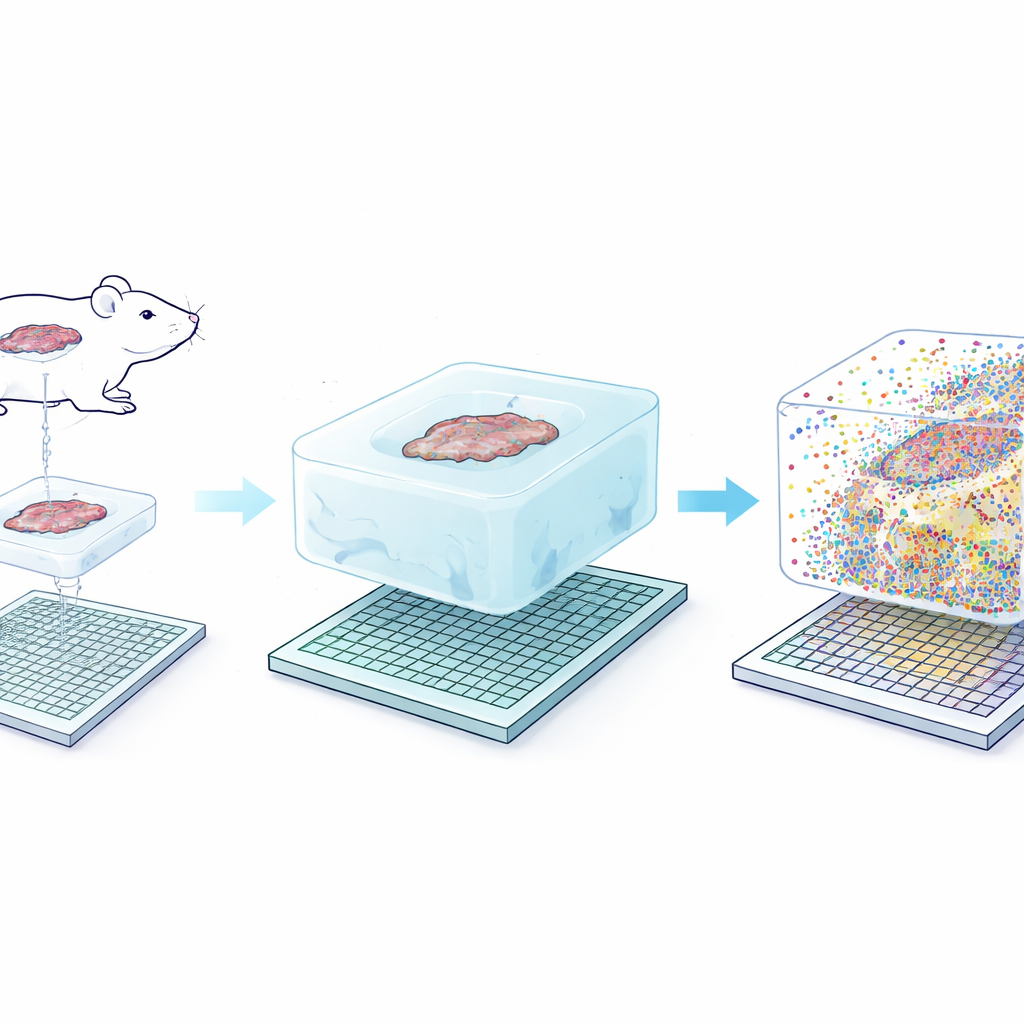
De células borrosas a mapas subcelulares
Cuando los investigadores aplicaron Seq-Scope-X al hígado de ratón, encontraron que el método mejoró la resolución espacial de aproximadamente 0,6 micrómetros a cerca de 0,2 micrómetros e incrementó el número de posiciones medibles por milímetro cuadrado casi diez veces. En términos prácticos, lo que antes parecía manchas difusas de señal se resolvió ahora en contornos nítidos de células individuales. Aún más llamativo, los cúmulos de ARN que no habían sido procesados por completo (no empalmados) se alinearon estrechamente con los centros de los núcleos, mientras que el ARN maduro (empalmado) trazaba el citoplasma circundante. Esto permitió a los autores dibujar los límites celulares usando solo ARN y separar las lecturas génicas nucleares y citoplasmáticas para casi cada hepatocito en el tejido, algo que los métodos basados en secuenciación anteriores solo podían sugerir.
Células con personalidades divididas
Con esta nueva claridad, el equipo descubrió una forma inesperada de “doble vida” molecular dentro de las células hepáticas. A lo largo del conocido gradiente desde los vasos sanguíneos en el lado portal del lóbulo hepático hasta los del lado central, los hepatocitos se especializan en diferentes tareas metabólicas. Seq-Scope-X mostró que, en muchas células, el patrón de genes en el núcleo no coincidía con el patrón en el citoplasma circundante. Aproximadamente un tercio de los hepatocitos parecía tener un perfil nuclear alineado con una zona y un perfil citoplasmático alineado con una zona vecina. Métodos independientes basados en imagen, incluidas MERFISH y ensayos de fluorescencia de ARN de molécula única, confirmaron que los transcritos individuales pueden concentrarse ya sea en el núcleo o en el citoplasma. En conjunto, estos hallazgos sugieren que los hepatocitos pueden cambiar dinámicamente sus roles metabólicos con el tiempo, con el núcleo preparando un estado futuro mientras el citoplasma refleja el estado actual. 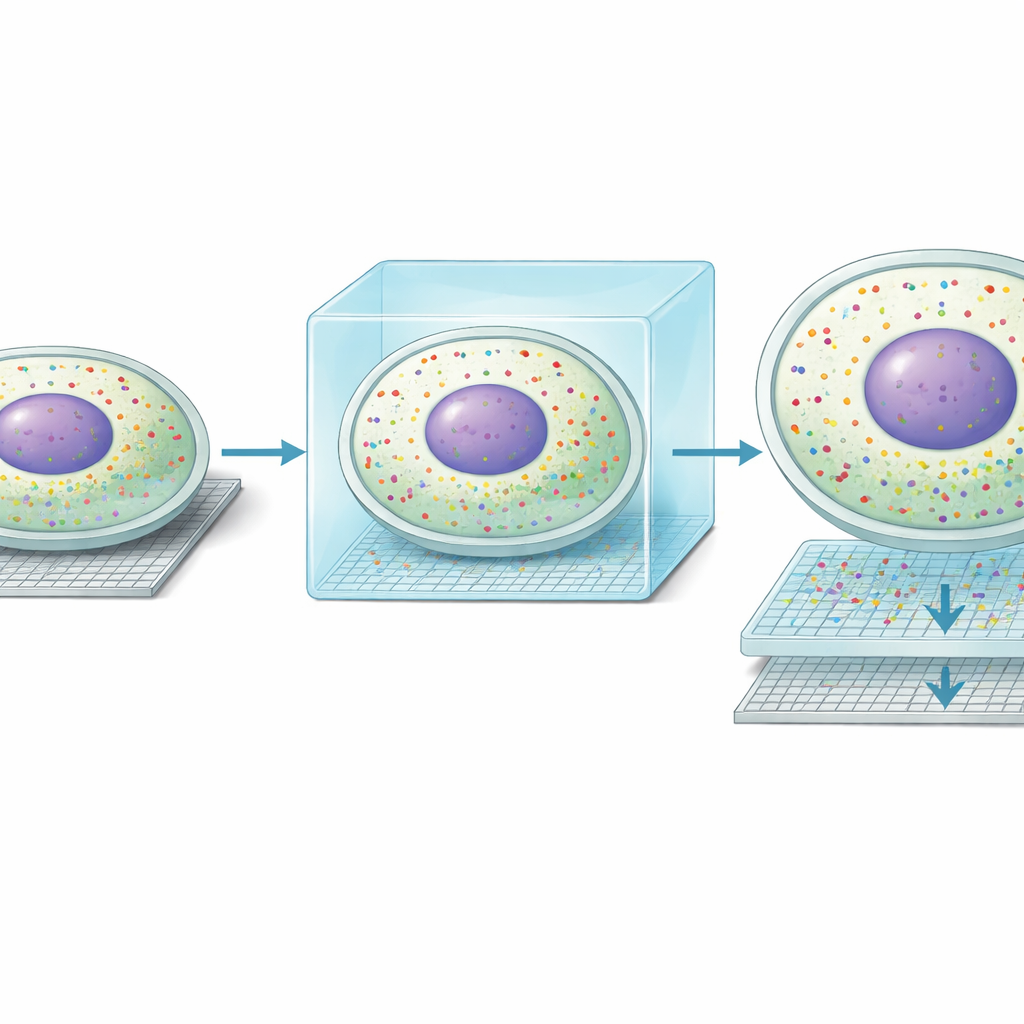
Más allá del hígado: cerebro, intestino y tejidos inmunitarios
Los autores probaron luego si Seq-Scope-X funciona en otros órganos. En el cerebro, separó con claridad distintos tipos de neuronas y células de soporte y reveló patrones subcelulares de ARN alrededor de los núcleos. En el colon, resolvió subtipos distintos de células caliciformes y capas de colonocitos a lo largo del eje de criptas a superficie, capturando de nuevo firmas nucleares. Quizá de forma más llamativa, el equipo adaptó el método a proteínas usando anticuerpos codificados con códigos de barras de ADN en bazo de ratón y amígdala humana. Seq-Scope-X pudo cartografiar simultáneamente más de cien marcadores de superficie celular a resolución de célula única, distinguiendo subconjuntos de células T y B muy juntas y células mieloides. Al cambiar a una química de gel más expandible, llevaron la resolución efectiva hacia la verdadera escala nanométrica, al tiempo que preservaron la arquitectura tisular lo suficiente para un mapeo detallado.
Qué implica esto en el futuro
Seq-Scope-X demuestra que ampliar físicamente los tejidos antes de secuenciarlos puede superar límites de resolución de larga data, ofreciendo un detalle cercano al nivel microscópico mientras sigue leyendo miles de genes o etiquetas proteicas a la vez. Para un observador general, esto significa que los científicos pueden ahora construir “atlas moleculares” que no solo indiquen qué células están dónde, sino que también revelen qué sucede dentro de distintas partes de cada célula. Tales mapas podrían ayudar a explicar cómo los tejidos responden a una lesión, cómo se organizan las células inmunitarias en órganos linfoides y tumores, o cómo cambios sutiles dentro de las células anuncian una enfermedad. Aunque se necesitan más refinamientos para ampliar la cobertura y mejorar algunos paneles de tinción, Seq-Scope-X abre una poderosa nueva ventana a los paisajes microscópicos que subyacen a la salud y la enfermedad.
Cita: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Palabras clave: transcriptómica espacial, expansión de tejidos, ómicas de una sola célula, proteómica espacial, zonación hepática