Clear Sky Science · es
El IPA derivado de la microbiota protege frente a la colitis regulando la cetogénesis mediada por HMGCS2 intestinal para facilitar la reparación de la mucosa
Por qué las bacterias intestinales importan para un intestino dañado
Cuando el revestimiento del intestino está dañado, como ocurre en la enfermedad inflamatoria intestinal (EII) o tras tratamientos médicos agresivos, el organismo debe reparar rápidamente esta “piel” interna para evitar que contenidos nocivos se filtren al torrente sanguíneo. Este estudio revela cómo una única molécula producida por bacterias intestinales beneficiosas puede ayudar al intestino a sanarse, apuntando a nuevas formas de tratar trastornos crónicos del intestino sin suprimir ampliamente el sistema inmunitario.
Una señal útil de microbios amigos
Los investigadores empezaron comparando huellas químicas en muestras de heces de personas con EII y voluntarios sanos, así como en varios modelos murinos de colitis. Entre cientos de moléculas, una destacó: el ácido indol-3-propiónico (IPA), un producto de degradación del aminoácido dietético triptófano generado por ciertas bacterias intestinales. Los niveles de IPA fueron sistemáticamente más bajos en personas con enfermedad de Crohn y en ratones con colitis que en sus homólogos sanos. Esto sugirió que la pérdida de IPA podría formar parte de lo que falla cuando el revestimiento intestinal se inflama y no logra repararse.
Fortaleciendo el muro protector del intestino
Para comprobar si el IPA solo era un marcador de la enfermedad o realmente la protegía, el equipo administró IPA a ratones antes de inducir varios tipos de lesión intestinal, incluida la colitis química y el daño por radiación. Los ratones que recibieron dosis adecuadas de IPA presentaron colon más largo y sano, menos cambios inflamatorios al microscopio y una capa de moco más gruesa con uniones celulares más firmes. Filtraron menos marcadores inflamatorios y tenían más células caliciformes, que producen el recubrimiento mucoso protector. Importante, estos beneficios se observaron incluso en ratones libres de gérmenes que carecen de microbioma residente, lo que demuestra que, una vez presente, el IPA puede actuar directamente sobre el revestimiento intestinal sin necesitar a otras microbios.
Alimentando a las células madre con un tipo especial de energía
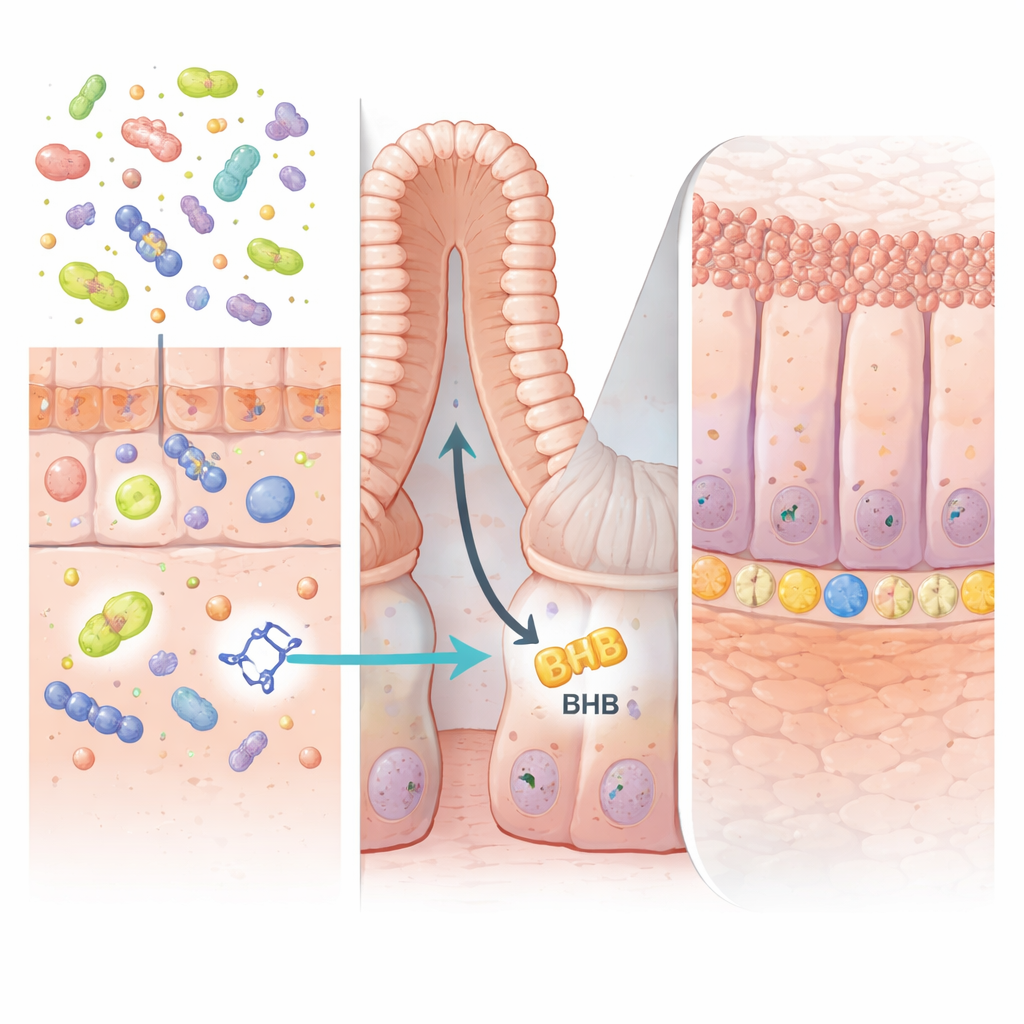
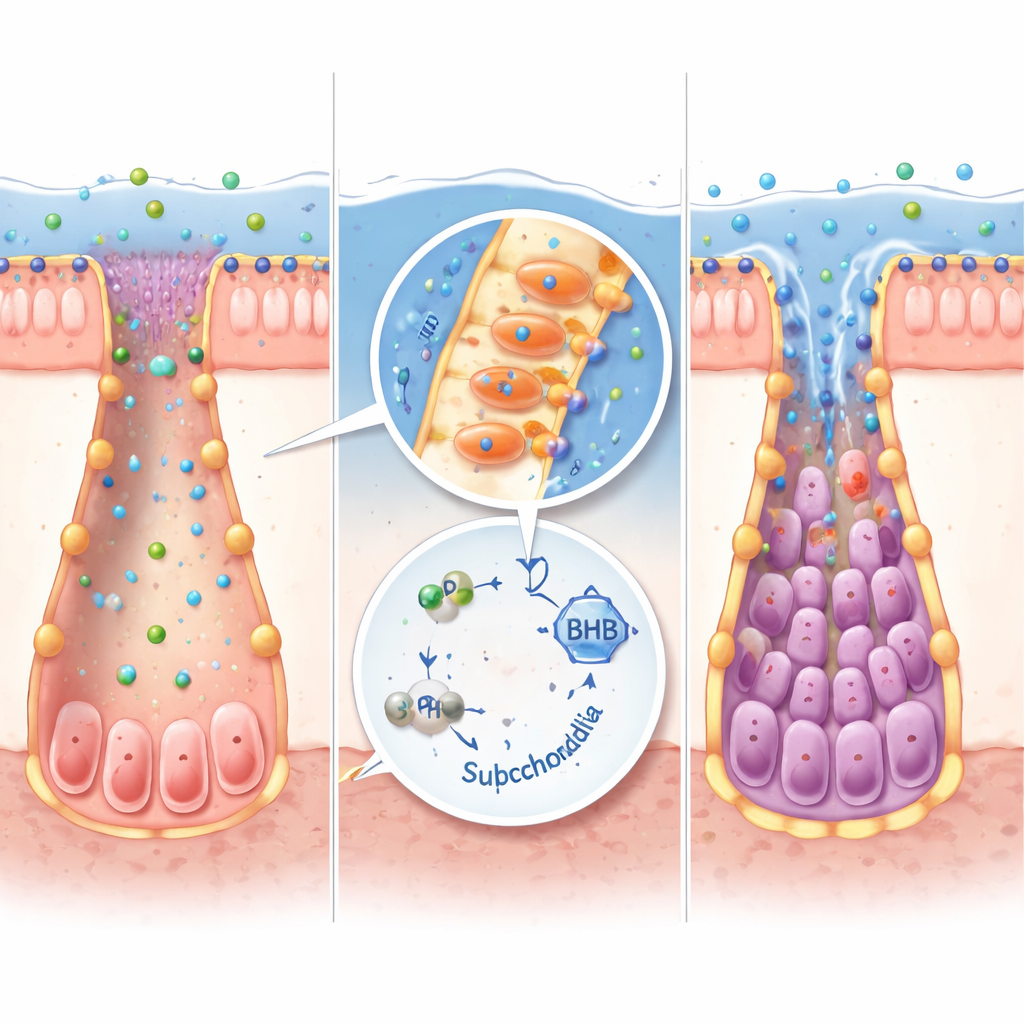
La clave de la acción del IPA residía en lo profundo de las “criptas” intestinales, las pequeñas cavidades donde se asientan las células madre y renuevan constantemente el revestimiento. Los autores mostraron que el IPA activa una proteína llamada PPARα en las células epiteliales intestinales. Esto, a su vez, aumenta la producción de una enzima denominada HMGCS2, que impulsa la cetogénesis —el proceso de producir la molécula energética β‑hidroxibutirato (BHB). El aumento de BHB dentro de la pared intestinal estimuló la expansión de las células madre LGR5 positivas y la regeneración más rápida del tejido dañado. Cuando la enzima HMGCS2 o PPARα se eliminaron selectivamente de las células intestinales en ratones, el IPA ya no pudo aumentar la actividad de las células madre ni proteger frente a la colitis, confirmando que esta vía productora de cetonas es esencial.
De las fábricas bacterianas a los tejidos humanos
No todas las bacterias intestinales pueden producir IPA. Al reanalizar grandes conjuntos de datos del microbioma, los investigadores identificaron a Peptostreptococcus russellii como un productor clave de IPA que está disminuido en varias cohortes de EII. En cultivos de laboratorio, esta bacteria convirtió el triptófano en IPA de manera eficiente. Cuando ratones libres de gérmenes fueron colonizados con P. russellii, sus niveles de IPA aumentaron, se activaron genes productores de cetonas, aumentaron marcadores de células madre y la gravedad de la colitis disminuyó en comparación con ratones que recibieron un trasplante microbiano genérico. La misma vía IPA–cetona funcionó en organoides intestinales en miniatura derivados de tejidos de ratón y humano, donde añadir IPA o BHB ayudó a que las células madre se recuperaran tras el daño inflamatorio mientras reducía las señales proinflamatorias.
Qué podría significar esto para tratamientos futuros
En conjunto, el trabajo describe una cadena de eventos simple pero potente: ciertas bacterias intestinales transforman el triptófano dietético en IPA; el IPA activa un interruptor metabólico en las células intestinales; este interruptor aumenta la producción de BHB; y el BHB, a su vez, reactiva las células madre que reconstruyen el revestimiento intestinal. Para personas con EII u otras condiciones que lesionan la barrera intestinal, las terapias que restauren IPA o imiten de forma segura sus efectos —mediante dieta, probióticos dirigidos o fármacos diseñados— podrían promover una curación verdadera de la mucosa sin supresión inmunitaria generalizada. Aunque se necesitan más estudios en pacientes, este eje microbio–metabolito–célula madre ofrece una nueva y prometedora vía para reparar el intestino desde dentro hacia afuera.
Cita: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Palabras clave: microbioma intestinal, células madre intestinales, enfermedad inflamatoria intestinal, metabolitos microbianos, curación de la mucosa