Clear Sky Science · es
CD38 degrada MAVS mediante mitofagia para inhibir la secreción de interferón de tipo I en células de carcinoma nasofaríngeo y perjudica la inmunidad antitumoral mediada por células T CD8+
Por qué esto importa para el tratamiento del cáncer
El carcinoma nasofaríngeo es un cáncer que se origina detrás de la nariz y es especialmente frecuente en el Este y Sudeste de Asia. Los fármacos basados en el sistema inmune que liberan a las propias células T del organismo han cambiado el pronóstico de algunos pacientes, pero la mayoría sigue sin beneficiarse. Este estudio descubre un freno oculto dentro de las propias células tumorales: una molécula llamada CD38 que apaga silenciosamente un sistema de alarma interno y debilita el ataque de las células T CD8 que matan tumorales. Comprender y desactivar este freno podría hacer que las inmunoterapias existentes funcionen para muchas más personas.
Un interruptor oculto en las células tumorales
Los investigadores se centraron en CD38, una proteína presente en muchas células inmunitarias pero también en células del carcinoma nasofaríngeo. Trabajos anteriores habían vinculado CD38 con la resistencia frente a fármacos de control inmunitario dirigidos a PD-1 y PD-L1. Aquí, el equipo preguntó si CD38 dentro de las propias células tumorales altera directamente la capacidad de las células T CD8 para reconocer y destruir esas células. Al cultivar células tumorales humanas con o sin CD38 junto a células T CD8 humanas activadas, hallaron que eliminar CD38 de las células cancerosas hacía a las células T mucho más potentes: secretaban niveles más altos de moléculas clave de ataque, sobrevivían mejor y mataban más células tumorales. Cuando se reincorporó CD38, la función de las células T descendió, lo que señala a CD38 como un supresor intrínseco tumoral del ataque inmunitario.
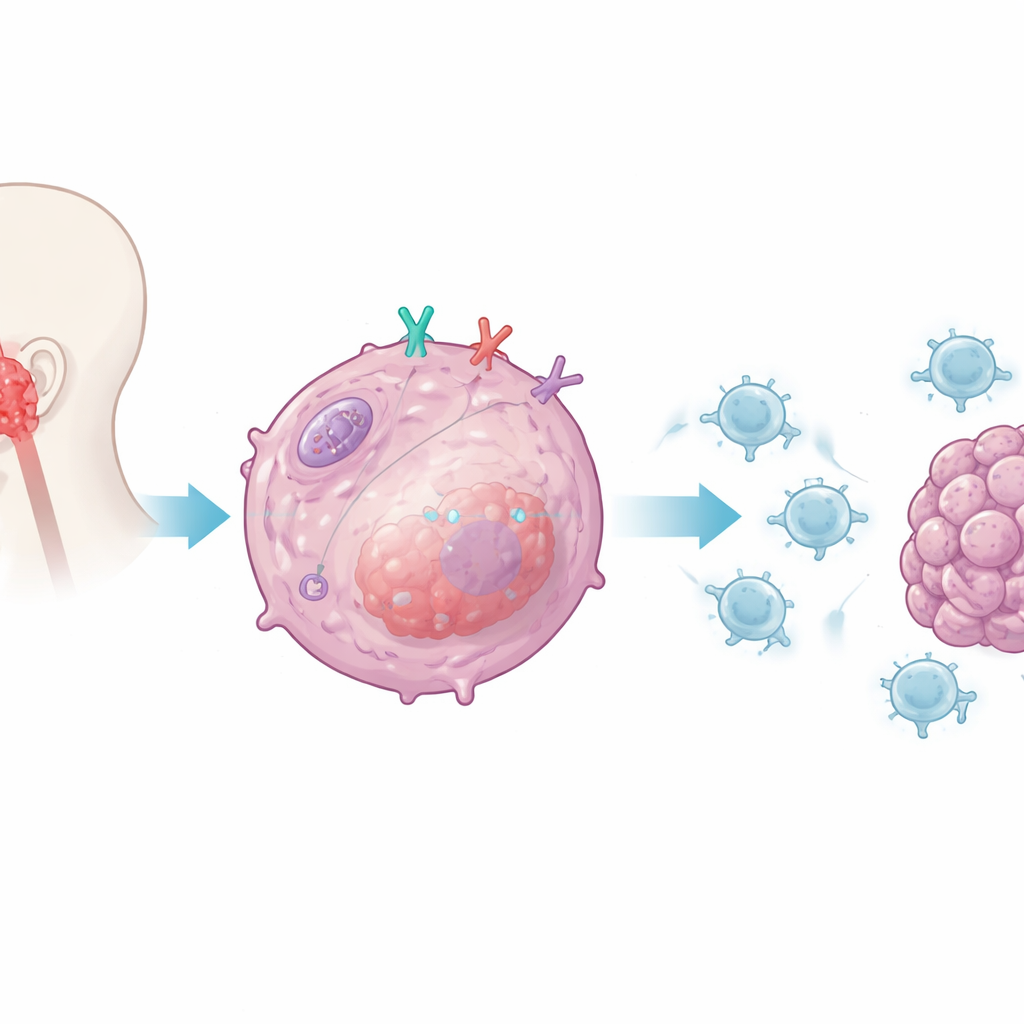
Atenuando la alarma interna de la célula
El equipo investigó entonces cómo CD38 envía esta señal supresora. Se centraron en el sistema de alarma innato de la célula tumoral, que normalmente detecta material genético tipo viral y desencadena interferones de tipo I, mensajeros potentes que estimulan la inmunidad. En las células tumorales carentes de CD38, los investigadores observaron un fuerte aumento de interferón beta y de quimioquinas que atraen células T CD8 hacia los tumores. Demostraron que CD38 atenúa selectivamente la vía controlada por un sensor interno llamado RIG-I y su proteína adaptadora MAVS, que se sitúa en las mitocondrias, las centrales energéticas de la célula. Cuando CD38 estaba presente, la activación de esta vía y de las moléculas de señalización aguas abajo quedaba amortiguada; cuando se eliminó CD38, la señalización y la producción de interferón aumentaron, mejorando la visibilidad del tumor para el sistema inmune.
Cómo CD38 destruye un punto clave de señalización
Indagando más, los científicos encontraron que CD38 se asocia físicamente con MAVS en las mitocondrias e interfiere con la asociación de MAVS con RIG-I, debilitando la transmisión de la señal. Más notable aún, niveles más altos de CD38 llevaron a una reducción de la proteína MAVS sin cambiar su código genético, lo que sugiere una destrucción activa. Ensayos con distintos inhibidores mostraron que esta pérdida dependía de la maquinaria de reciclaje celular conocida como autofagia, y específicamente de una forma que dirige a las mitocondrias. CD38 aumentó marcadores de "autofagia mitocondrial", redujo varias proteínas mitocondriales y promovió el empaquetamiento de MAVS en estructuras autofagocíticas que luego se degradan. Bloquear la autofagia mitocondrial preservó MAVS y restauró la señalización de interferón, indicando que CD38 desactiva la alarma al llevar a MAVS hacia la corriente de desecho celular.
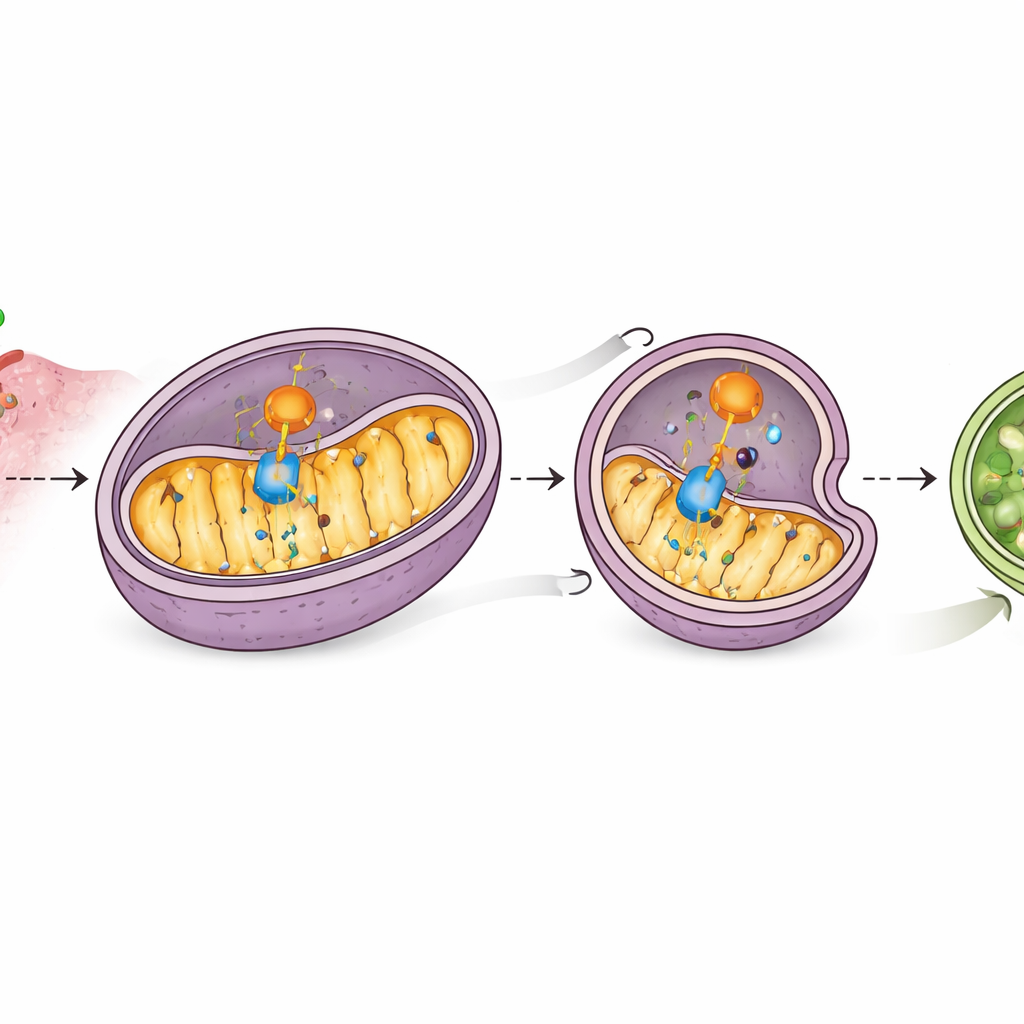
Un ayudante que guía a las mitocondrias hacia la autodestrucción
El estudio identificó a otro actor, PHB2, una proteína dentro de las mitocondrias que actúa como receptor para la eliminación selectiva de mitocondrias. Experimentos de espectrometría de masas y de unión mostraron que CD38 interactúa con PHB2 y aumenta la presencia de PHB2 en las mitocondrias, donde PHB2 a su vez recluta la maquinaria central de la autofagia. PHB2 también se une a MAVS, y CD38 refuerza este contacto. Cuando PHB2 se redujo, CD38 ya no pudo desencadenar eficazmente la autofagia mitocondrial, los niveles de MAVS se recuperaron y se reactivaron genes relacionados con el interferón. Esto revela una cadena de eventos: CD38 recluta a PHB2, PHB2 recluta a MAVS, y juntos conducen a MAVS hacia mitocondrias destinadas a la degradación, silenciando la alarma de interferón.
Pruebas en modelos animales
Para evaluar el impacto en organismos vivos, los investigadores usaron tumores de ratón diseñados para carecer de CD38. En ratones inmunocompetentes, estos tumores crecieron más despacio, contenían más células T CD8 y presentaban una mayor fracción de células que producían interferón-gamma, un sello de respuestas antitumorales activas. Bloquear el receptor de los interferones de tipo I eliminó esta ventaja, confirmando que la señalización de interferón es esencial para la inmunidad mejorada. En ratones humanizados portadores de tumores nasofaríngeos humanos, reducir CD38 también ralentizó el crecimiento y aumentó la infiltración de células T CD8, pero este beneficio desapareció cuando MAVS también se redujo en las células tumorales. Estos hallazgos in vivo afianzan la idea de que el eje CD38–PHB2–MAVS dentro de las células tumorales configura la intensidad de la respuesta de las células T del organismo.
Qué significa esto para terapias futuras
En conjunto, el trabajo muestra que CD38 en las células de carcinoma nasofaríngeo actúa como un saboteador interno de la inmunidad antitumoral. Al promover una forma selectiva de reciclaje mitocondrial, CD38 agota MAVS, debilita la producción de interferón de tipo I, reduce la presentación de antígenos y, en última instancia, atenúa el ataque de las células T CD8. Los compuestos actuales que bloquean CD38 atacan principalmente su actividad enzimática y no eliminan la proteína ni restauran MAVS. Los autores sostienen que nuevas estrategias dirigidas a reducir los niveles de CD38 o a interrumpir su asociación con PHB2 o MAVS podrían reactivar la alarma de interferón dentro de los tumores. Combinadas con los inhibidores de puntos de control existentes, tales aproximaciones podrían convertir más carcinomas nasofaríngeos —y potencialmente otros cánceres— de inmunológicamente fríos a inmuno‑responsivos.
Cita: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Palabras clave: carcinoma nasofaríngeo, inmunoterapia tumoral, interferón de tipo I, células T CD8, mitofagia