Clear Sky Science · es
Evaluación comparativa de la inferencia de la vía de señalización EGF usando fosfoproteómica e interacciones cinasa-sustrato
Por qué importa más allá del laboratorio
Nuestras células están constantemente escuchando y reaccionando a señales del entorno. Una de las más importantes es el factor de crecimiento epidérmico (EGF), que ayuda a controlar cómo las células crecen, se dividen y sobreviven. Cuando este sistema de comunicación falla, puede impulsar cánceres y otras enfermedades. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones: si usamos las potentes tecnologías de medición y los modelos informáticos actuales, ¿cuánto mejor podemos entender realmente la vía de señalización de EGF respecto a lo que muestran los diagramas de los libros de texto?
De líneas rectas a diagramas de cableado de la vida real
Las “vías de señalización” tradicionales suelen representarse como cadenas ordenadas y casi lineales de proteínas que transmiten un mensaje desde la superficie celular al núcleo. Esos mapas se construyeron durante décadas con experimentos lentos y dirigidos que solo podían observar unas pocas proteínas a la vez. Los autores sostienen que eso nos ha dejado con una visión limitada, como la que da solo la luz de una farola: sabemos mucho sobre las pocas proteínas que eran fáciles de estudiar y mucho menos sobre la red más amplia de conexiones que probablemente existe en células reales.
Escuchar miles de interruptores moleculares a la vez
Para ir más allá de esa visión limitada, el equipo empleó fosfoproteómica, una técnica de espectrometría de masas que puede rastrear decenas de miles de diminutas marcas químicas llamadas grupos fosfato en proteínas en un solo experimento. Estas marcas las colocan enzimas llamadas quinasas y actúan como interruptores rápidos de encendido/apagado para la señalización. Los investigadores primero reunieron los mapas más completos hasta la fecha de “quién-puede-fosforilar-a-quién” combinando tres tipos de información: hallazgos curados de la literatura, predicciones de un modelo de inteligencia artificial que lee secuencias de proteínas y amplias pantallas experimentales de preferencias de las quinasas. Esto amplió considerablemente la cobertura de relaciones quinasas–sustrato conocidas o sospechadas, pasando de alrededor del 5 % de los sitios medibles hasta un 70–80 %.
Poner a prueba la señal EGF a través de muchos experimentos
A continuación se centraron en la respuesta a EGF, una vía clásica y protagonista en cánceres de pulmón, mama, piel y cerebro. El grupo combinó tres conjuntos de datos publicados de última generación con tres mediciones nuevas, muy profundas y con resolución temporal en células derivadas del riñón, además de dos estudios de control con distintos estímulos. En conjunto, estos experimentos midieron más de 40.000 sitios de fosforilación por conjunto de datos y siguieron cómo subían o bajaban en los minutos posteriores a la estimulación con EGF. Aunque los patrones generales diferían algo entre tipos celulares y tecnologías, sitios clave de fosforilación en la vía EGF se activaron repetidamente, confirmando que la señal central es robusta incluso a través de experimentos diversos.
Reconstruyendo la conversación oculta entre quinasas
Tras inferir qué quinasas se volvían más o menos activas, los autores trataron de reconstruir la “conversación” subyacente entre ellas: qué quinasas probablemente activan o influyen en otras. Convirtieron sus mapas quinasas–sustrato en redes de quinasas–quinasas y aplicaron tres estrategias computacionales, que van desde esquemas de clasificación simples hasta un enfoque más complejo que obliga al resultado a parecerse a un árbol dirigido con raíz en el receptor de EGF. Compararon las rutas inferidas resultantes con varios tipos de “verdad de referencia”: un mapa de EGF cuidadosamente curado en una base de datos, experimentos a gran escala donde se sobreexpresaron quinasas individuales y pares de sitios de quinasas cuyo comportamiento estaba fuertemente correlacionado a lo largo del tiempo.
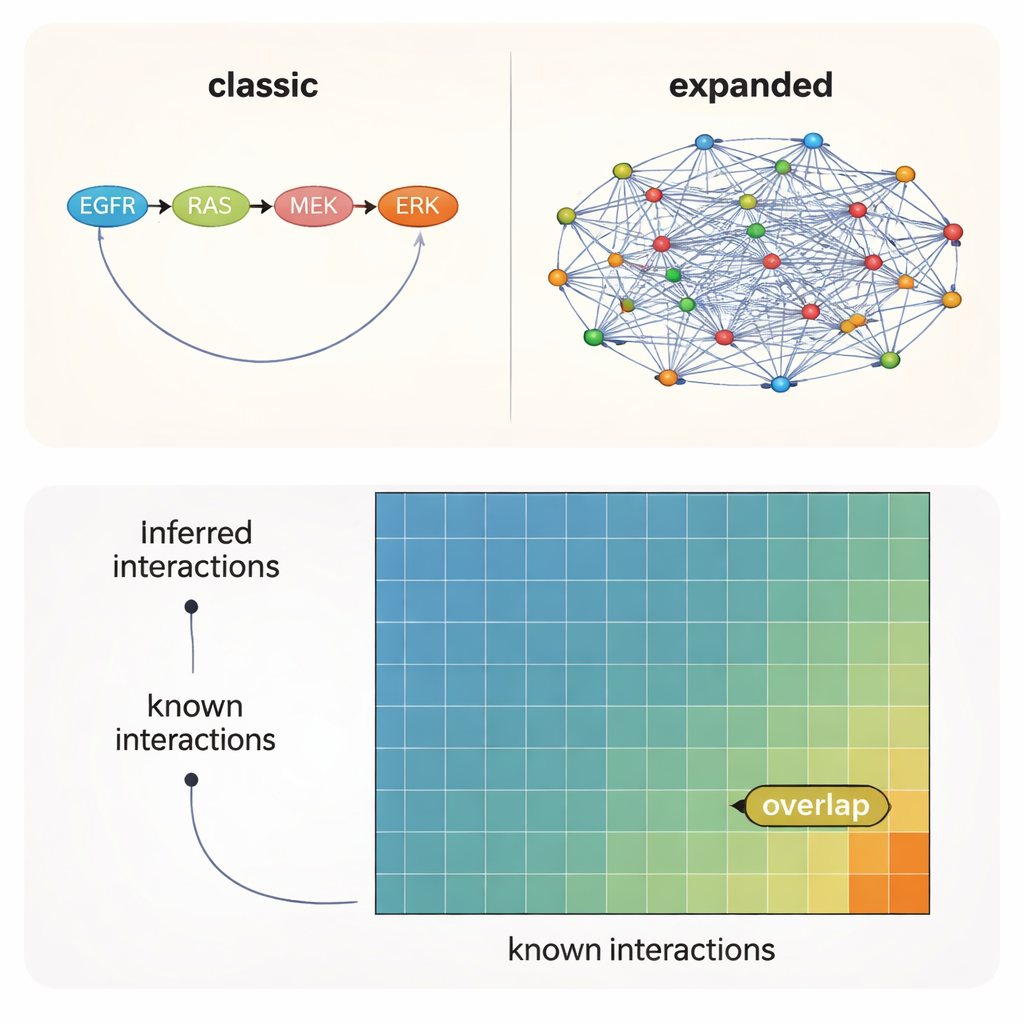
Los enlaces más plausibles siguen fuera del mapa oficial
En todas las pruebas quedó claro un mensaje: la elección del conocimiento previo —la red inicial que alimentas al algoritmo— importaba más que el método concreto o incluso el contexto experimental. Las redes construidas a partir de la literatura recuperaron el mayor número de interacciones conocidas, mientras que recursos predictivos más amplios apuntaron a muchas conexiones plausibles adicionales que aún no se han documentado formalmente. Sin embargo, incluso en las mejores condiciones, solo alrededor del 10–12 % de las interacciones sugeridas por los datos y los modelos estaban presentes en alguno de los conjuntos de referencia. En otras palabras, aproximadamente el 90 % de los enlaces quinasas–quinasas respaldados se sitúan en territorio inexplorado.
Qué significa esto para futuros tratamientos
Para el público general, la conclusión es que el conocido diagrama de la vía EGF en los libros de texto probablemente es solo la punta del iceberg. La fosfoproteómica moderna combinada con métodos computacionales avanzados revela una red de señalización mucho más rica y enmarañada. Muchas de estas conexiones recién sugeridas pueden representar vías pasadas por alto en las que las células cancerosas redirigen señales para evadir fármacos, o nuevas oportunidades para diseñar combinaciones de fármacos más inteligentes. El estudio no demuestra que cada nuevo enlace sea real, pero proporciona una hoja de ruta y herramientas abiertas para que los investigadores prueben estas ideas, con el objetivo final de terapias más precisas y efectivas en enfermedades donde la señalización EGF desempeña un papel central.
Cita: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Palabras clave: señalización EGF, fosfoproteómica, cinasas de proteínas, redes de señalización celular, biología del cáncer