Clear Sky Science · es
Mycobacterium tuberculosis modula la fosforilación de la subunidad ATP6V1E1 del huésped para promover la supervivencia intracelular
Por qué esto importa para combatir la tuberculosis
La tuberculosis sigue siendo una de las enfermedades infecciosas más mortales del mundo, causando la muerte de más de un millón de personas cada año. Nuestras células inmunitarias disponen de potentes “contenedores ácidos de reciclaje” que normalmente digieren los microbios invasores. Este artículo revela cómo la bacteria de la tuberculosis, Mycobacterium tuberculosis (Mtb), sabotea ese sistema de acidificación dentro de nuestras células y muestra que un fármaco dirigido a este mecanismo puede ayudar a animales infectados a eliminar la infección con mayor eficacia.
El baño ácido celular para los gérmenes
Cuando las bacterias de la tuberculosis se inhalan en los pulmones, son rápidamente engullidas por células inmunitarias llamadas macrófagos. Las bacterias acaban en burbujas membranosas que deberían fusionarse con lisosomas, sacos pequeños llenos de enzimas digestivas que funcionan mejor en un entorno muy ácido. Esa acidez la crea una bomba molecular, la ATPasa vacuolar (V-ATPasa), que usa el combustible celular para introducir protones en los lisosomas y bajar el pH interno. Una acidificación adecuada es crucial para descomponer a Mtb, sin embargo décadas de trabajo han mostrado que este patógeno de algún modo mantiene sus compartimentos menos ácidos y sobrevive.
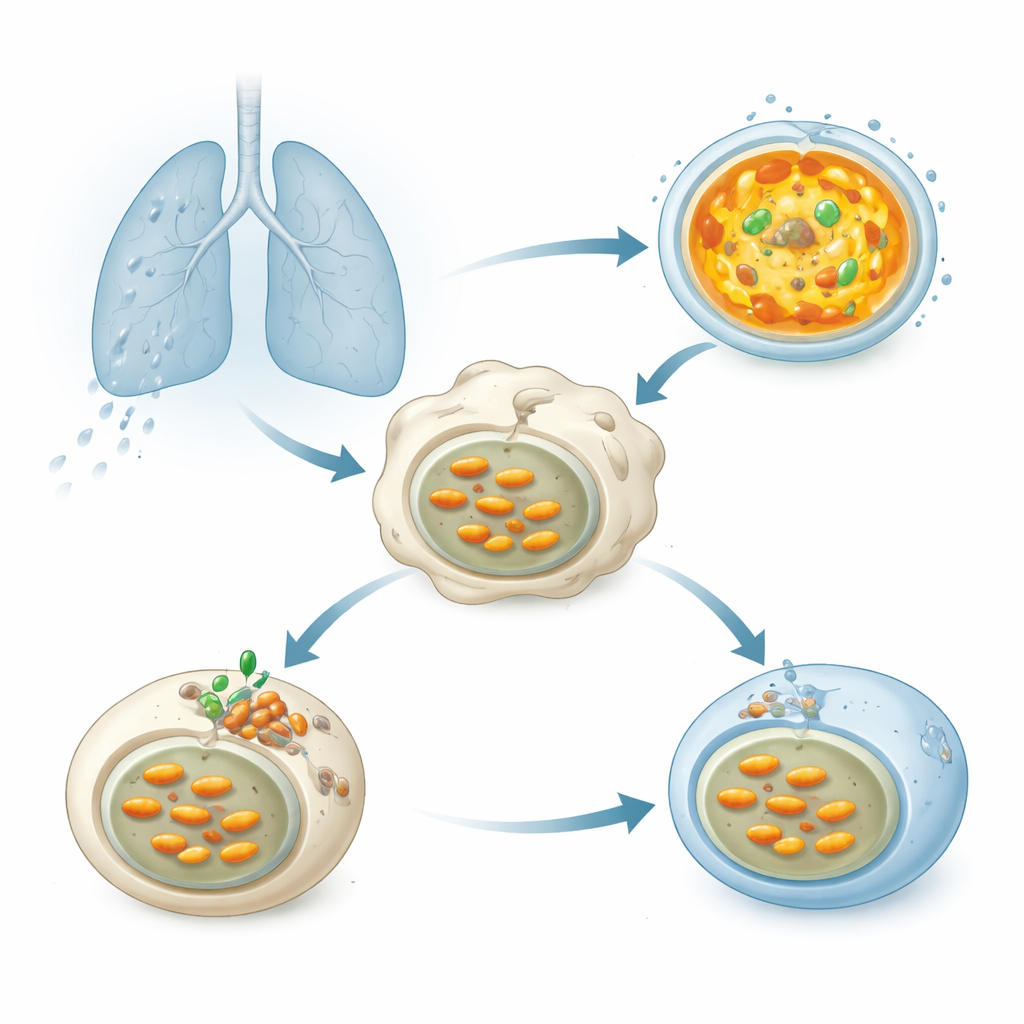
Un ayudante bacteriano secreto que bloquea la acidificación
Los investigadores analizaron más de 200 proteínas que Mtb puede liberar para ver cuáles debilitan la acidificación lisosomal en células humanas. Una destacó: una enzima llamada Chp2 (también conocida como Rv1184). Cuando las células producían Chp2, sus lisosomas se teñían con menos intensidad con tintes sensibles al ácido, lo que indica un pH más alto y menos hostil. Cepas de Mtb diseñadas para carecer de Chp2 dejaron de suprimir la acidificación; en macrófagos infectados y en ratones, estas bacterias mutantes fueron eliminadas con mayor eficacia y causaron menos daño pulmonar. Restaurar Chp2 en la cepa mutante devolvió tanto el bloqueo de la acidificación como la mayor carga bacteriana, identificando a Chp2 como un factor de virulencia que ayuda a Mtb a persistir dentro de las células del huésped.
La subunidad de la bomba del huésped que actúa como interruptor de control
Para entender cómo Chp2 interfiere con la acidificación, el equipo buscó componentes del huésped a los que pudiera unirse. Encontraron que Chp2 se adhiere directamente a una parte particular de la V-ATPasa, una subunidad llamada ATP6V1E1 (E1, en abreviatura), que ayuda a estabilizar la estructura de la bomba. Aumentar la cantidad de E1 en las células incrementó la acidificación lisosomal y dificultó la supervivencia de Mtb, mientras que reducir E1 tuvo el efecto contrario. Ratones que solo tenían una copia funcional del gen de E1 presentaron lisosomas menos ácidos, más carga bacteriana en los pulmones y un daño tisular más grave tras la infección, lo que demuestra que E1 es un defensor importante del huésped contra la tuberculosis.
Una etiqueta de quinasa en la bomba que disminuye la acidez
Los autores se preguntaron si las “etiquetas” químicas en E1 podrían ajustar la actividad de la bomba. Descubrieron que añadir grupos fosfato a dos tirosinas específicas (Tyr56 y Tyr57) de E1 actúa como un freno: imitar la fosforilación redujo la acidificación e impidió el ensamblaje completo de la V-ATPasa, mientras que prevenir la fosforilación tuvo el efecto opuesto. Mediante el cribado de un panel de enzimas, identificaron una quinasa llamada BMX como la proteína del huésped que coloca esta etiqueta. Cuando BMX fue bloqueada genéticamente o con un inhibidor de pequeña molécula, la fosforilación de E1 disminuyó, la bomba se ensambló con mayor eficacia en las membranas lisosomales, los lisosomas se volvieron más ácidos y la supervivencia de Mtb dentro de los macrófagos se redujo.
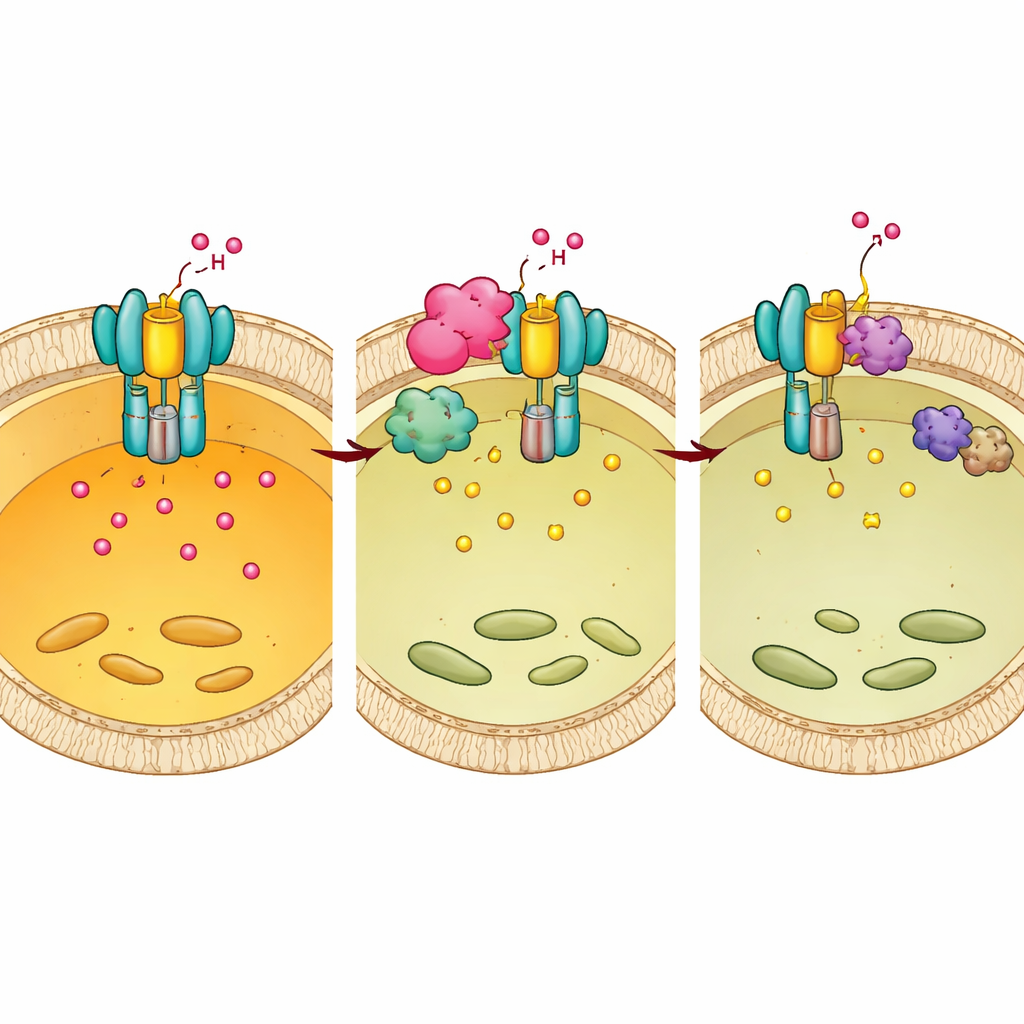
Cómo Mtb reconfigura el interruptor del huésped a su favor
Chp2 y BMX resultan funcionar juntos. Experimentos estructurales y bioquímicos mostraron que Chp2 actúa como andamio que acerca E1 y BMX en la superficie lisosomal, incrementando la fosforilación de E1 en Tyr56/57. Esta etiqueta extra interfiere con el ensamblaje completo de la bomba, eleva el pH lisosomal y crea un entorno más suave en el que Mtb puede persistir. Cuando BMX fue inhibida, desapareció la ventaja de supervivencia que confiere Chp2, tanto en células en cultivo como en ratones infectados. De forma importante, tratar a ratones con el inhibidor de BMX después de la infección redujo la carga bacteriana y la patología pulmonar en animales normales, pero no en ratones con E1 debilitada, lo que indica que el fármaco actúa restaurando la acidificación eficaz impulsada por E1.
Convertir el truco del patógeno en una idea terapéutica
En términos cotidianos, este estudio muestra que las bacterias de la tuberculosis introducen una proteína ayudante en nuestras células que interfiere con la “bomba ácida” del sistema de eliminación de desechos, atenuándola lo justo para que los microbios sobrevivan a la destrucción. Al identificar la subunidad de la bomba que sirve como el mando de control (E1) y la enzima del huésped que la activa (BMX), los autores revelan un punto preciso donde un fármaco puede intervenir. Inhibir BMX en ratones reactiva de forma eficaz el baño ácido interno de la célula y mejora la eliminación bacteriana. Estos hallazgos abren la puerta a terapias dirigidas al huésped que hagan a nuestras propias células más hostiles a Mtb, potencialmente complementando a los antibióticos y ayudando a combatir la tuberculosis resistente a fármacos.
Cita: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Palabras clave: tuberculosis, lisosomas, terapia dirigida al huésped, Mycobacterium tuberculosis, V-ATPasa