Clear Sky Science · es
Desarrollo de un anticuerpo monoclonal potente para el tratamiento de infecciones por metapneumovirus humano
Por qué importa un virus invernal oculto
Cada temporada de resfriados y gripe, un virus poco conocido llamado metapneumovirus humano (HMPV) envía silenciosamente a millones de niños pequeños, adultos mayores y personas con sistemas inmunitarios debilitados a clínicas y hospitales. A diferencia de su pariente viral, el virus respiratorio sincitial (VRS), no existen vacunas ni tratamientos dirigidos para HMPV. Este estudio informa del descubrimiento de un anticuerpo fabricado en laboratorio, denominado 4F11, que puede detener al HMPV en células y proteger a animales infectados, apuntando a un fármaco muy necesario para algunos de los pacientes más vulnerables.
El virus que pasa desapercibido
HMPV es un virus respiratorio común en todo el mundo, responsable de una estimación de 14 millones de infecciones del tracto respiratorio inferior en niños menores de cinco años cada año, y también causa una carga considerable en adultos mayores de 60 años. En pacientes con sistemas inmunitarios gravemente debilitados —como receptores de trasplante de células madre— la tasa de mortalidad por infecciones pulmonares por HMPV puede ser alarmantemente alta. Las vacunas apenas están empezando a aparecer para virus relacionados como el VRS, y aun si existiera una vacuna contra HMPV, muchos pacientes muy inmunocomprometidos responderían mal. Debido a esta laguna, los investigadores recurren a anticuerpos monoclonales —proteínas inmunitarias de acción muy precisa que se pueden administrar como fármacos— para prevenir o tratar infecciones graves.
Encontrar un anticuerpo protector sobresaliente
El equipo se propuso encontrar un anticuerpo con tres rasgos clave: debía ser extremadamente potente, actuar frente a muchas cepas diferentes de HMPV y dejar poco margen al virus para evolucionar resistencia. Se centraron en la proteína de fusión del virus, una estructura en tensión en la superficie viral que debe cambiar de forma para permitir que el virus se fusione con y entre en las células pulmonares. Usando una estrategia de «cebo y cambio», pescaron células B humanas raras en muestras de sangre y bazo que podían reconocer una cepa de HMPV pero neutralizar otra, enriqueciendo así anticuerpos de acción amplia. De más de mil células candidatas, aislaron tres anticuerpos prometedores y hallaron que uno —4F11— era excepcionalmente potente, bloqueando la infección de células a concentraciones casi 50 veces más bajas que un anticuerpo líder previo y funcionando contra los cuatro subtipos principales de HMPV en todo el mundo.
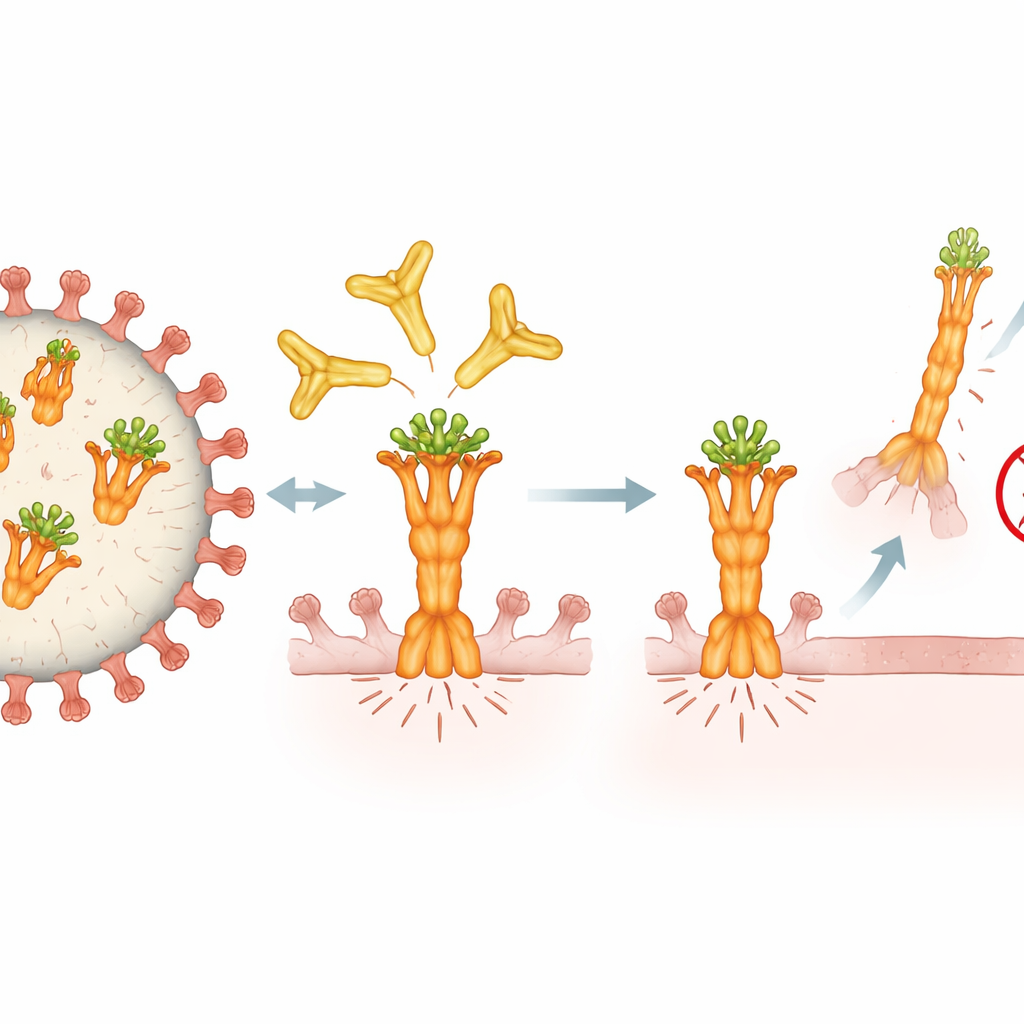
Cómo 4F11 se aferra al punto débil del virus
Para entender por qué 4F11 es tan eficaz, los investigadores utilizaron criomicroscopía electrónica de alta resolución para visualizar cómo se fija a la proteína de fusión. Descubrieron que 4F11 se dirige a un pequeño parche conservado en la cima misma de la forma prefusión de la proteína —el muelle antes de que se dispare. A diferencia de otros anticuerpos que se unen tres copias por proteína de fusión, 4F11 se coloca sola en el ápice en una relación uno a uno, alcanzando hacia abajo e incluso sujetando una decoración azucarada que protege la superficie. Este ángulo de unión inusual y su dependencia de ese azúcar hacen de 4F11 un tipo de anticuerpo singular. Reconoce únicamente la forma prefusión, que está presente en el virus infeccioso, y probablemente impide que la proteína se repliegue en la forma necesaria para perforar y fusionarse con una célula huésped.
¿Puede el virus escapar, y a qué precio?
El equipo hizo crecer entonces el virus en cultivo celular en presencia constante de 4F11 para ver qué tan fácilmente podía evolucionar una vía de escape. En comparación con otro anticuerpo de control, que rápidamente indujo la aparición de varias mutaciones de escape, a HMPV le resultó mucho más difícil evadir a 4F11. Solo un cambio en la proteína de fusión, alterando un aminoácido en la posición 179, interrumpió por completo la unión de 4F11. Sin embargo, los virus con esta mutación crecieron mucho peor que el virus normal, lo que indica un serio perjuicio en la aptitud viral. Búsquedas en bases de datos de cientos de secuencias de HMPV mostraron que este cambio dañino nunca se ha observado en la naturaleza, lo que sugiere que, aunque el virus pueda, en principio, escapar de 4F11 en el laboratorio, paga un precio tan alto en crecimiento que es improbable que se propague ampliamente en el mundo real.
Probar la protección en un modelo animal
La potencia en el laboratorio debe traducirse aún en protección real. Para probarlo, los investigadores infectaron hamsters sirios dorados con HMPV y, al día siguiente, los trataron con 4F11 —simulando una terapia temprana más que una prevención. Una única inyección de baja dosis de 4F11 redujo drásticamente los niveles de virus tanto en los pulmones como en las cavidades nasales, y a la dosis más alta eliminó por completo el virus detectable en los pulmones en la mayoría de los animales. Cabe destacar que estas dosis fueron menores que las usadas para varios anticuerpos monoclonales ya aprobados para VRS en humanos. En contraste, un anticuerpo descrito previamente que puede reaccionar de forma cruzada con varios virus ofreció poca protección a la misma dosis, lo que subraya la fuerza particular de 4F11 como terapia enfocada contra HMPV.
Qué podría significar para los pacientes
En conjunto, estos hallazgos sitúan a 4F11 como un fuerte candidato para el desarrollo clínico. Combina alta potencia, cobertura amplia de las cepas circulantes de HMPV, una forma distintiva de fijarse a una región vulnerable de la proteína de fusión y un panorama de resistencias en el que la vía de escape evidente del virus conlleva una desventaja autoimpuesta sustancial. Para lactantes, adultos mayores y pacientes inmunocomprometidos con alto riesgo de enfermedad grave por HMPV, un fármaco basado en 4F11 podría algún día ofrecer tanto tratamiento de emergencia tras la infección como protección añadida junto a, o en lugar de, las vacunas.
Cita: Harris, E.D., McGovern, M., Pernikoff, S. et al. Development of a potent monoclonal antibody for treatment of human metapneumovirus infections. Nat Commun 17, 2714 (2026). https://doi.org/10.1038/s41467-026-69328-w
Palabras clave: metapneumovirus humano, anticuerpo monoclonal, infección respiratoria, proteína de fusión, terapia antivírica