Clear Sky Science · es
La red neuronal preóptica kisspeptina-nNOS-GnRH (KiNG) regula la ritmicidad de la LH mediante activación-inhibición en ratones
Por qué esta historia cerebral importa para la fertilidad
La ovulación y la fertilidad dependen de un pequeño grupo de células cerebrales que liberan una hormona maestra en pulsos y en ocasionales picos. Cuando este cronometraje falla, la reproducción puede verse comprometida. Este estudio revela cómo dos tipos de moléculas de señalización en el cerebro del ratón, una que activa la actividad y otra que la apaga de forma discreta, trabajan juntas para moldear estos ritmos hormonales. Comprender este circuito de temporización oculto podría, a la larga, ayudar a explicar ciertas formas de infertilidad y sugerir nuevas vías para tratar los trastornos reproductivos.
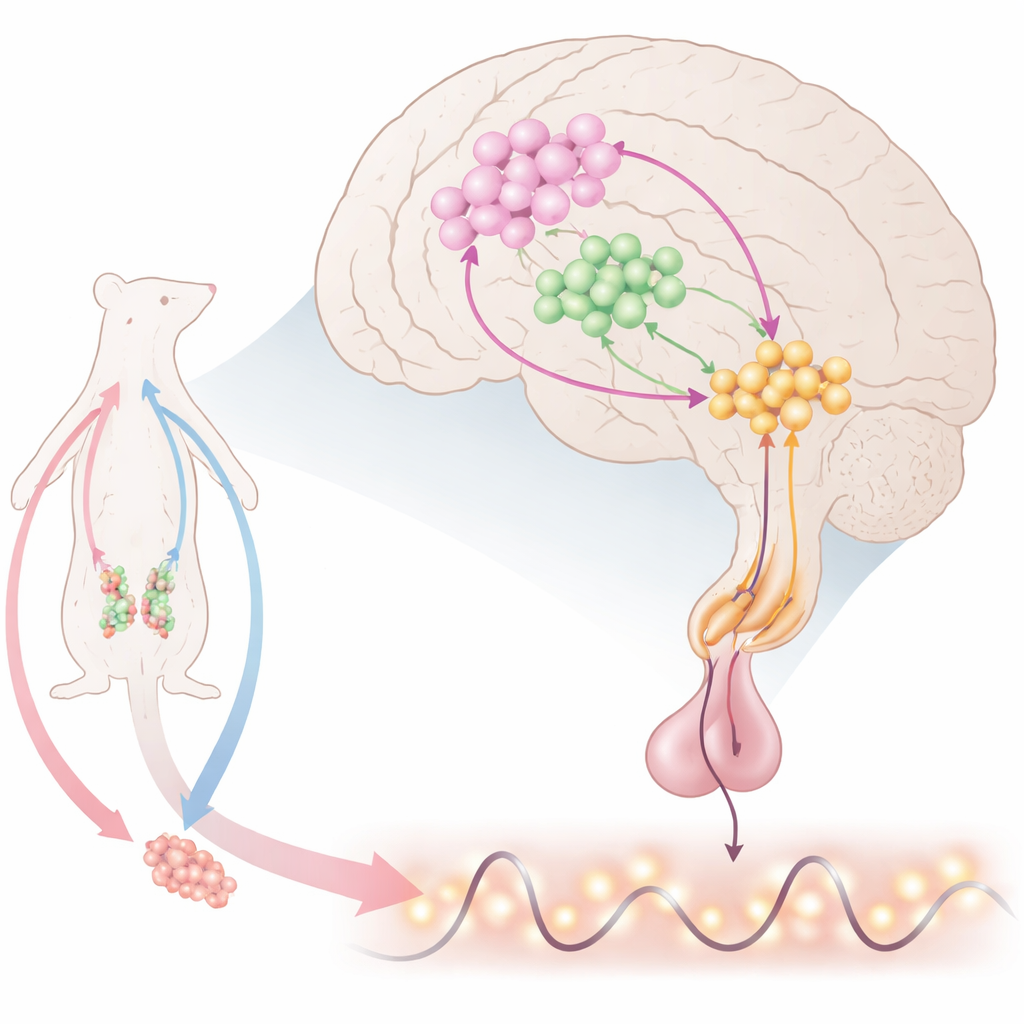
El reloj cerebral de la reproducción
En lo más profundo del cerebro, células nerviosas especiales liberan la hormona liberadora de gonadotropina (GnRH), que indica a la hipófisis que libere la hormona luteinizante (LH) y la hormona foliculoestimulante. Estas, a su vez, controlan los ovarios y los testículos. La GnRH no se secreta de manera continua; en su lugar aparece en pulsos regulares y, en las hembras, en un gran pico preovulatorio. Los científicos saben que muchas señales convergen sobre las células de GnRH, pero la combinación exacta que genera tanto los pulsos como los picos ha permanecido poco clara. Este trabajo se centra en una pequeña región en la parte frontal del hipotálamo, donde las células de GnRH se mezclan con otros dos actores importantes: neuronas productoras de kisspeptina que excitan a GnRH, y neuronas que sintetizan óxido nítrico (NO), una señal gaseosa que puede difundirse en distancias cortas.
Una asociación de encendido–apagado entre dos señales
Los investigadores proponen una red de tres componentes denominada “KiNG”, formada por kisspeptina, neuronas productoras de NO (nNOS) y células de GnRH. La kisspeptina es un potente activador que puede impulsar la liberación de GnRH y LH, pero la estimulación continua en realidad desactiva el sistema, lo que sugiere que se necesita un freno interno. Empleando sondas moleculares de alta sensibilidad, herramientas genéticas y grabaciones en cortes cerebrales en ratones, el equipo muestra que la kisspeptina hace más que excitar directamente a las neuronas GnRH. También activa las neuronas nNOS cercanas en el área preóptica, especialmente en una región llamada OV/MePO. Cuando los niveles de kisspeptina aumentan, estas células nNOS producen pulsos de NO, que desencadenan la producción de un segundo mensajero, el GMP cíclico (cGMP), en las células circundantes, incluidas las propias neuronas GnRH. Esta señal NO–cGMP atenúa la descarga de GnRH, proporcionando un interruptor de apagado incorporado al impulso de la kisspeptina.
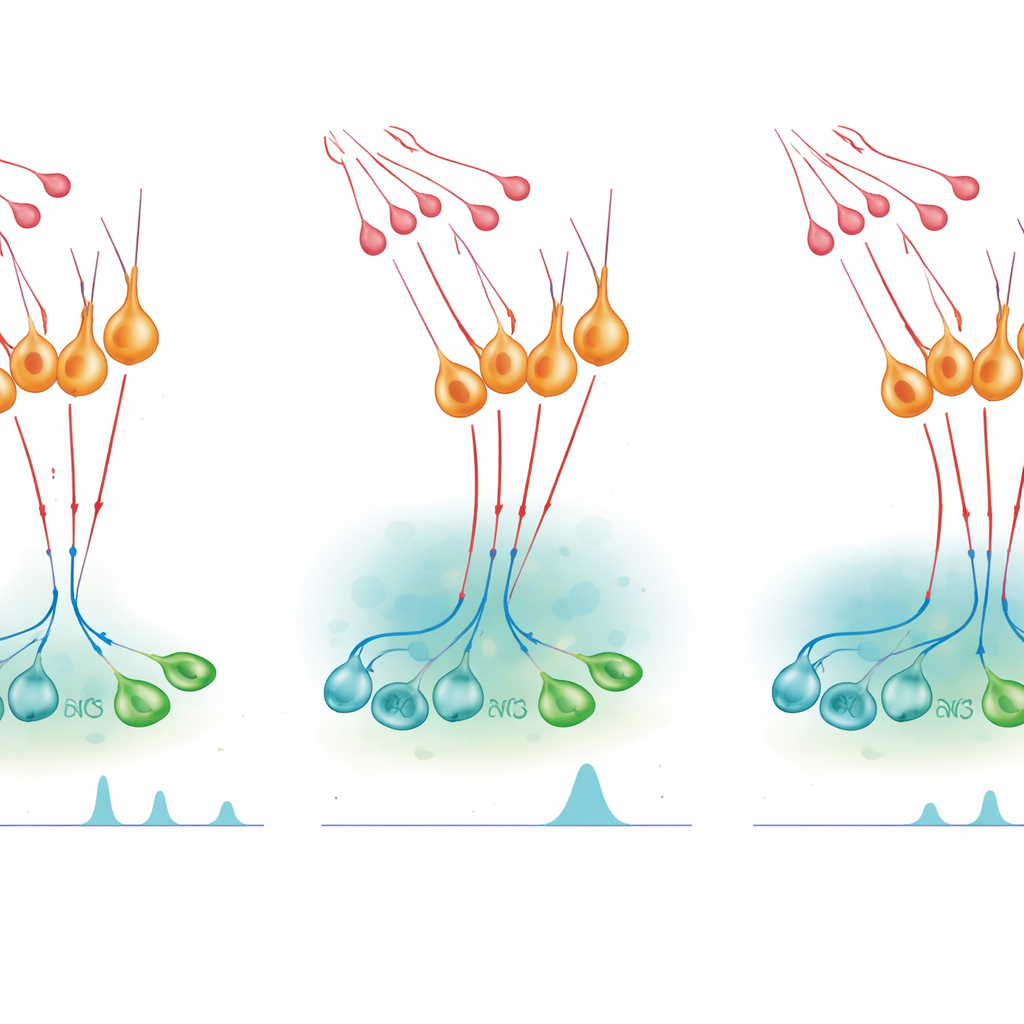
Encender los picos hormonales y recortarlos
Para probar cómo afecta este microcircuito a la liberación hormonal, el equipo usó conmutadores quimiogenéticos —receptores diseñados activados por un fármaco por lo demás inerte— para activar o silenciar las neuronas nNOS en ratones vivos. Activar artificialmente las células nNOS durante una fase normalmente silenciosa del ciclo femenino fue suficiente para producir un aumento en sangre de LH de tipo pico, y lo mismo ocurrió en machos. Bloquear la producción de NO eliminó este efecto, demostrando que el NO de estas neuronas es necesario para el pico. Sin embargo, cuando los científicos inhibieron las neuronas nNOS o redujeron su sensibilidad a la kisspeptina, una inyección de kisspeptina produjo un aumento de LH exagerado y prolongado. Fármacos que bloquean la síntesis de NO tuvieron un efecto amplificador similar, mientras que un fármaco que prolonga la señalización por cGMP acortó la respuesta a la kisspeptina y redujo la secreción posterior de LH. En conjunto, estos experimentos indican que el NO tanto ayuda a sincronizar las neuronas GnRH para crear picos como limita cuánto tiempo la kisspeptina puede mantener su actividad.
Un ritmo flexible a lo largo del ciclo ovárico
El estudio también revela que este equilibrio de encendido–apagado cambia a lo largo del ciclo femenino. Empleando un método sensible de detección de ARN, los autores encontraron que más neuronas nNOS expresan el receptor de kisspeptina el día anterior a la ovulación, cuando los niveles de estrógeno son altos y ocurre el pico de LH. Durante las etapas más tranquilas, menos neuronas nNOS responden a la kisspeptina, produciendo solo pequeñas cantidades locales de NO que moderan suavemente los pulsos de GnRH sin detenerlos. En el día del pico, una entrada de kisspeptina más fuerte y una mayor expresión del receptor aumentan masivamente la producción de NO, permitiendo que el NO se difunda más y silencie brevemente a muchas neuronas GnRH a la vez. A medida que la señal de NO se desvanece, estas células se recuperan de forma conjunta, generando el gran pico coordinado de LH necesario para la ovulación.
Qué significa esto para la salud humana
En términos sencillos, este trabajo muestra que la misma señal que pone en marcha a las neuronas GnRH —la kisspeptina— también recluta un sistema de frenado retardado mediante NO, garantizando que los arrebatos hormonales sean intensos pero no descontrolados. La red KiNG actúa, por tanto, tanto como acelerador como freno del tiempo reproductivo, afinando los pulsos de GnRH durante la mayor parte del ciclo y moldeando el pico que desencadena la ovulación. Dado que se han encontrado variaciones genéticas en las vías de la kisspeptina y del NO en personas con problemas reproductivos, comprender este circuito finamente equilibrado podría aportar enfoques nuevos para diagnosticar y tratar la infertilidad y condiciones relacionadas.
Cita: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Palabras clave: hormonas reproductivas, hipotálamo, kisspeptina, óxido nítrico, cronometraje de la ovulación