Clear Sky Science · es
La lactilación de histonas aumenta la expresión de CXCL1 para la infiltración de neutrófilos y la evasión inmune en el cáncer de páncreas
Por qué importa este estudio sobre el cáncer
El cáncer de páncreas es uno de los más letales, en parte porque con frecuencia resiste las inmunoterapias modernas que funcionan en otros tumores. Este estudio revela cómo los tumores pancreáticos reprograman su propio metabolismo de la glucosa para desarmar silenciosamente al sistema inmune, y cómo bloquear ese proceso podría reabrir una vía para que las defensas del organismo —y fármacos ya existentes— vuelvan a combatirlo.
Tumores hambrientos de azúcar y un vecindario hostil
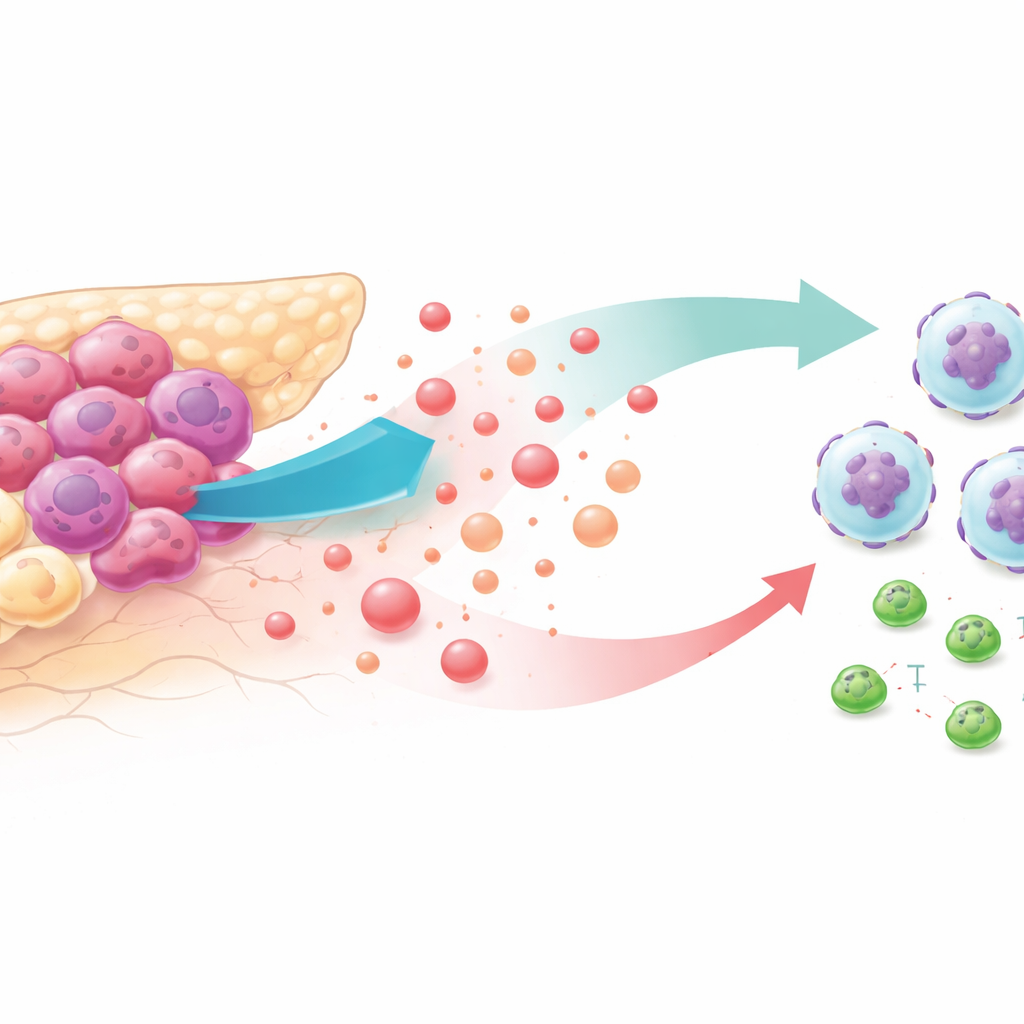
Las células cancerosas son famosas por consumir glucosa a un ritmo frenético, incluso cuando hay oxígeno disponible. Este estilo de “alta glucólisis” inunda el entorno tumoral con lactato, un subproducto que antes se consideraba un desperdicio metabólico. Analizando bases de datos de tumores de pacientes y modelos en ratón, los investigadores encontraron que los cánceres pancreáticos con la glucólisis más intensa estaban llenos de neutrófilos —glóbulos blancos que, en este contexto, ayudan al tumor a crecer— y tenían menos células CD8 que matan el cáncer. Los pacientes cuyos tumores mostraban este perfil tendieron a vivir menos tiempo, lo que sugiere que el metabolismo alterado y la evasión inmune están estrechamente vinculados.
Cómo los tumores usan el lactato para atraer la ayuda equivocada
Para entender cómo la glucólisis atrae neutrófilos, el equipo redujo la glucólisis tumoral con fármacos o trucos genéticos en líneas celulares de cáncer de páncreas y en ratones. Cuando se bloqueó la degradación de azúcar, las células tumorales liberaron mucho menos una señal química llamada CXCL1, y los niveles circulantes de esta señal bajaron en ratones y en muestras de pacientes. En pruebas de migración en laboratorio, los neutrófilos se desplazaron con entusiasmo hacia el medio procedente de células cancerosas altamente glucolíticas pero no hacia el medio de células con glucólisis bloqueada, a menos que los investigadores añadieran CXCL1 purificado. En ratones vivos, restaurar CXCL1 en tumores con glucólisis reducida devolvió los neutrófilos y debilitó el efecto antitumoral de la inhibición de la glucólisis.
Un nuevo interruptor epigenético impulsado por el lactato
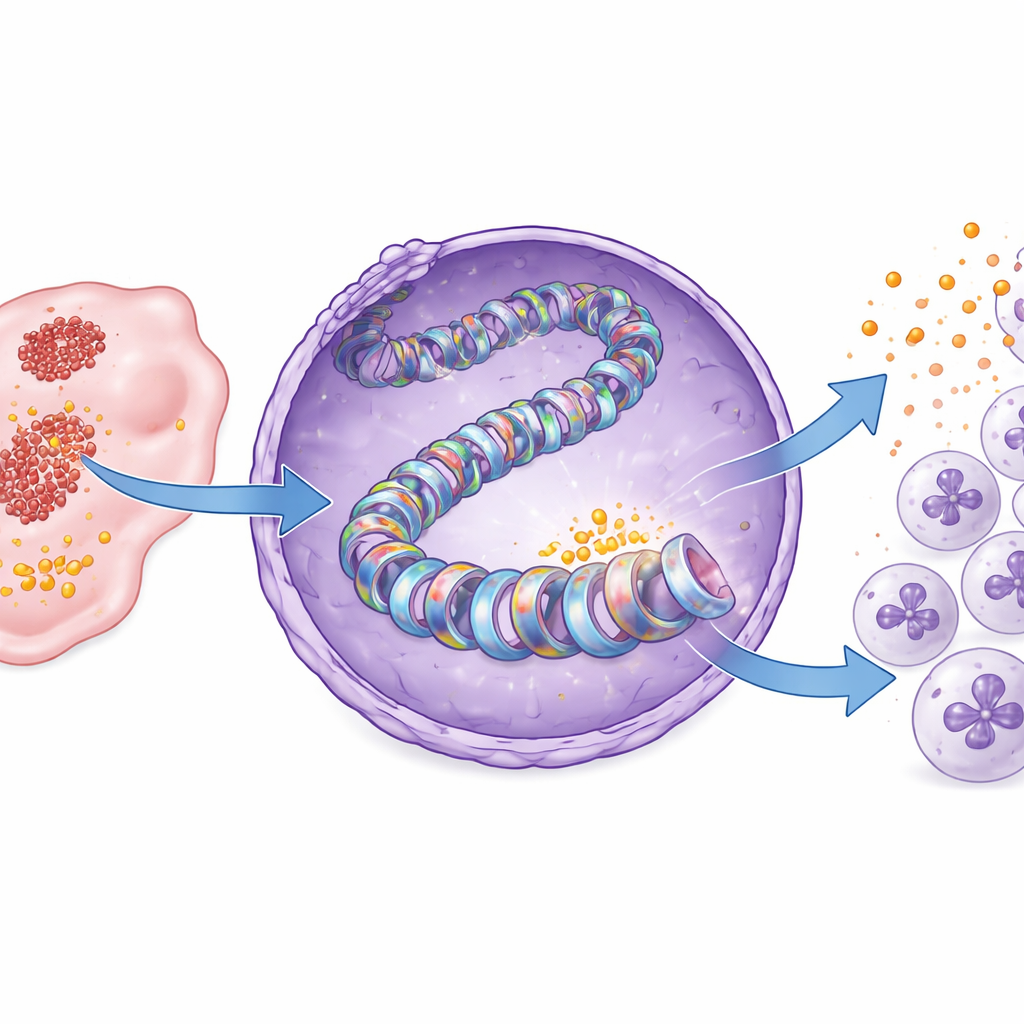
El estudio se centró luego en el nivel del empaquetamiento del ADN. Nuestros genes están envueltos alrededor de proteínas en forma de carrete llamadas histonas, cuyas marcas químicas actúan como interruptores de encendido/apagado de la actividad génica. Los autores muestran que, en el cáncer de páncreas, el lactato producido por la glucólisis añade una marca específica “lactilo” en una posición de la histona conocida como H3K18. Esta modificación, llamada lactilación de la histona H3K18, fue notablemente más alta en tejidos tumorales que en el páncreas normal. Cuando se bloqueó la glucólisis, la lactilación en H3K18 cayó, especialmente cerca de la región de control del gen CXCL1, y la producción de CXCL1 disminuyó. Volver a añadir lactato restableció tanto la marca en la histona como la expresión de CXCL1. En las muestras de pacientes, los tumores con más lactilación en H3K18 también mostraron mayor CXCL1, vinculando esta señal molecular con un paisaje inmune pro‑tumoral.
Identificación de la enzima y un punto débil atacable
Las marcas en histonas las escriben enzimas especializadas. Mediante cribado de inhibidores de proteínas conocidas por modificar histonas, los investigadores identificaron una llamada PCAF como el escritor clave de la marca de lactilación en H3K18 en el cáncer de páncreas. El modelado estructural sugirió que PCAF puede unirse a lactil‑CoA, la forma activada del lactato usada para marcar, y ensayos bioquímicos confirmaron que PCAF purificada puede añadir directamente grupos lactilo a la histona H3. Bloquear PCAF con una pequeña molécula, bromosporina, redujo la lactilación en H3K18 y la producción de CXCL1 en células cancerosas y en tumores de ratón. Como resultado, entraron menos neutrófilos en los tumores, se acumularon más células CD8, y el crecimiento tumoral se ralentizó, todo ello sin pérdida de peso evidente ni toxicidad en los ratones.
Convertir un tumor frío en caliente con terapia combinada
Puesto que los fármacos estándar de bloqueo de puntos de control inmunitarios, como los anticuerpos anti–PD‑1, han mostrado un éxito limitado en el cáncer de páncreas, el equipo probó si desmantelar la vía lactato–PCAF–CXCL1 podría hacer que estos tumores respondieran mejor. En modelos de ratón subcutáneos y ortotópicos pancreáticos, la combinación de bromosporina con anti–PD‑1 encogió los tumores más que cualquiera de los tratamientos por separado, redujo la infiltración de neutrófilos, aumentó las células CD8 activas y prolongó significativamente la supervivencia. Esto sugiere que cortar la “sirena” metabólica del tumor para los neutrófilos ayuda a convertir un tumor inmunológicamente “frío” en uno más “caliente” al que la terapia con inhibidores de puntos de control puede implicarse mejor.
Qué significa esto para el tratamiento futuro
En términos sencillos, el estudio revela una reacción en cadena: los tumores pancreáticos queman azúcar, liberan lactato, usan ese lactato para activar un interruptor epigenético en sus proteínas de empaquetamiento del ADN, aumentan CXCL1 y así reclutan neutrófilos que les ayudan a ocultarse de las células T asesinas. Interrumpir esta cadena en el paso de PCAF con un fármaco no solo ralentiza los tumores sino que también potencia la inmunoterapia existente en ratones. Aunque se necesita más trabajo para asegurar la seguridad y encontrar la mejor manera de dirigir esta vía en personas, estos hallazgos destacan una estrategia prometedora: reprogramar el metabolismo y los interruptores génicos del tumor para dar al sistema inmune una oportunidad justa de combatirlo.
Cita: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Palabras clave: cáncer de páncreas, metabolismo tumoral, lactilación de histonas, microambiente tumoral, inmunoterapia contra el cáncer