Clear Sky Science · es
Aprovechando la cinética de unión predecible de DNA-PAINT para eliminar ruido en imágenes de superresolución
Vistas más nítidas del mundo diminuto
Los microscopios modernos ya pueden “ver” moléculas individuales dentro de las células, pero estas imágenes a menudo aparecen salpicadas de puntos de fondo engañosos. Este estudio presenta una forma de limpiar esas imágenes aprovechando cómo fragmentos de ADN se unen y se separan de manera natural con el tiempo. El resultado son imágenes más nítidas de la maquinaria molecular dentro de las células, lo cual es importante tanto para la biología básica como para el descubrimiento de fármacos.
Cómo un truco de parpadeo revela detalles ocultos
Un método de imagen potente, llamado DNA-PAINT, convierte la unión aleatoria de hebras cortas de ADN en un microscopio de superresolución. Una hebra de ADN se une a la proteína que el científico quiere ver; una hebra complementaria con un tinte fluorescente flota en la solución. Cuando la hebra flotante se une brevemente a su pareja, produce un pequeño destello de luz. Registrando muchos de esos parpadeos y localizando su posición, los investigadores pueden reconstruir las posiciones de las proteínas con precisión nanométrica—mucho más nítido que los microscopios ópticos convencionales.
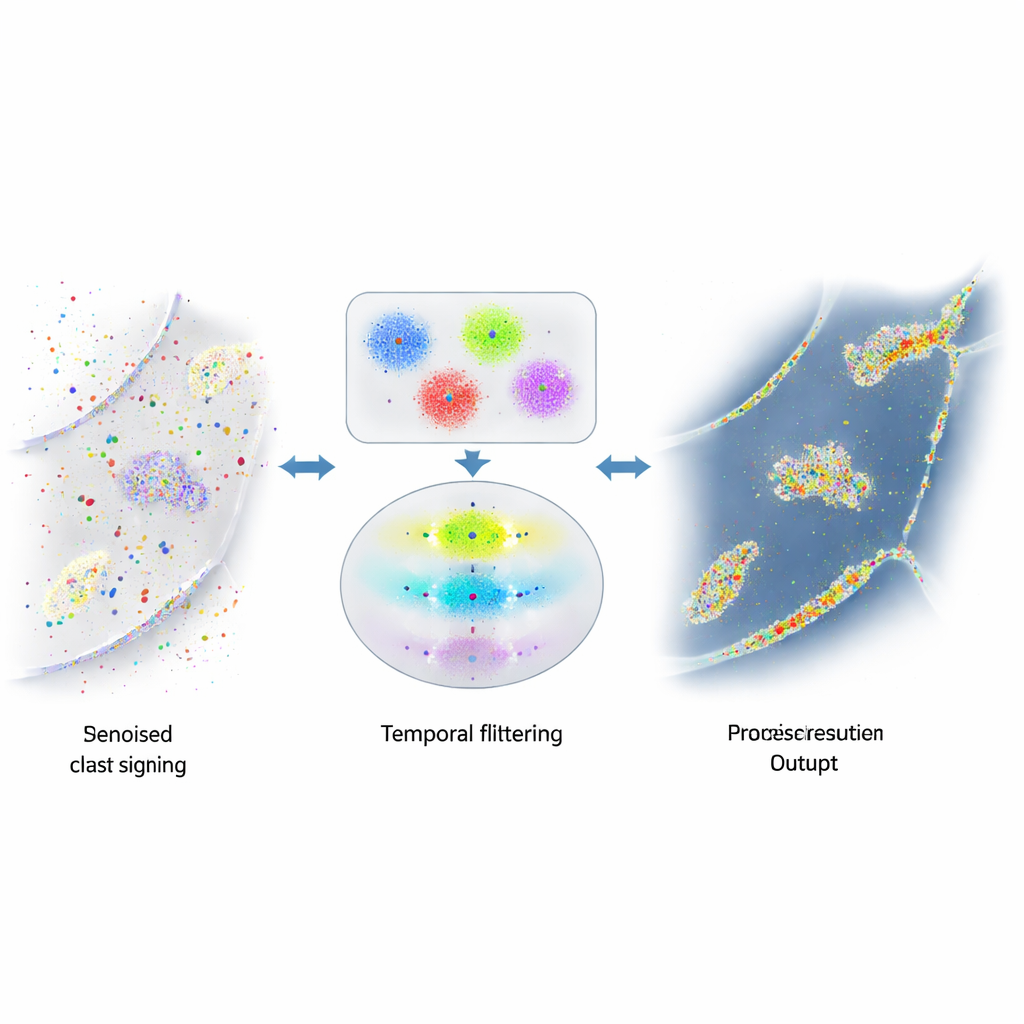
Cuando las señales útiles quedan enterradas en ruido
La fortaleza de DNA-PAINT—la abundancia de hebras fluorescentes en movimiento libre—también crea un problema. Esas hebras se adhieren ocasionalmente donde no deberían, por ejemplo a superficies celulares aleatorias o al abundante ADN dentro del núcleo. Esos destellos accidentales son indistinguibles en apariencia de los verdaderos y ensucian la imagen final con puntos y cúmulos falsos. Intentos previos para reducir este ruido se centraron en cambiar la química para hacer la unión no deseada más rara, o en reglas toscas para detectar valores atípicos evidentes. Aun así, quedó una cantidad considerable de señal engañosa, lo que limitó la fiabilidad de mediciones del número de proteínas o de sus relaciones espaciales.
Usar el tiempo para distinguir verdad de engaño
Los autores se dieron cuenta de que los pares de ADN reales en DNA-PAINT obedecen una regla temporal simple: las pausas entre eventos de unión genuinos siguen un patrón exponencial predecible. En contraste, los eventos de adhesión aleatoria no lo hacen. Construyeron un algoritmo en varios pasos que primero agrupa parpadeos cercanos en pequeños cúmulos según su ubicación, usando una combinación de clustering basado en densidad y k-means para descomponer formas complejas en unidades del tamaño de una localización. Para cada cúmulo, luego construyen una “traza temporal” de eventos de unión, fusionando cuidadosamente parpadeos rápidos de encendido-apagado procedentes de la misma unión en eventos únicos. Finalmente, aplican una prueba estadística para preguntar si los intervalos entre eventos en cada cúmulo coinciden con el comportamiento exponencial esperado. Los cúmulos que aprueban se tratan como reales; los que fallan se descartan como ruido.
Poniendo el método a prueba en células reales
Para probar su enfoque, el equipo imagenó la proteína de adhesión celular E-cadherina en cámaras de huevo de mosca de la fruta, donde algunas células producían la proteína etiquetada y las células vecinas no. Esto creó áreas contiguas ricas en señal genuina y áreas que deberían contener solo fondo. Ajustando cuántos eventos de unión debe mostrar un cúmulo antes de ser evaluado, encontraron configuraciones que eliminaron más del 90% de los cúmulos espurios mientras conservaban más del 98% de los verdaderos en los bordes celulares. En las imágenes desruidas, características finas como estructuras tubulares delgadas y vesículas se hicieron mucho más claras. La misma estrategia funcionó en otros sistemas, incluidas mitocondrias y microtúbulos, e incluso en proteínas con distribuciones más difusas y amorfas, donde los patrones espaciales por sí solos no ofrecen pistas sobre qué es real.
Mapas moleculares más claros para estudios futuros
Al escuchar el “ritmo” de la unión del ADN en lugar de fijarse solo en dónde ocurren los parpadeos, este método elimina de forma fiable el fondo engañoso de los datos de DNA-PAINT. Para no especialistas, el resultado clave es simple: mapas moleculares dentro de las células más nítidos y de mayor confianza. Esto facilita contar cuántas moléculas de proteína hay, juzgar cuán cerca están distintas proteínas entre sí y construir imágenes más precisas de la vida interna de las células. A medida que la imagenología basada en ADN continúa creciendo, este tipo de desruido inteligente será esencial para convertir imágenes granuladas crudas en conocimientos biológicos sólidos.
Cita: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Palabras clave: DNA-PAINT, microscopía de superresolución, reducción de ruido en imágenes, imagen de molécula única, mapeo de proteínas