Clear Sky Science · es
La activación de STING induce respuestas citotóxicas e inmunitarias en meningiomas a través de vías de muerte celular inflamatoria
Volver las alarmas del cuerpo contra los tumores cerebrales
Los meningiomas están entre los tumores cerebrales más comunes y, aunque la cirugía y la radiación suelen ayudar, algunos tumores reaparecen. Estos crecimientos persistentes pueden causar convulsiones, dolores de cabeza y discapacidad, y no existen tratamientos farmacológicos ampliamente aceptados. Este estudio explora una manera de hacer que las propias células tumorales y las células inmunitarias circundantes activen una potente alarma interna mediante una molécula que enciende un sistema innato de detección de peligro llamado STING. Al hacerlo, los investigadores pretenden no solo matar directamente las células tumorales, sino también despertar al sistema inmunitario y suavizar el andamiaje rígido del tumor.
Un tumor oculto en un vecindario inmunitario silencioso
Los autores primero cartografiaron el “vecindario” celular dentro de meningiomas humanos mediante secuenciación unicelular e imágenes espaciales. Encontraron que estos tumores están llenos de células inmunitarias innatas, especialmente macrófagos, mientras que las clásicas células T y células asesinas naturales (NK) que combaten tumores son escasas y con frecuencia están agotadas. Rodeando a las células tumorales hay una densa capa de colágeno y otras proteínas de la matriz que forman una estructura blindada y estratificada. Muchos macrófagos en estas regiones portan receptores inhibitorios que se activan por el colágeno, creando un entorno fuertemente reprimido en el que las células inmunitarias están presentes pero contenidas en lugar de desplegarse contra el cáncer.
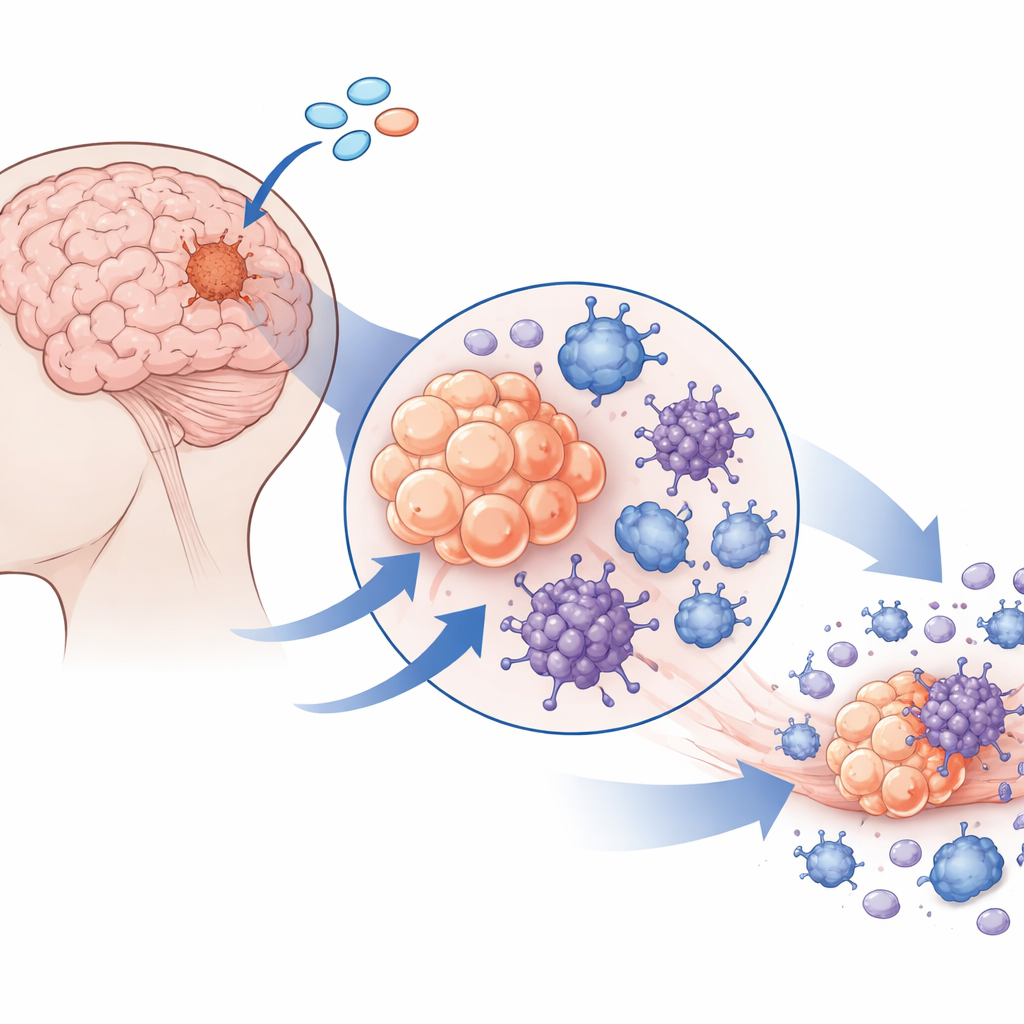
Descubrir un interruptor que las células tumorales aún conservan
A continuación, el equipo buscó vías que pudieran convertir este escenario supresor en uno inflamado y hostil al tumor. Se centraron en STING, un sensor que normalmente responde al ADN fuera de lugar dentro de las células y desencadena respuestas antivirales e inflamatorias. A diferencia de muchos otros tumores cerebrales, las células de meningioma mostraron niveles inusualmente altos de STING. Esto se atribuyó a cromatina abierta y baja metilación del ADN en el gen STING, lo que significa que el gen está epigenéticamente predispuesto a estar activo. STING no solo era abundante en las células tumorales, sino también en células de los vasos sanguíneos cercanos y en macrófagos, lo que sugiere que un solo fármaco podría afectar simultáneamente a muchos actores clave en el microambiente tumoral.
Forzar a las células tumorales a una auto-destrucción inflamatoria
Los investigadores trataron muestras de meningiomas recién extirpados a pacientes con un potente agonista de STING llamado 8803. Incluso cuando se eliminaban las células inmunitarias, las células tumorales morían, lo que demuestra un efecto directo. Al añadir fármacos que bloquean selectivamente distintas rutas de muerte celular y al analizar la actividad génica, mostraron que 8803 no provocaba simplemente apoptosis silenciosa. En su lugar, empujó a las células de meningioma hacia varias formas inflamatorias de muerte: piroptosis, necroptosis y ferroptosis, que hacen que las células estallen en lugar de desmantelarse ordenadamente. Un paso clave fue la activación y escisión de una proteína llamada gasdermina D, que forma poros en la membrana celular. La microscopía electrónica reveló células tumorales llenas de agujeros en la membrana y mitocondrias dañadas, y bloquear las especies reactivas de oxígeno redujo la muerte, vinculando el estrés mitocondrial con esta marcha inflamatoria.
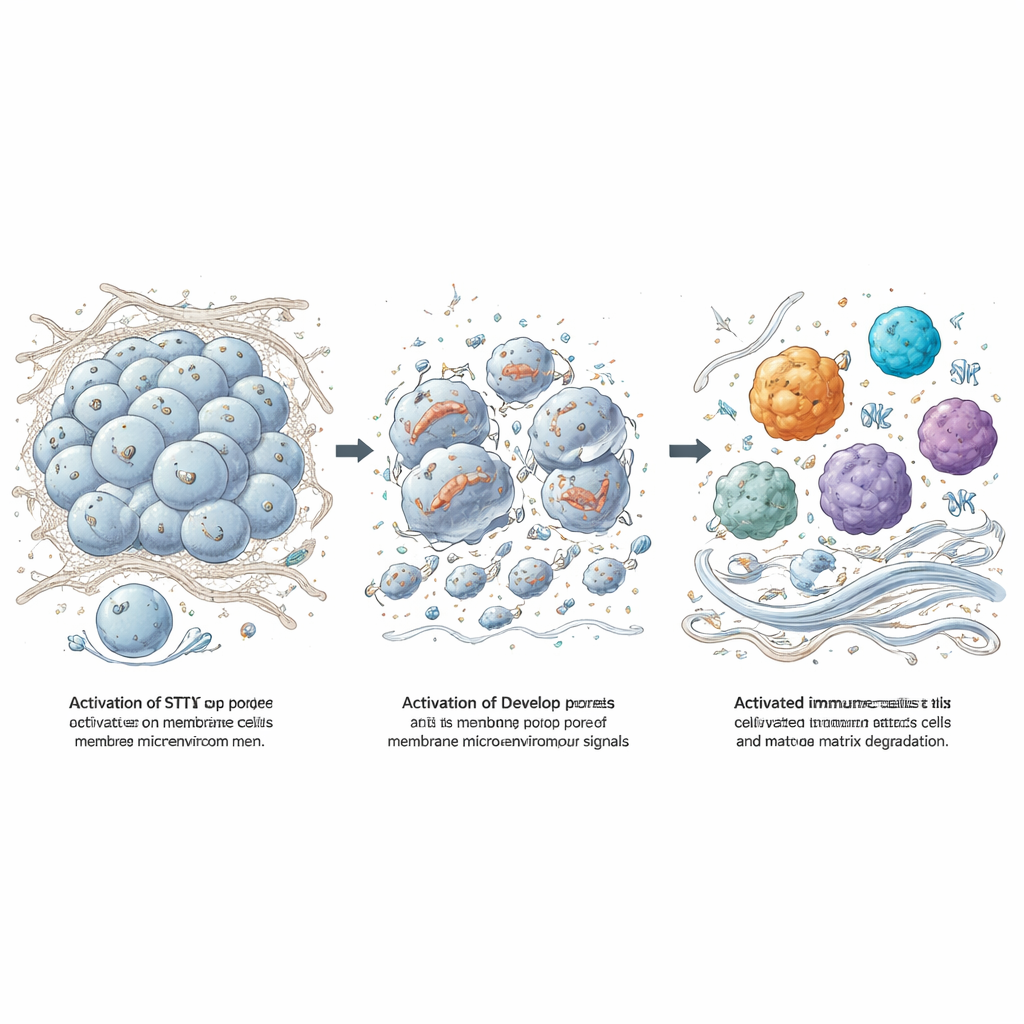
Del desecho tumoral al despertar inmunitario y la erosión de la matriz
Cuando las células tumorales mueren de esta manera dramática, liberan moléculas de “peligro” que pueden activar a las células inmunitarias. El equipo expuso macrófagos de ratón a células de meningioma lisadas y observó un aumento de factores inflamatorios y de enzimas que degradan el colágeno, en especial la metaloproteinasa de matriz-3 (MMP-3). Trabajando con ratones carentes de adaptadores de señalización específicos, demostraron que los receptores tipo toll (TLR), otro sistema de detección de peligro, son cruciales para esta respuesta, mientras que la activación de STING por 8803 añade su propia capa de estimulación inmune. En modelos murinos de meningioma, la inyección directa de 8803 en los tumores redujo o estabilizó el crecimiento, prolongó la supervivencia y convirtió el sitio tumoral de una masa silenciosa y rica en colágeno a otra repleta de macrófagos activos, células NK, células T y con una tinción de colágeno marcadamente reducida.
Por qué este enfoque podría cambiar el tratamiento de los pacientes
En conjunto, el estudio muestra que los meningiomas albergan una vulnerabilidad incorporada: sus células tumorales conservan un interruptor STING accesible que, al activarse con 8803, las empuja hacia una muerte celular explosiva e inflamatoria. Este proceso tanto mata células cancerosas como llena el área de señales de alarma que reclutan y energizan a las células inmunitarias, además de ayudar a degradar el andamiaje de colágeno que contribuye al efecto de masa. Dado que los meningiomas son típicamente localizados en lugar de ampliamente metastásicos, y porque las opciones estándar son limitadas para la enfermedad recurrente, un agonista de STING administrado localmente como 8803 podría ofrecer una nueva vía dirigida para reducir la masa tumoral y reprogramar su entorno inmunitario para un control duradero.
Cita: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
Palabras clave: meningioma, vía STING, inmunoterapia de tumores cerebrales, muerte celular inflamatoria, microambiente tumoral