Clear Sky Science · es
Adgrg6/Gpr126 es necesario para la integridad de la pared compacta y para establecer la identidad trabecular durante la trabeculación cardíaca
Por qué importa la arquitectura de la pared cardíaca
Cada latido depende de una pared interna del corazón finamente esculpida. En los embriones en desarrollo, esta pared se forma primero como una capa lisa y después crece hasta convertirse en un bosque de crestas musculares llamadas trabéculas que ayudan al corazón a bombear con eficiencia. Cuando este proceso falla, niños y adultos pueden desarrollar cardiomiopatías graves. Este estudio explora cómo un receptor poco conocido, Gpr126, ayuda a las células cardíacas a decidir si permanecer en la pared compacta externa o integrarse en esas crestas internas.
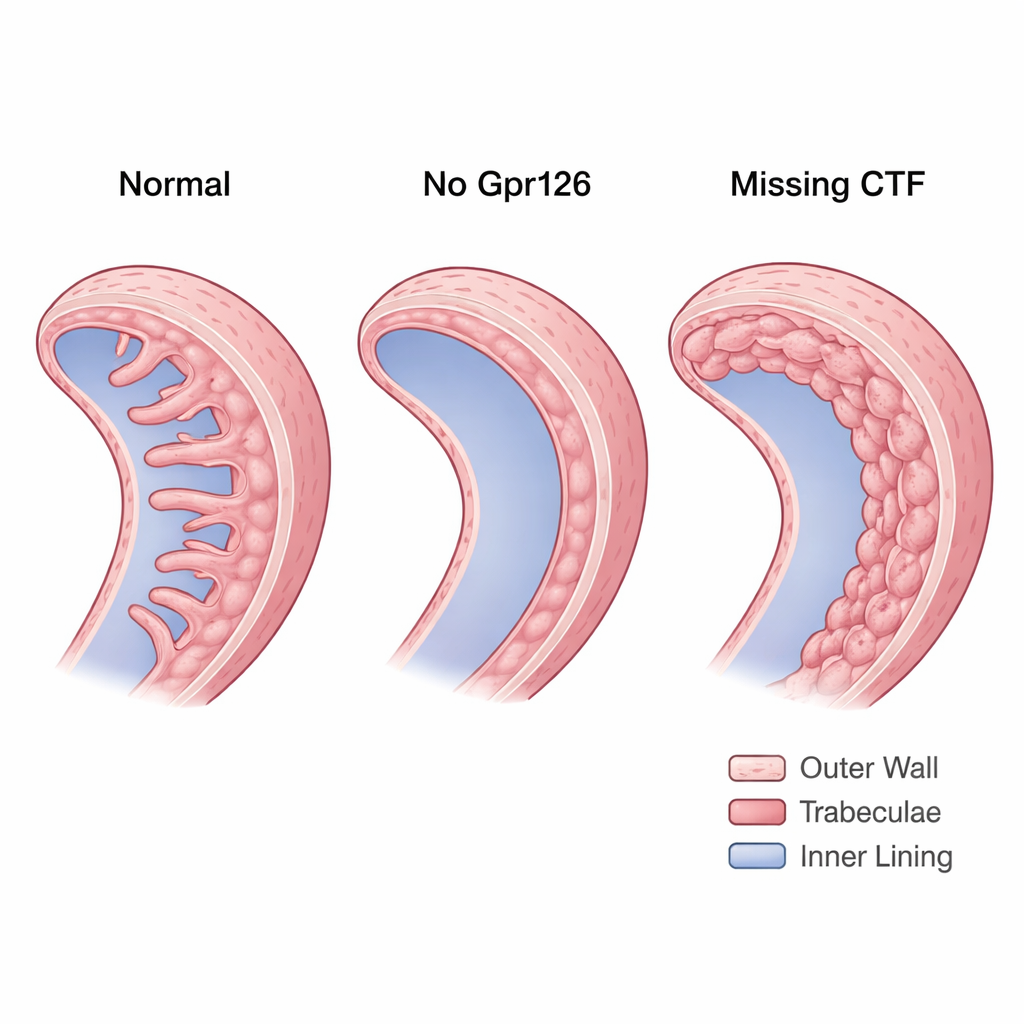
Un receptor de función partida en el corazón
Gpr126 pertenece a una familia de receptores acoplados a proteínas G de adhesión que se sitúan en la membrana celular y perciben el entorno celular. Estos receptores son especialmente interesantes porque muchos fármacos existentes ya apuntan a receptores relacionados, lo que los convierte en candidatos terapéuticos atractivos. Gpr126 es inusual en que se divide de forma natural en dos piezas principales: un fragmento N-terminal (NTF), que sobresale fuera de la célula y puede contribuir a la adhesión célula–célula, y un fragmento C-terminal (CTF), que atraviesa la membrana y desencadena señalización interna. Trabajos previos vincularon a Gpr126 con el desarrollo cardíaco, pero no estaba claro qué hace cada fragmento durante la formación de las trabéculas.
Usar pez cebra para observar cómo toma forma el corazón
Los investigadores emplearon pez cebra, cuyos embriones transparentes permiten la imagen en tiempo real del corazón latiendo. Estudiaron dos variantes genéticas de gpr126. Una (stl47) produce solo una proteína diminuta y gravemente truncada; la otra (st49) produce un NTF estable y secretado que carece de la parte señalizadora CTF. Al combinar estos mutantes con líneas informadoras fluorescentes, el equipo pudo ver células cardíacas individuales, seguir la formación de las trabéculas y monitorizar moléculas clave como N-cadherina (que ayuda a las células a adherirse) y Notch (una vía de señalización que indica a las células qué identidad adoptar).
Mantener unida la pared frente a formar las crestas
Los mutantes stl47, que esencialmente carecen de ambos fragmentos funcionales, revelaron que Gpr126 es necesario para formar trabéculas normales. En embriones materno‑zigóticos stl47 —donde no llega Gpr126 sano ni del progenitor materno ni del paterno— muchos corazones se desarrollaron con trabéculas ausentes o muy reducidas. La N-cadherina, que en corazones sanos se concentra ordenadamente en los laterales de los cardiomiocitos de la pared compacta, apareció dispersa por la superficie celular. Esta desorganización sugiere que sin el NTF la adhesión célula–célula en la pared compacta se vuelve inestable, minando la base sobre la que deberían formarse las trabéculas.
Demasiada pared, poca identidad
Los mutantes st49, que todavía producen el NTF pero carecen del CTF, mostraron el problema opuesto. En lugar de trabéculas ausentes, sus corazones formaron una pared interna gruesa y multilaminar. Las capas extra no eran verdaderas trabéculas: las células permanecieron polarizadas como células de la pared compacta y no remodelaron sus contactos de N-cadherina hacia el patrón puntiforme típico de las células que forman crestas. Usando un reportero de actividad de Notch, el equipo encontró que estos corazones tenían una señalización Notch anormalmente alta en el miocardio. Se sabe que Notch alto mantiene a las células en la pared compacta e impide que se desprendan para formar trabéculas. De forma importante, cuando los investigadores reintrodujeron solo el CTF en células endocárdicas, las trabéculas reaparecieron y la actividad de Notch volvió hacia niveles normales, demostrando que la señalización del CTF es crucial para conferir a los cardiomiocitos identidad trabecular.
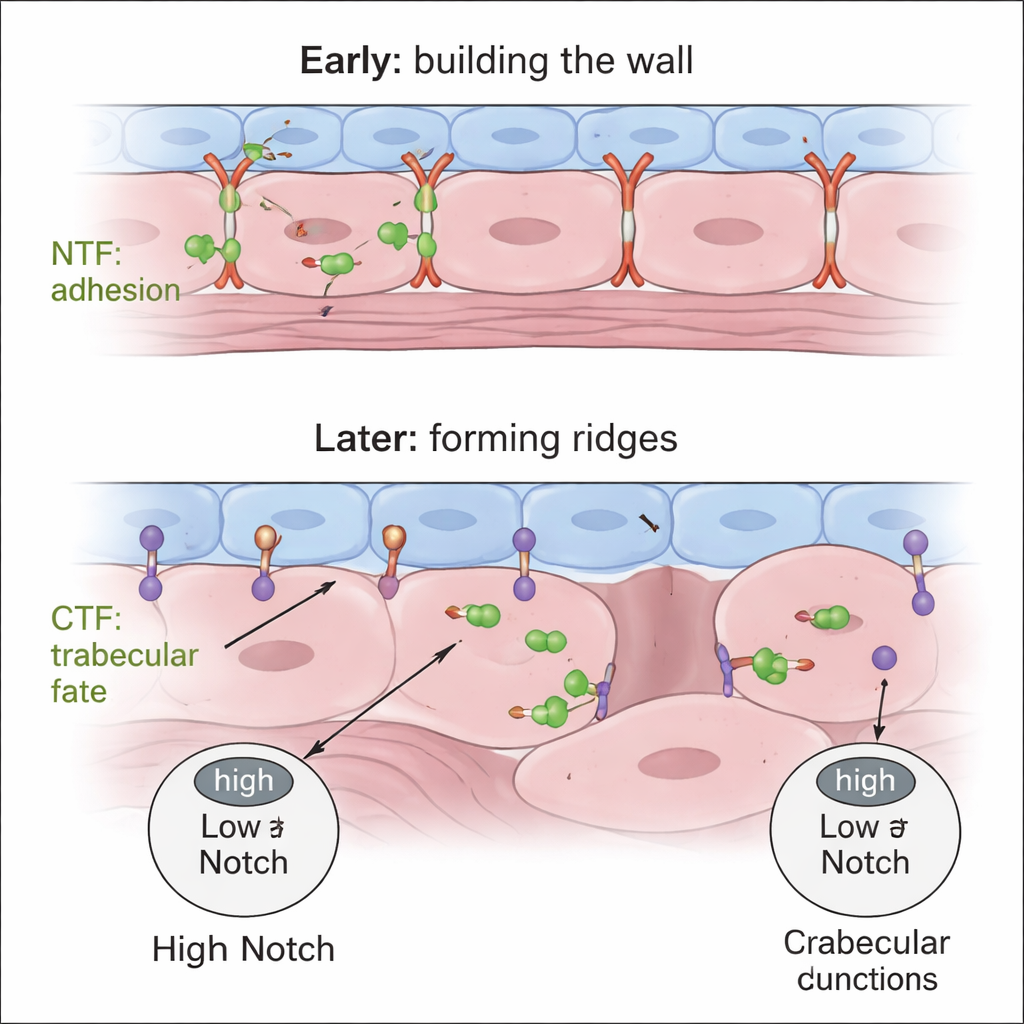
Equilibrar señales para un corazón sano
En conjunto, los hallazgos apoyan un modelo en dos pasos y con dos partes. Primero, el NTF secretado de Gpr126 ayuda a los cardiomiocitos de la pared compacta a mantener uniones estrechas y correctamente posicionadas, garantizando una pared sólida de una sola capa. Más tarde, el CTF —actuando desde células endocárdicas— modula la señalización Notch del miocardio para que solo algunos cardiomiocitos se despolaricen, aflojen sus uniones y protruyan hacia el interior para formar trabéculas, mientras que sus vecinos permanecen en la pared compacta. Si falta el NTF, la pared nunca se organiza bien; si falta el CTF, la pared crece en exceso y las células no adquieren la identidad trabecular. Este control dependiente del dominio sobre la arquitectura de la pared cardíaca destaca a Gpr126 como un posible nexo entre la adhesión celular, vías de señalización como Notch y enfermedades estructurales del corazón, y sugiere que afinar diferentes partes de un mismo receptor podría algún día ayudar a corregir defectos del desarrollo.
Cita: Srivastava, S., Gunawan, F., Vergarajauregui, S. et al. Adgrg6/Gpr126 is required for compact wall integrity and establishing trabecular identity during cardiac trabeculation. Nat Commun 17, 1484 (2026). https://doi.org/10.1038/s41467-026-69292-5
Palabras clave: trabeculación cardíaca, Gpr126, desarrollo del corazón, señalización Notch, modelo de pez cebra