Clear Sky Science · es
El impulsor genético de la encefalopatía necrosante aguda, RANBP2, regula la respuesta inflamatoria a la infección por virus de la influenza A
Cuando la gripe daña el cerebro
La mayoría de la gente piensa en la influenza como una semana de fiebre, tos y reposo. Sin embargo, en casos raros, sobre todo en niños, una infección gripal habitual puede convertirse de forma abrupta en un trastorno cerebral potencialmente mortal llamado encefalopatía necrosante aguda (ANE). Las familias y los médicos han sospechado durante mucho tiempo que los genes pueden influir en quién desarrolla esta complicación catastrófica. Este estudio revela cómo una única proteína guardiana celular, RANBP2, normalmente mantiene a raya al virus de la gripe y evita que la propia respuesta inflamatoria del organismo se descontrole.
Una complicación gripal rara pero devastadora
La ANE aparece de forma repentina tras una enfermedad febril, a menudo una influenza, y puede provocar con rapidez convulsiones, coma y daños neurológicos duraderos. Aproximadamente la mitad de los episodios de ANE conocidos en el mundo están vinculados al virus de la influenza A, en particular al subtipo H1N1. Los niños que heredan ciertos cambios en el gen RANBP2 tienen un riesgo mucho mayor, en una condición conocida como ANE1. Hasta ahora, sin embargo, los científicos no comprendían qué hace exactamente esta proteína durante la infección por la gripe, ni por qué su alteración haría que la inflamación cerebral fuera tan intensa.
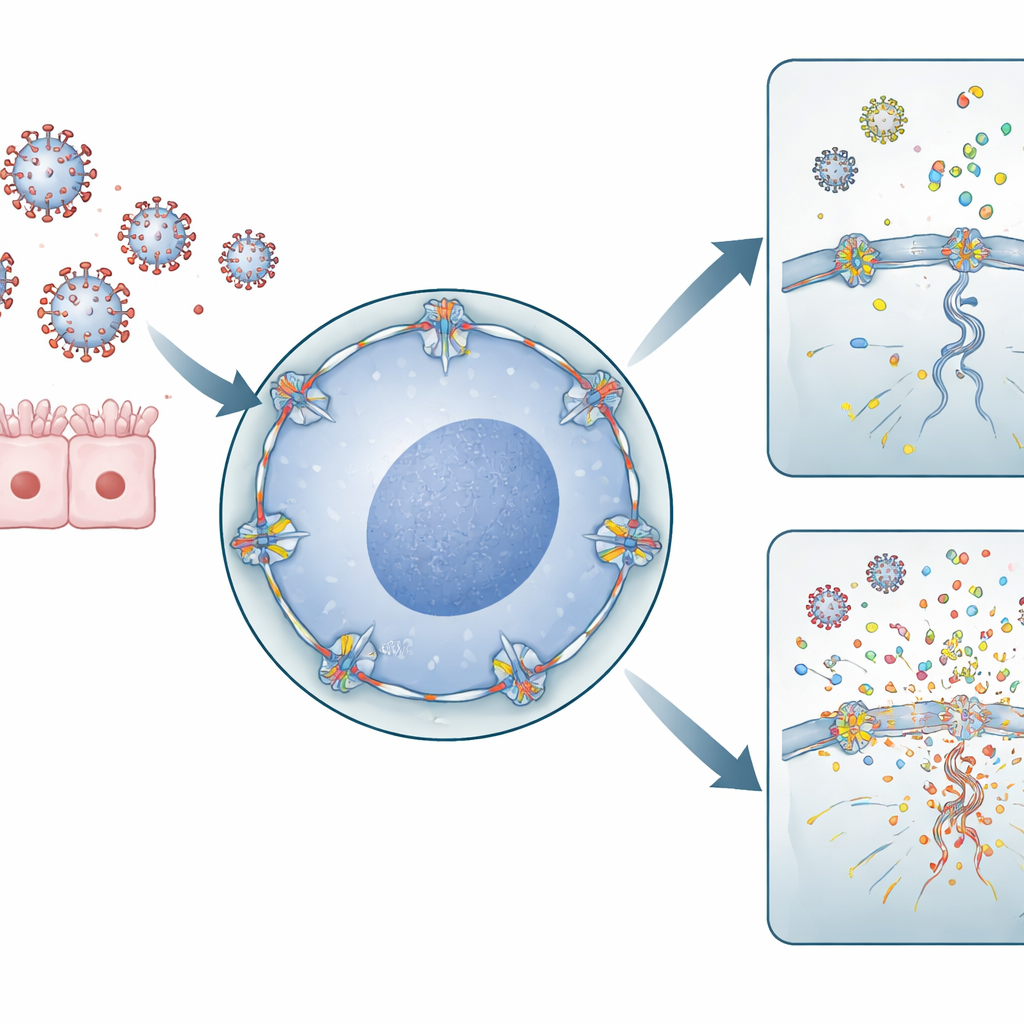
Puertas celulares y genomas virales
El virus de la influenza A tiene un estilo de vida inusual para un virus de ARN: debe entrar en el núcleo de la célula para copiar su material genético. Para ello pasa por los poros nucleares, grandes puertas en la envoltura nuclear que controlan el tráfico entre el núcleo y el citoplasma circundante. RANBP2 es un componente principal en el lado externo de estos poros. Los autores usaron células humanas derivadas del pulmón y células inmunitarias para reducir los niveles de RANBP2 o introducir la mutación vinculada a la ANE. Encontraron que cuando RANBP2 faltaba o estaba mal ubicado, los genomas gripales se replicaban más extensamente dentro del núcleo y los segmentos genéticos virales se exportaban al citoplasma de manera desequilibrada. Sorprendentemente, este exceso de ARN viral no produjo más partículas virales infecciosas, pero sí cambió dónde y cómo se acumulaba el material viral dentro de la célula.
Cuando los restos virales alimentan el sistema de alarma
El sistema inmunitario se basa en sensores moleculares que detectan fragmentos de ARN viral sueltos en el citoplasma como señales de peligro. El equipo demostró que, en células sin RANBP2 normal, se acumulaban en el citoplasma segmentos virales adicionales, creando exactamente los patrones que estos sensores reconocen. En las células derivadas del pulmón, esto desencadenó niveles más altos de moléculas inflamatorias como IL‑6 e IL‑1β. En macrófagos humanos primarios —células inmunitarias de primera línea de donantes de sangre— la pérdida de RANBP2 condujo a un notable aumento de quimiocinas proinflamatorias, incluidas CXCL8, CXCL10, CCL2, CCL3 y CCL4. Estos mensajeros químicos reclutan y activan células inmunitarias adicionales, amplificando la reacción global frente a la infección.
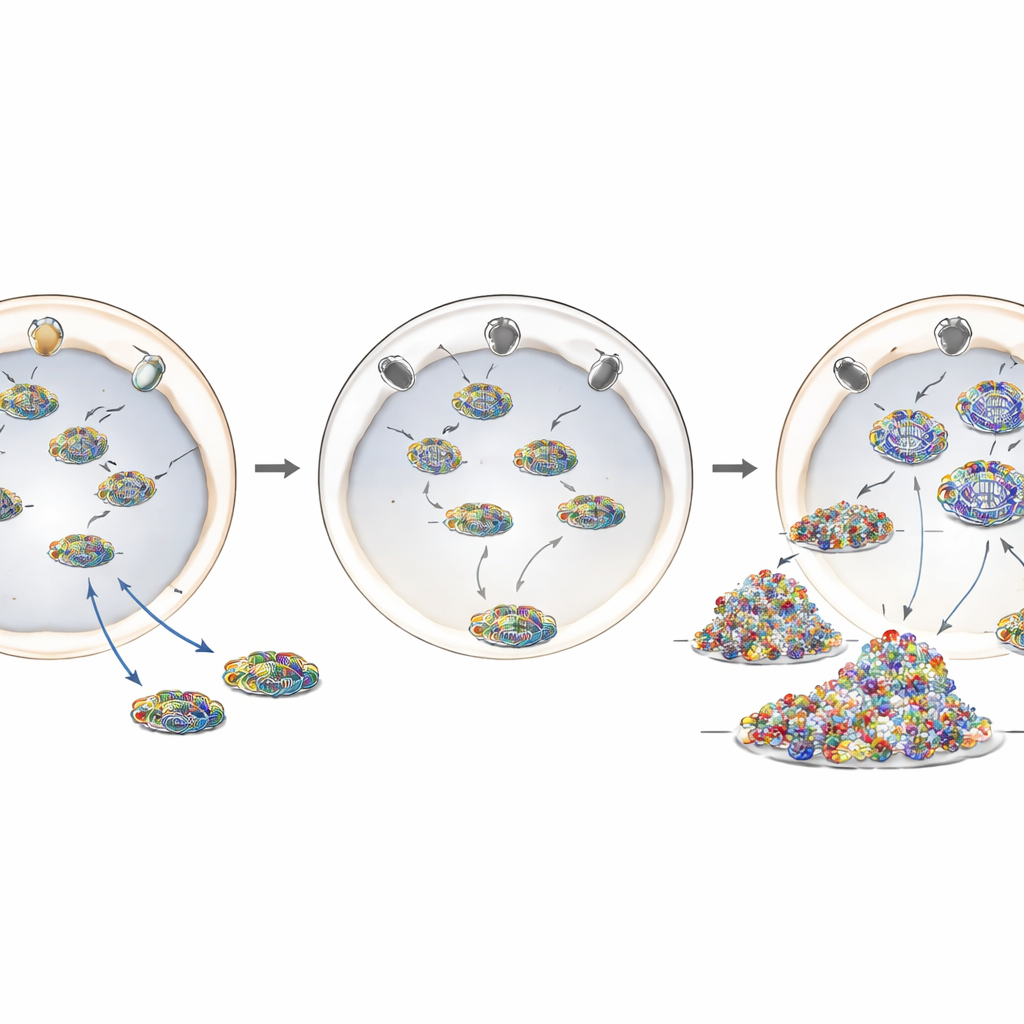
Una mutación de la enfermedad que desplaza a un guardián
Para modelar mejor la ANE1, los investigadores utilizaron la edición génica CRISPR‑Cas9 para introducir el cambio asociado a la enfermedad más común, T585M, en el gen humano RANBP2. En estas células editadas, los niveles de proteína RANBP2 eran en gran medida normales, pero su localización no lo era: en lugar de formar un borde brillante alrededor de la envoltura nuclear, gran parte de la proteína quedaba desplazada hacia el interior celular. Las células portadoras de esta mutación, ya fuera en una o en ambas copias del gen, se comportaron de forma muy parecida a las células con RANBP2 reducido. Favorecían una mayor replicación del genoma de la influenza, mostraban más material viral en el citoplasma y desencadenaban una respuesta inflamatoria más intensa tras la infección. Esto sugiere que posicionar correctamente a RANBP2 en los poros nucleares —más que su abundancia total— es crucial para su papel protector.
Por qué esto importa para los niños en riesgo
En conjunto, los hallazgos describen a RANBP2 como un guardián celular que ajusta finamente cómo el material genético de la influenza se mueve hacia dentro y fuera del núcleo. Cuando RANBP2 está ausente o mal localizado, el ARN viral se sobrerreplica y se exporta de forma caótica, llenando el citoplasma de restos moleculares que intensifican de manera notable la señalización inmune. Para la mayoría de los tejidos, esto puede significar un episodio de gripe más severo pero sobrevivible. En los niños vulnerables con ANE1, sin embargo, esta inflamación descontrolada —especialmente si alcanza el cerebro— puede ayudar a explicar el daño neurológico súbito y grave observado tras infecciones que por lo demás serían habituales. Entender esta vía podría orientar estrategias futuras para identificar temprano a los pacientes en riesgo y para adaptar tratamientos antiinflamatorios antes de que la respuesta inmune pase de protectora a destructiva.
Cita: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Palabras clave: influenza, encefalopatía necrosante aguda, RANBP2, hiperinflamación, poro nuclear