Clear Sky Science · es
Ensamblaje asimétrico de 4-alquil-butenolidos catalizado por una flavoenzima trifuncional en la biosíntesis de avenolida
Por qué nos importan los anillos pequeños en las bacterias
Muchos medicamentos que salvan vidas, desde antiparasitarios hasta protecciones para cultivos, dependen de un pequeño motivo químico llamado butenolido. Hoy esos anillos se fabrican mayoritariamente a partir de materias primas derivadas del petróleo mediante procesos industriales multi‑paso que consumen energía y generan residuos. Este estudio revela cómo las bacterias del suelo construyen uno de esos anillos: una hormona llamada avenolida que activa la producción de los medicamentos antiparasitarios estrella, las avermectinas. Comprender esta vía natural señala caminos más limpios y baratos para elaborar compuestos útiles y podría ayudar a descubrir nuevos antibióticos.
El anillo especial en el corazón de muchos fármacos
Los butenolidos son anillos compactos de cinco miembros que los químicos aprecian porque reaccionan de maneras versátiles y aparecen en numerosos productos naturales y fármacos modernos. Contribuyen a dar forma a moléculas con actividades anticancerígenas, antifúngicas, antiinflamatorias e insecticidas empleadas en medicina y agricultura. Sin embargo, las rutas sintéticas tradicionales para obtener estos anillos suelen requerir varios pasos controlados, catalizadores caros y materias primas petroquímicas. Esa combinación encarece el proceso y aumenta su impacto ambiental, lo que impulsa a los investigadores a buscar atajos biológicos que la naturaleza ya ha perfeccionado.
Una hormona bacteriana que enciende un fármaco estrella
En la bacteria del suelo Streptomyces avermitilis, la molécula que contiene butenolido avenolida actúa como una diminuta hormona. A concentraciones extremadamente bajas se une a una proteína reguladora y libera el freno molecular sobre los genes que sintetizan las avermectinas, potentes agentes que paralizan gusanos parásitos y algunos insectos. Trabajos genéticos previos habían sugerido que dos enzimas, llamadas SavA y SavB, construyen la avenolida, pero los pasos concretos eran desconocidos. El equipo trasladó primero los genes relevantes a un pariente más cooperativo, Streptomyces albidoflavus, y optimizó las condiciones de cultivo hasta que la cepa modificada produjo cantidades miligramo de avenolida pura —suficiente para diseccionar la vía en detalle. 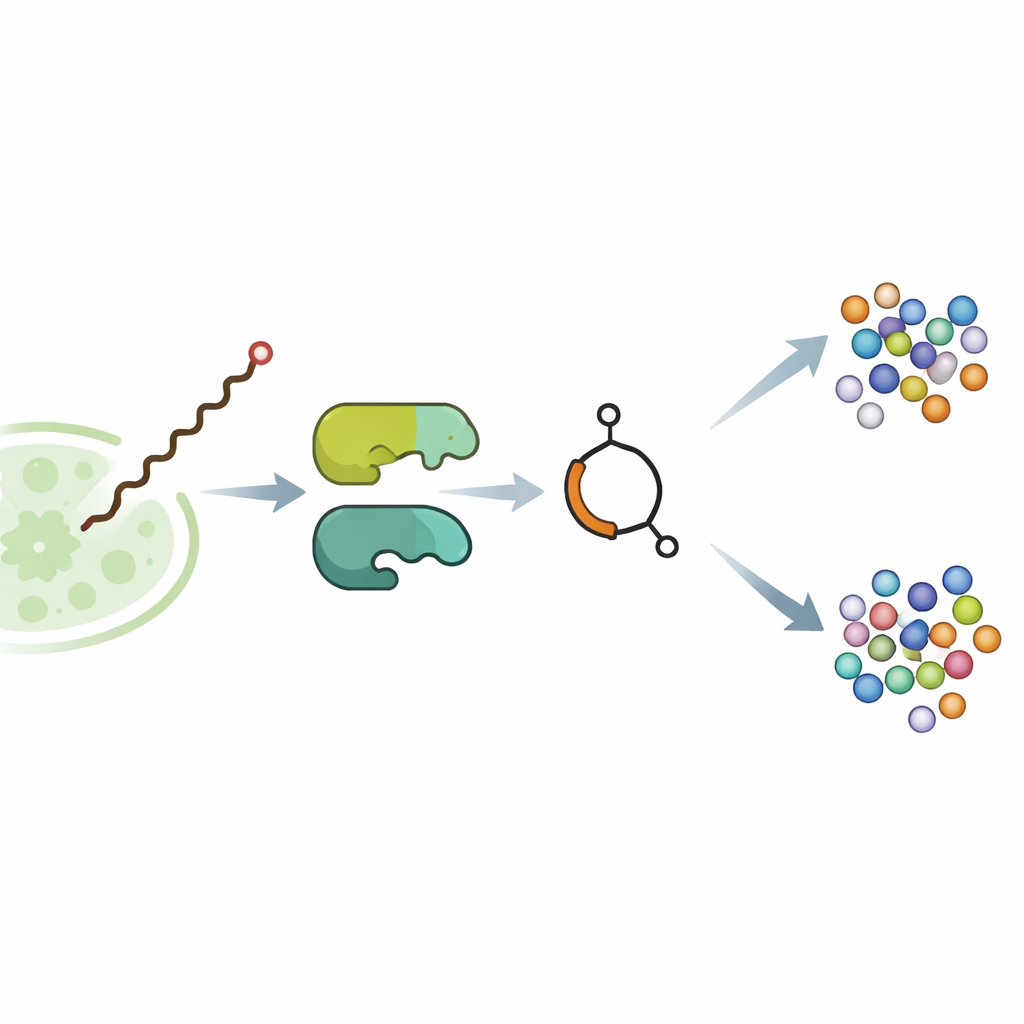
Una sola enzima que realiza tres tareas seguidas
La sorpresa central del estudio es SavA, una enzima que contiene flavina y que efectúa tres transformaciones químicas distintas sobre un fragmento inicial parecido a un ácido graso, proveniente del metabolismo celular normal. En reacciones de tubo de ensayo con sustratos miméticos cuidadosamente sintetizados, los investigadores mostraron que SavA primero extrae átomos de hidrógeno para introducir un doble enlace, luego añade un grupo que contiene oxígeno en una posición específica y finalmente promueve el cierre de la cadena formando el anillo butenolido. Experimentos isotópicos usando oxígeno gaseoso enriquecido con una forma más pesada confirmaron que el oxígeno del anillo procede directamente del aire. Modelado estructural y mutaciones dirigidas señalaron un único aminoácido como la base que inicia la reacción, y revelaron cómo la coenzima flavina ligada cicla entre las formas oxidadas y reducidas sin consumirse.
Una enzima finalizadora que afina la cadena lateral
Una vez SavA ha construido el andamiaje butenolídico quiral, SavB —una citocromo P450— se encarga de decorar la cadena carbonada adjunta. En presencia de sus socios redox y de un cofactor celular común, SavB realiza una serie precisa de oxidaciones en dos átomos de carbono adyacentes. El análisis temporal reveló dos moléculas intermedias: primero un producto mono‑hidroxilado, luego una forma cetónica, antes de que aparezca la avenolida completamente funcional. Mediciones por resonancia magnética nuclear confirmaron las posiciones y las disposiciones tridimensionales de estos nuevos grupos. El trabajo muestra que SavB introduce estos átomos de oxígeno en un orden definido y con estricto control de orientación, característica importante para la actividad biológica de la hormona. 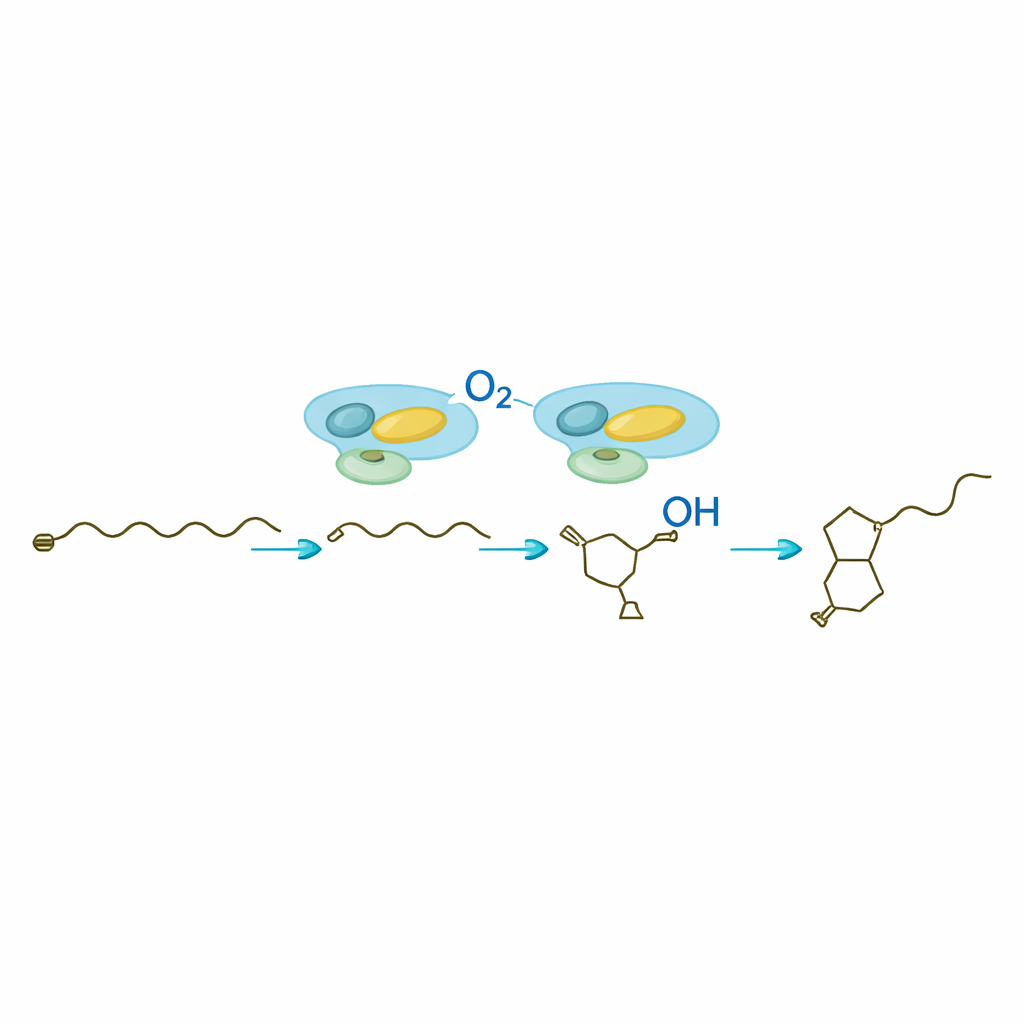
Lecciones de química verde a partir de enzimas bacterianas
En conjunto, SavA y SavB convierten un bloque de construcción derivado de ácidos grasos ordinarios en una molécula señalizadora finamente afinada usando únicamente el oxígeno del aire y auxiliares celulares estándar. A diferencia de muchos procesos industriales, SavA no necesita agentes reductores adicionales ni reactivos sacrificiales; su cofactor de flavina simplemente transporta electrones mientras el propio sustrato proporciona la fuerza impulsora. Los autores destacan a SavA como un nuevo tipo de flavoenzima polivalente con un fuerte potencial como biocatalizador para la fabricación sostenible de butenolidos y motivos relacionados. En términos prácticos, aprovechar o diseñar enzimas así podría permitir algún día a fábricas —o microbios diseñados— producir fragmentos de fármacos y productos agrícolas importantes a partir de materias primas renovables en condiciones suaves, reduciendo tanto el coste como la huella ambiental.
Cita: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Palabras clave: biosíntesis de butenolidos, flavoenzima SavA, hormona avenolida, biocatálisis, señalización de Streptomyces