Clear Sky Science · es
Degradadores de la proteína de la cápside del virus del dengue muestran farmacología diferenciada respecto a los inhibidores de cápside
Volver la coraza del virus contra sí misma
La fiebre del dengue infecta a cientos de millones de personas cada año, pero los médicos aún carecen de fármacos antivirales confiables para tratarla. Este estudio explora una vía nueva para desarmar al virus del dengue destruyendo uno de sus bloques constructivos más importantes dentro de las células infectadas, en lugar de limitarse a bloquear su actividad. El trabajo muestra que moléculas cuidadosamente diseñadas pueden etiquetar una proteína viral clave para su eliminación por el propio sistema de gestión de desechos de la célula, reduciendo la producción viral y mermando su capacidad para ocultarse de nuestras defensas inmunitarias.
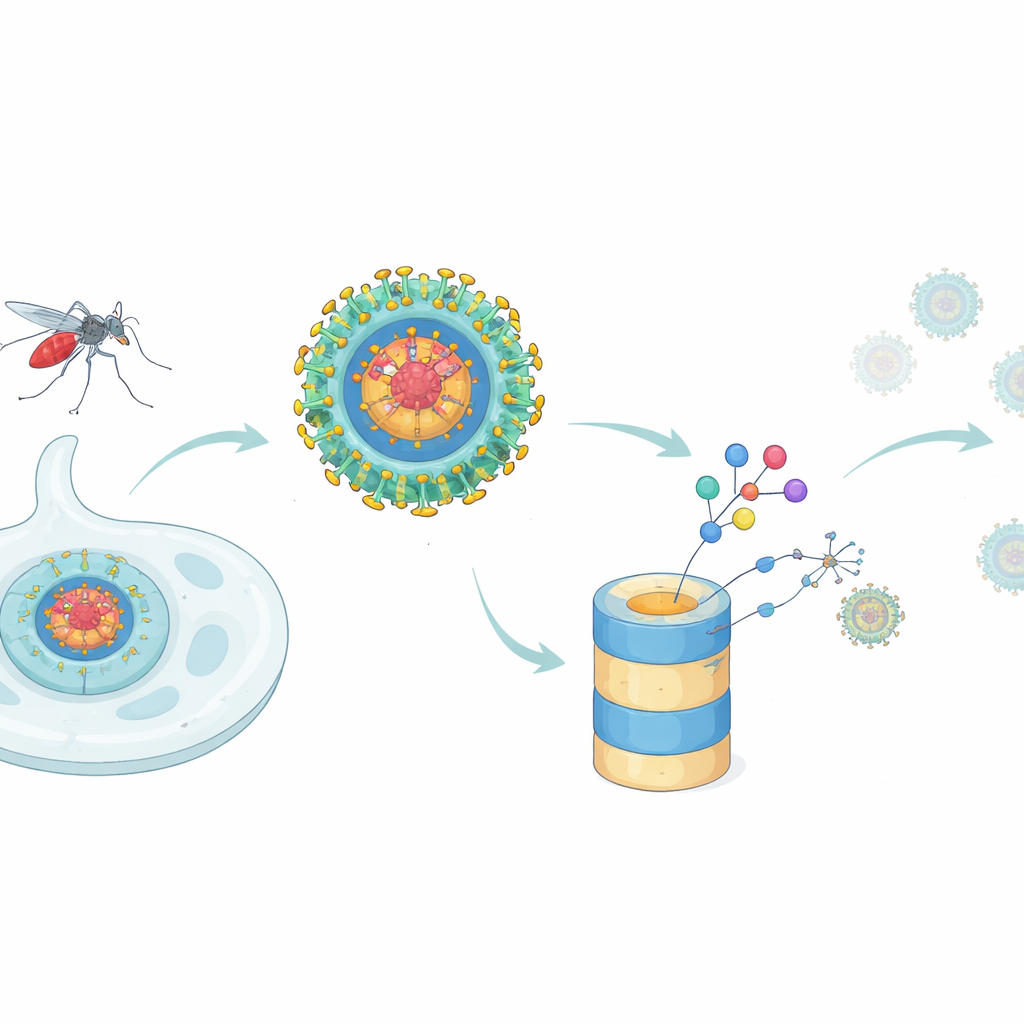
Una táctica nueva para detener el dengue
La mayoría de los antivirales actúan como tapones en una máquina: se sientan en un punto funcional de una proteína viral e intentan bloquearla. Ese enfoque tiene dificultades cuando una sola proteína viral realiza muchas funciones diferentes, o cuando pequeñas mutaciones debilitan el anclaje del fármaco. La proteína de la cápside del dengue es un ejemplo paradigmático. Forma la cubierta central que empaqueta el material genético viral en nuevas partículas, pero también interfiere con la célula huésped al interactuar con muchas proteínas humanas y al atenuar la respuesta de interferón del organismo, una alarma antiviral de primera línea. Los autores se preguntaron si un concepto más reciente de fármacos—la degradación dirigida de proteínas—podría ir más allá de los inhibidores clásicos al eliminar realmente la proteína de la cápside de las células infectadas.
Diseñando un “cazarrecompensas” molecular
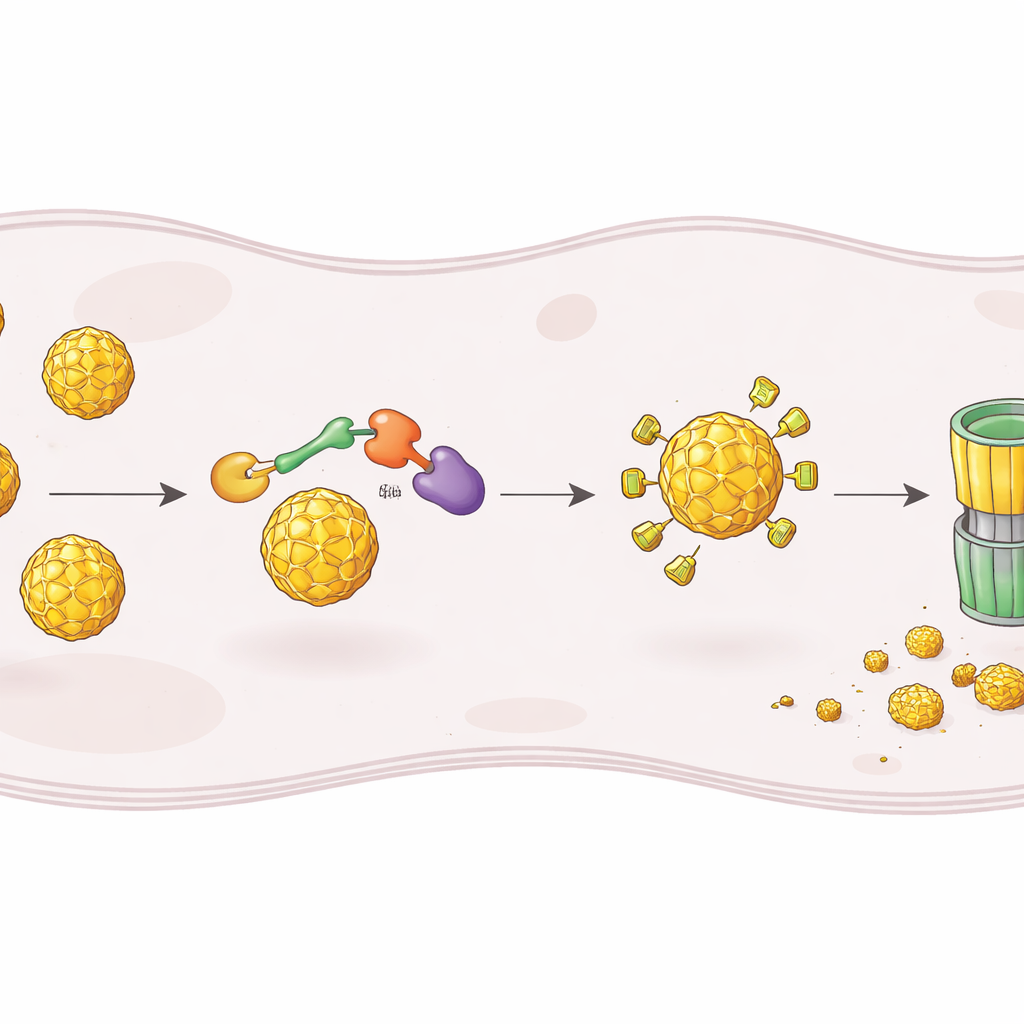
Para construir un degradador así, los investigadores partieron de ST148, una pequeña molécula conocida que se une a la cápside del dengue e interfiere con el ensamblaje de nuevas partículas virales. Enlazaron químicamente ST148 a un segundo módulo que recluta a un complejo enzimático humano responsable de etiquetar proteínas para su destrucción. Las moléculas quiméricas resultantes, llamadas PROTACs, están diseñadas para agarrar la cápside por un extremo y un ligador E3 por el otro, acercándolos para que la cápside pueda ser marcada con ubiquitina y dirigida al proteasoma celular, el principal trituradora de proteínas. Al probar muchas longitudes de enlace y grupos reclutadores de ligasa, identificaron un compuesto destacado, denominado RPG‑01‑132, que redujo de forma fiable los niveles de cápside en células infectadas de manera dependiente de la forma CRBN de la ligasa y del funcionamiento normal del proteasoma.
Deteniendo la producción viral y la evasión inmune
Una vez que tuvieron un degradador funcional, el equipo examinó qué efecto tenía realmente sobre la infección por dengue. En células derivadas del hígado infectadas con dengue, RPG‑01‑132 provocó una fuerte caída en el número de virus infecciosos liberados, a concentraciones en las que solo disminuía parcialmente el nivel total de cápside. De forma importante, otras proteínas virales y el ARN viral permanecieron sin cambios, lo que muestra que el compuesto no estaba simplemente intoxicando la replicación en general, sino actuando específicamente a través de la pérdida de cápside. La microscopía electrónica ofreció una lectura visual: las células tratadas con el inhibidor original ST148 acumulaban pilas de partículas virales parcialmente formadas en el retículo endoplásmico, coherente con un bloqueo en el ensamblaje, mientras que las células tratadas con el degradador mostraban casi ninguna partícula viral visible. El degradador también alivió la capacidad de la cápside para silenciar la señalización de interferón‑β en un sistema reportero, lo que sugiere que el papel no estructural de la cápside en desactivar la inmunidad innata puede revertirse degradándola.
Superar la diversidad viral y la resistencia a fármacos
El virus del dengue existe en cuatro serotipos principales que difieren en su respuesta a los inhibidores dirigidos a la cápside, y la resistencia puede surgir por mutaciones puntuales. Los autores compararon el degradador con ST148 en cepas representativas de los cuatro serotipos y frente a un virus que porta una mutación (S34L en la cápside) que anteriormente se había mostrado capaz de hacer ineficaz a ST148. Como era de esperar, ST148 funcionó mejor en un serotipo y perdió actividad frente al mutante resistente. RPG‑01‑132, en contraste, mostró una potencia antiviral similar entre todos los serotipos y retuvo actividad contra el mutante S34L, al tiempo que seguía actuando mediante la misma vía de degradación dependiente de CRBN. Esto ilustra una ventaja clave de la farmacología “dirigida por eventos”: el degradador no necesita permanecer fuertemente unido a cada molécula de cápside en todo momento, siempre que pueda desencadenar suficientes eventos de degradación para inclinar la balanza.
Qué significa esto para futuros tratamientos del dengue
Este estudio demuestra que la proteína de la cápside del dengue puede atacarse no solo como un componente estructural del virus sino como un centro removible que sostiene múltiples pasos de la infección y la evasión inmune. Al convertir un inhibidor tradicional en un degradador, los investigadores crearon un compuesto que bloquea la producción viral, revierte parte de la supresión de la inmunidad innata por el virus y sigue siendo eficaz frente a cepas virales diversas y a una mutación de resistencia conocida. RPG‑01‑132 necesitará optimización—mejor entrada en células, mayor actividad en modelos animales y controles de seguridad cuidadosos—pero proporciona una prueba de concepto convincente. Más en general, el trabajo sugiere que secuestrar la propia maquinaria de eliminación de la célula podría abrir nuevas vías hacia fármacos antivirales más difíciles de eludir por los virus y capaces de neutralizar proteínas con múltiples funciones dentro de las células infectadas.
Cita: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Palabras clave: virus del dengue, proteína de la cápside, degradación dirigida de proteínas, diseño de fármacos antivirales, PROTACs