Clear Sky Science · es
Activación cooperativa de aniones en un centro de cobalto mediante apareamiento iónico y diseño de ligandos
Por qué importan los pequeños compañeros alrededor de los metales
Los químicos suelen centrarse en el “actor” principal de una reacción: un átomo de metal que ayuda a romper y formar enlaces. Pero este artículo muestra que los compañeros discretos que lo rodean, invisibles a simple vista, pueden cambiar por completo lo que hace el metal. Mediante el modelado cuidadoso del espacio alrededor de un átomo de cobalto, los autores revelan cómo dos aniones casi intercambiables, a menudo tratados como meros espectadores en química y baterías, pueden conducir a resultados marcadamente diferentes. 
Construyendo un bolsillo a medida alrededor del cobalto
Los investigadores diseñaron un armazón orgánico en forma de jaula llamado Py4Im que envuelve estrechamente un ion de cobalto. Este armazón está compuesto por varios anillos de piridina enlazados y una unidad de imidazolidina, que en conjunto crean una cavidad rígida en forma de cuenco que contiene un único grupo N–H. Esa pequeña cavidad es “prótica”, es decir, puede formar enlaces de hidrógeno, y apunta en una dirección específica, como una diminuta esclusa de atraque para aniones entrantes. Cuando el cobalto se monta con este ligando, el resultado es una familia de complejos cargados positivamente cuya forma global y bolsillo interior permanecen constantes mientras se puede intercambiar el contraión —la pareja cargada negativamente—. Esto convierte al sistema en una plataforma ideal para observar cómo se comportan diferentes aniones en el mismo entorno controlado.
Dos aniones parecidos, dos comportamientos muy distintos
El equipo comparó dos aniones de uso habitual, tetrafluoroborato (BF4−) y hexafluorofosfato (PF6−), ampliamente empleados como llamados aniones débilmente coordinantes. Son populares porque suelen mantenerse a distancia de los centros metálicos, ayudando a estabilizar especies muy cargadas sin implicarse directamente. Sorprendentemente, dentro de la cavidad Py4Im no se comportan igual. Bajo condiciones suaves, PF6− dona un ion fluoruro al cobalto, rompiendo un fuerte enlace P–F y formando un complejo bien definido de cobalto–fluoruro. En contraste, BF4−, que suele considerarse el más “frágil” de los dos, se niega a ceder fluoruro en el mismo entorno. En lugar de ello, se acomoda en una disposición estable unida al centro de cobalto sin completar el paso de ruptura del enlace.
Observando cómo los iones se aparean y se mueven
Para entender estos comportamientos contrastantes, los autores emplearon una combinación de técnicas de RMN de alta resolución y cálculos cuántico‑químicos. Experimentos de RMN de difusión midieron la rapidez con que las especies positivas y negativas se desplazan en solución, lo que revela cuán fuertemente están apareadas. Estas mediciones mostraron que BF4− forma un par iónico más cercano y persistente con el complejo de cobalto que PF6−. La cavidad Py4Im posiciona al anión directamente debajo del anillo de imidazolidina, donde enlaces de hidrógeno del N–H y grupos C–H próximos lo mantienen en su lugar. Los cálculos por ordenador confirmaron que este apareamiento más fuerte y direccional con BF4− estabiliza tanto el estado inicial que romper el enlace B–F resulta ligeramente desfavorable, aunque ese enlace sea intrínsecamente más débil que el P–F en PF6−. PF6−, al aparearse de forma más laxa, puede acercarse, transferir fluoruro al cobalto y desprenderse como PF5, conduciendo a un complejo de cobalto portador de fluoruro que es termodinámicamente accesible. 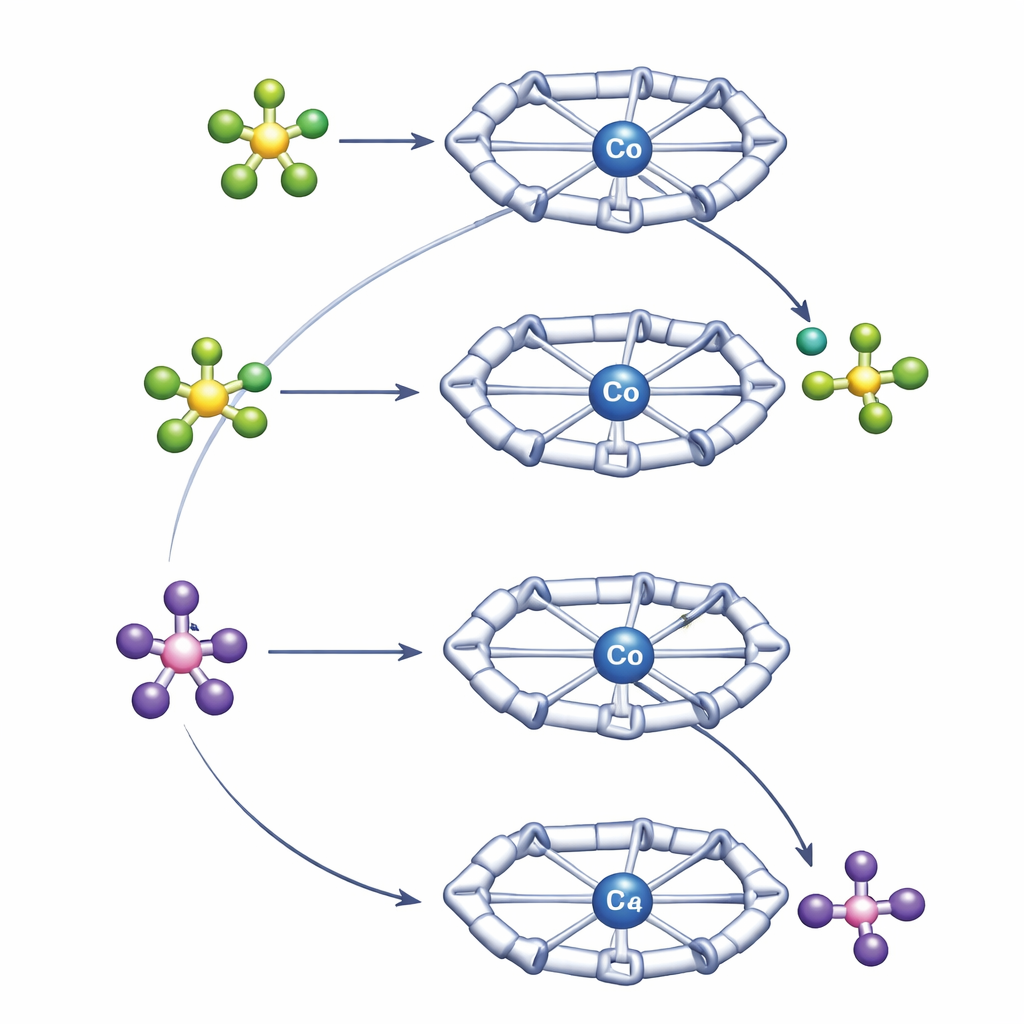
Convertir un fluoruro ligado en una herramienta útil
Una vez formado, el complejo cobalto–fluoruro no es un callejón sin salida. Los autores muestran que se comporta como una fuente nucleofílica de fluoruro —en términos sencillos, puede entregar fluoruro a socios cargados positivamente o pobres en electrones. En solución, esta especie de cobalto–fluoruro transfiere limpiamente fluoruro a centros carbonosos reactivos, a átomos de silicio en clorosilanos y a cloruros de acilo, generando fluoruros orgánicos mientras el complejo de cobalto vuelve a su forma cloruro o se enlaza con el nuevo socio. En un giro ingenioso, el equipo también demuestra que BF4− puede ser inducido a ceder fluoruro si en el sistema está presente una base separada que “capture” el fragmento BF3 que queda atrás. Esto convierte la vía normalmente reacia de BF4− en una que también produce el mismo producto de cobalto–fluoruro.
Qué significa esto para diseñar catalizadores más inteligentes
Para un no especialista, el mensaje clave es que iones considerados antaño sales de fondo inertes pueden, en realidad, dirigir reacciones químicas de maneras potentes. Al esculpir un bolsillo preciso alrededor de un centro metálico y controlar cuán firmemente se aparean los aniones con él, los autores invirtieron la reactividad esperada de dos especies casi idénticas. PF6−, normalmente visto como muy robusto, se convierte en la fuente de fluoruro más fácil, mientras que BF4− queda bloqueado por un apareamiento más fuerte a menos que el sistema reciba ayuda externa. Este trabajo ofrece un plano para usar conjuntamente el diseño de ligandos y la elección del contraión para ajustar la reactividad de un complejo metálico —una idea que podría influir en campos que van desde la catálisis homogénea hasta el diseño de electrolitos para baterías avanzadas, donde los “compañeros silenciosos” en solución pueden estar lejos de ser pasivos.
Cita: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Palabras clave: complejos de cobalto, aniones débilmente coordinantes, transferencia de fluoruro, apareamiento iónico, diseño de ligandos