Clear Sky Science · es
El sulfuro de molibdeno metálico cataliza redes protometabólicas de reacción del dióxido de carbono en condiciones extremas
Cómo las rocas pudieron poner en marcha la química de la vida
Mucho antes de que las células vivas desarrollaran enzimas, la Tierra necesitaba mecanismos para transformar gases simples como el dióxido de carbono en las moléculas orgánicas de las que depende la vida. Este estudio explora si ciertos minerales que se encuentran de forma natural, similares a los presentes cerca de fuentes termales submarinas, podrían haber actuado como “motores químicos” primitivos. Al demostrar que una forma metálica de sulfuro de molibdeno puede convertir el dióxido de carbono en una sorprendentemente rica red de compuestos orgánicos, el trabajo ofrece un escenario concreto sobre cómo pudo empezar la química central de la vida en un planeta sin vida.

Chimeneas calientes y motores químicos ocultos
La vida moderna funciona gracias a redes intrincadas de reacciones que movilizan el carbono a través de células y ecosistemas. Estas redes dependen de proteínas llamadas enzimas, que a su vez son producto de la evolución. La gran pregunta es qué existió antes. Los autores se centraron en las chimeneas hidrotermales—estructuras naturales de agua caliente en el fondo del océano ricas en sulfuros metálicos y gas hidrógeno—como escenarios probables para la química carbonada más temprana. En esos lugares, agua caliente y presurizada entra en contacto con rocas que contienen metales como hierro, níquel y molibdeno. Experimentos previos mostraron que algunos de estos metales pueden transformar el dióxido de carbono en pequeños compuestos orgánicos, pero por lo general solo a lo largo de fragmentos de las vías metabólicas, no en redes completas.
Un mineral que imita a las enzimas antiguas
El equipo se centró en una forma particular de sulfuro de molibdeno, denominada fase 1T′, cuya disposición atómica imita los centros metal–azufre presentes en enzimas modernas que procesan el dióxido de carbono. Bajo altas temperaturas y presiones en agua, con hidrógeno como combustible, este mineral catalizó la conversión de dióxido de carbono disuelto (modelado como bicarbonato) en una gama inesperadamente amplia de ácidos orgánicos. Variando cuidadosamente la temperatura, el tiempo de reacción y la presión del gas, y analizando los productos mediante cromatografía, espectrometría de masas y RMN, identificaron 32 intermediarios y productos finales diferentes que surgían de la misma fuente simple de carbono.
Reconstruir las rutas centrales del carbono de la vida sin enzimas
Esos 32 compuestos no son aleatorios. Muchos son las mismas moléculas que se encuentran en el corazón del metabolismo moderno—como acetato, piruvato, oxaloacetato, succinato y alfa-cetoglutarato. En conjunto, se corresponden con cinco rutas principales de fijación de carbono utilizadas por microbios contemporáneos: la vía acetil–CoA y variantes del ciclo de Krebs y bucles relacionados. En los experimentos, estas rutas aparecieron como una red interconectada: el acetato unía varios ciclos; moléculas más grandes se descomponían y volvían a formarse; e intermedios clave desaparecían y reaparecían según cambiaban las condiciones. La producción de ácidos con varios carbonos alcanzó alta eficiencia, con hasta aproximadamente un 70% del carbono convertido terminando en moléculas que contienen dos o más carbonos. La red de reacciones también mostró oscilaciones en las que las cantidades de ciertos productos aumentaban y disminuían con el tiempo, evocando el comportamiento dinámico de los sistemas químicos vivos.
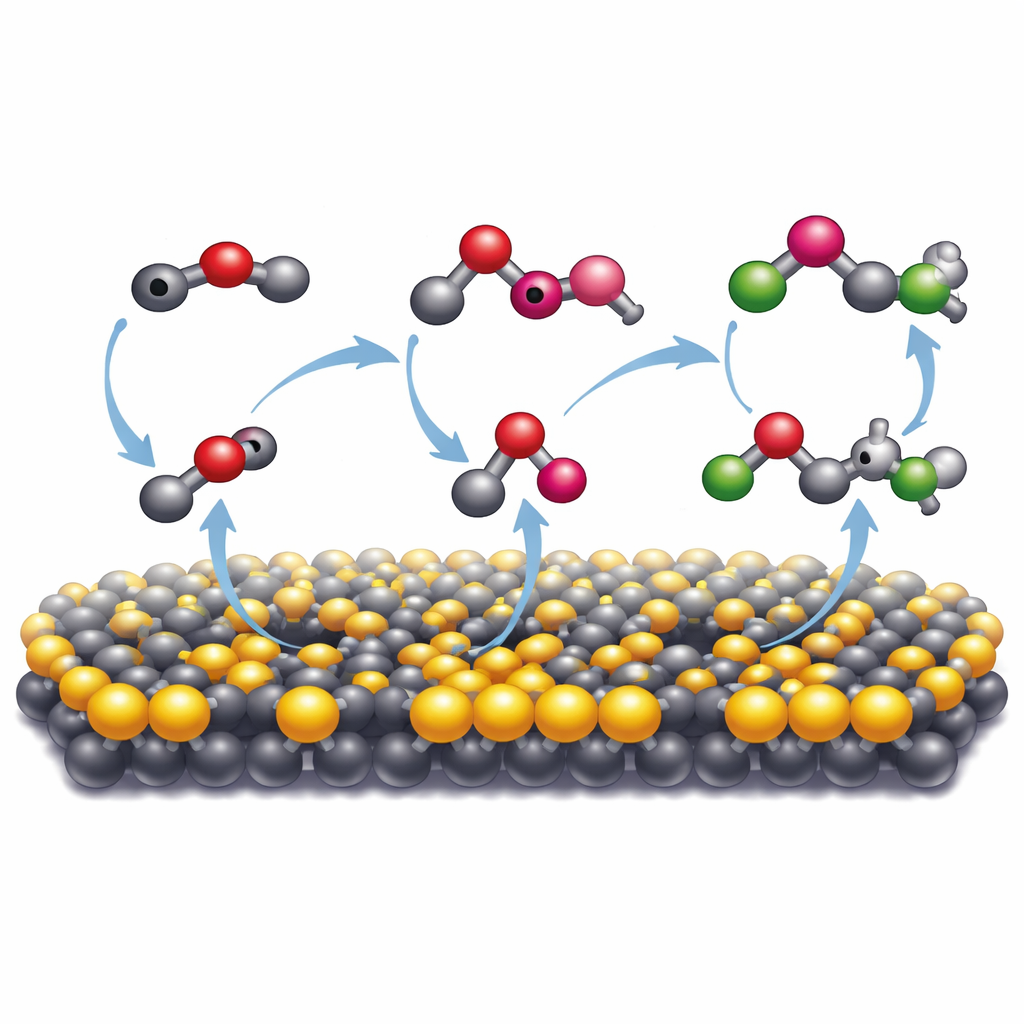
Cómo el mineral hace que los átomos de carbono se unan
Para entender por qué este mineral en particular era tan efectivo, los investigadores lo compararon con una forma más común de sulfuro de molibdeno que tiene una estructura atómica distinta. Solo la forma metálica y distorsionada—con muchas vacancias de azufre—impulsó la formación extensa de orgánicos más grandes. Técnicas espectroscópicas revelaron que en esta superficie, el monóxido de carbono derivado del dióxido de carbono se une con fuerza y se reduce aún más a fragmentos altamente reactivos, o radicales. Estos radicales se estabilizan lo justo en la superficie mineral para encontrarse entre sí y formar nuevos enlaces carbono–carbono. Mediciones de espín electrónico confirmaron la presencia de tales radicales, y la adición de un compuesto “trampa” de radicales suprimió drásticamente los productos multicarábono. Simulaciones por computador respaldaron este panorama, mostrando que las vacancias de azufre y la estructura electrónica alterada de la fase 1T′ facilitan que la superficie done electrones y acerque fragmentos de carbono para que puedan combinarse.
De la química de las piedras al primer metabolismo
En conjunto, estos hallazgos sugieren que ciertos sulfuros metálicos en la Tierra primitiva podrían haber sostenido una química carbonada compleja y autoorganizada mucho antes de que existieran las enzimas. En entornos de chimeneas hidrotermales, donde fluidos calientes ricos en hidrógeno se encuentran con dióxido de carbono y rocas portadoras de metales, un mineral como el sulfuro de molibdeno 1T′ podría haber convertido de forma continua el carbono inorgánico en una red de rutas orgánicas interconectadas que recuerdan a los ciclos metabólicos modernos. Para un público no especialista, el mensaje clave es que la química central de la vida quizá no necesitó de la vida para comenzar: en las condiciones adecuadas, rocas simples, agua y gas pueden construir espontáneamente muchas de las mismas moléculas y circuitos de reacción que las células vivas siguen utilizando hoy.
Cita: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Palabras clave: origen de la vida, química prebiótica, chimeneas hidrotermales, fijación de carbono, sulfuro de molibdeno