Clear Sky Science · es
Modelos de aprendizaje profundo interpretables y generativos explican motivos intrínsecamente desordenados que separan fases
Por qué importan los segmentos pequeños de proteínas
Dentro de cada una de nuestras células, moléculas vitales a menudo se agrupan en gajos parecidos a gotas llamados condensados biomoleculares. Estas gotas ayudan a organizar la química sin las paredes de una membrana, modulando cómo se activan los genes, cómo se transmiten las señales y cómo las células responden al estrés. Muchas de estas gotas se forman por tramos flexibles de proteínas conocidos como regiones intrínsecamente desordenadas. Sin embargo, los biólogos todavía encuentran difícil identificar los fragmentos cortos de la secuencia que realmente hacen que estas gotas se formen. Este estudio presenta un marco de aprendizaje profundo, PhaSeMotif, que puede tanto encontrar estos segmentos clave como diseñar otros nuevos, ofreciendo a los investigadores una forma potente de sondear y reconfigurar las gotas celulares.
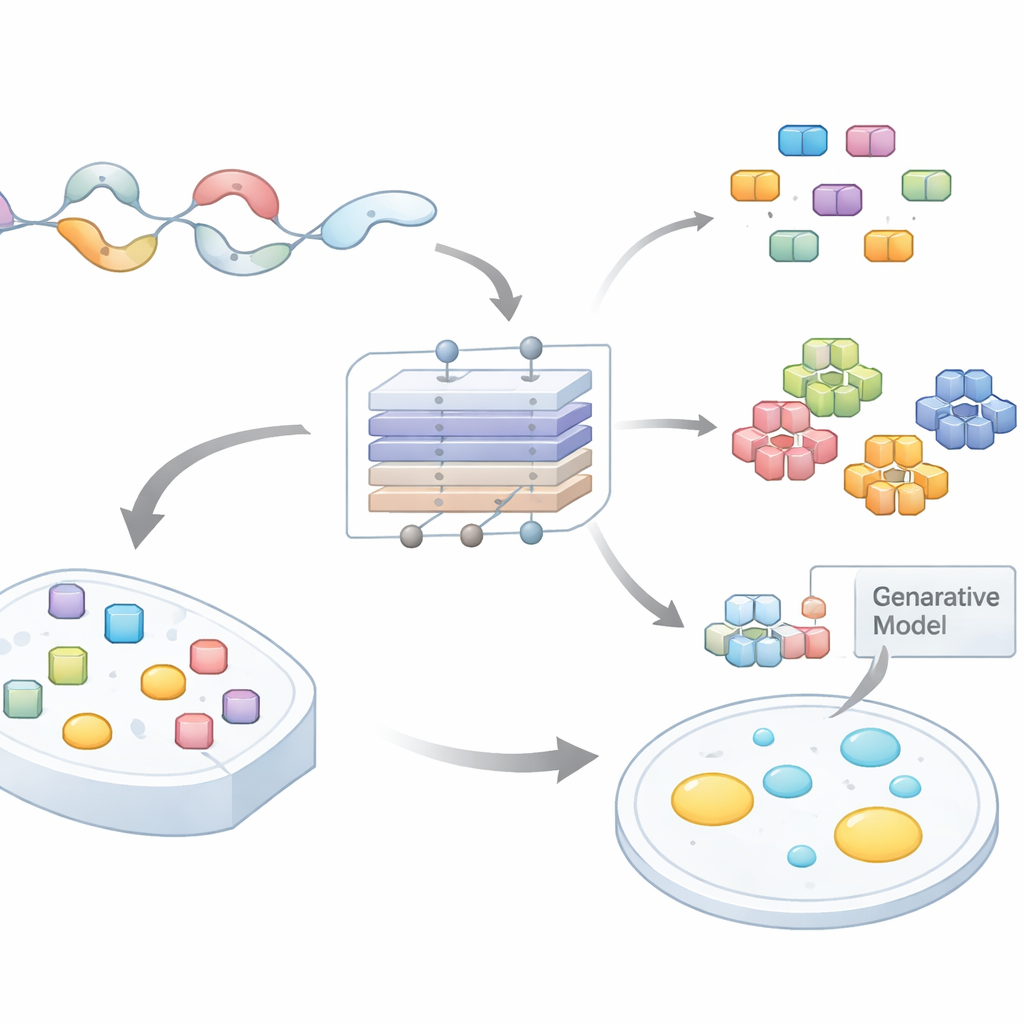
De colas proteicas desordenadas a ideas comprobables
Muchas proteínas contienen colas largas y flexibles que no se pliegan en formas fijas. Estas regiones desordenadas están enriquecidas en ciertos aminoácidos y a menudo contienen patrones repetidos o motivos cortos. Un número creciente de trabajos muestra que dichos motivos impulsan la condensación al permitir muchas interacciones débiles a la vez. Sin embargo, escanear proteomas enteros para encontrar qué tramos cortos importan y por qué ha sido un cuello de botella importante. Las herramientas computacionales existentes normalmente evalúan proteínas completas o regiones grandes, ofreciendo poca orientación sobre dónde mutar o qué probar en el laboratorio. Los autores se propusieron construir un modelo que predijera no solo si una región desordenada puede formar gotas, sino también qué subsecuencias exactas están realizando el trabajo principal.
Un mapa de aprendizaje profundo de motivos que promueven gotas
El equipo compiló grandes conjuntos de datos de regiones desordenadas en varias especies y las etiquetó según la probabilidad de que sus proteínas anfitrionas sufrieran separación de fases. Luego entrenaron una red neuronal basada en atención, PhaSeMotif, que toma una secuencia de aminoácidos de cualquier longitud y devuelve una puntuación de formación de gotas. De forma crucial, la red usa una combinación de capas convolucionales y mecanismos de atención para evaluar cuánto contribuye cada ventana corta de la secuencia a esa puntuación. Al rastrear hacia atrás a través del modelo (usando técnicas similares a la retropropagación guiada), los autores extrajeron parches de alta importancia—motivos cortos a menudo de menos de 20 residuos—que el modelo consideró esenciales para la formación de gotas.
Poner las predicciones a prueba en células vivas
Para comprobar si estos motivos realmente importaban, los investigadores recurrieron a un sistema activado por luz en células humanas. Fusionaron regiones desordenadas predichas como formadoras de gotas a un módulo de oligomerización sensible a la luz y a una etiqueta fluorescente. Bajo luz azul, estos constructos se condensaron rápidamente en puntos brillantes, informando sobre la separación de fases en tiempo real. El equipo luego eliminó quirúrgicamente motivos individuales reemplazándolos por conectores neutrales y flexibles de la misma longitud. En el 82% de las 17 secuencias alteradas probadas, la formación de gotas se debilitó drásticamente o desapareció por completo, mientras que las mutaciones de control fuera de los segmentos identificados por PhaSeMotif a menudo tuvieron poco efecto. Importante, muchos de estos motivos clave coincidían con sitios donde se sabe que mutaciones vinculadas a enfermedades alteran la condensación, subrayando su relevancia biológica.
Descubrir un vocabulario de tipos de motivos
Con más de 17 000 motivos en mano, los autores se preguntaron si existían “sabores” comunes de segmentos que promueven gotas. Analizaron la composición y el patrón de aminoácidos, y luego agruparon los motivos en nueve clústeres. Algunos clústeres eran ricos en residuos aromáticos y glicina, consistentes con interacciones adhesivas π–π y catión–π. Otros contenían parches separados de cargas positivas y negativas, favoreciendo la atracción electrostática y la partición selectiva hacia condensados particulares. Clústeres adicionales estaban dominados por prolina y glicina, que aportan flexibilidad, o por largas repeticiones de glutamina que pueden formar redes densas de enlaces de hidrógeno. Diferentes compartimentos celulares y tipos de condensados mostraron mezclas características de estas clases de motivos, lo que sugiere que la composición de los motivos ayuda a determinar dónde y con qué socios una proteína se condensará.
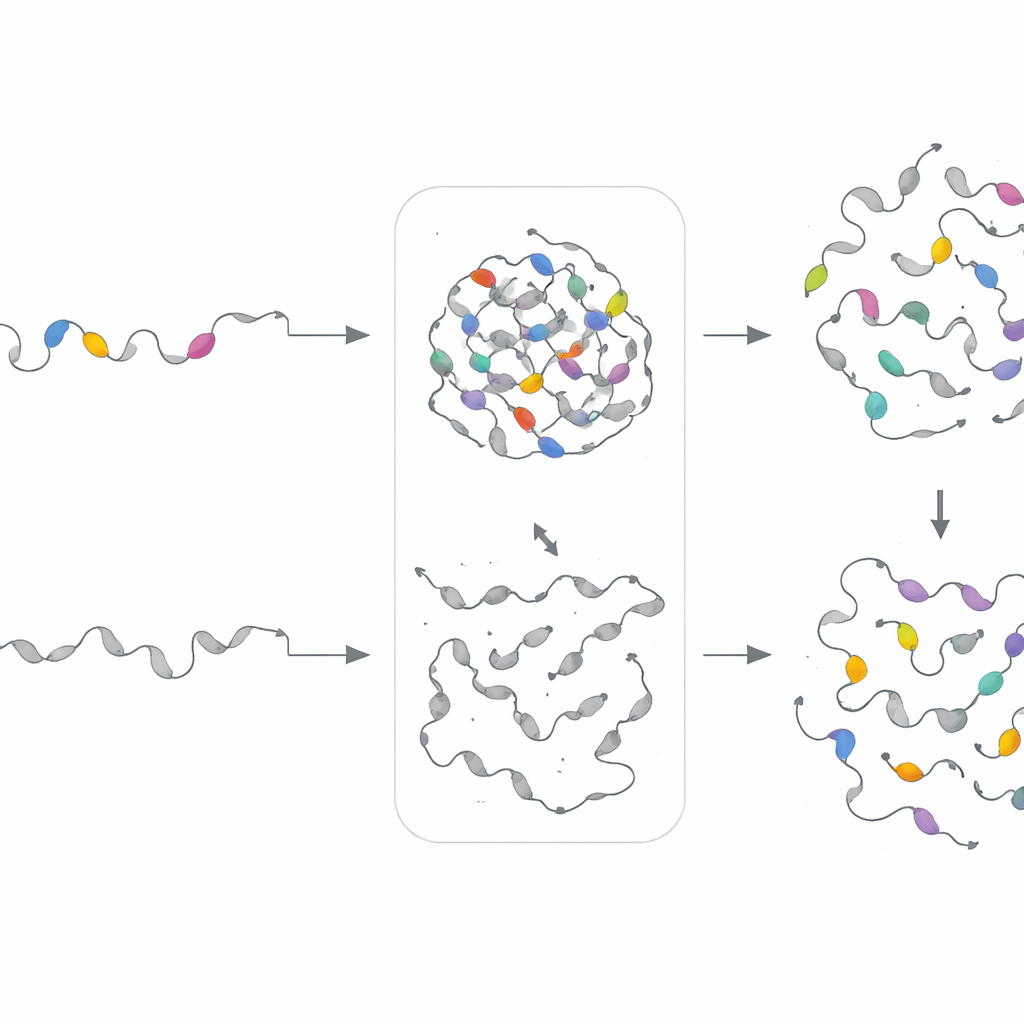
Diseñar nuevos motivos para probar las reglas
Para verificar si las “recetas” de motivos—más que secuencias exactas—gobiernan el comportamiento de las gotas, el equipo construyó modelos generativos separados para cada clúster de motivos. Estos autoencoders variacionales aprendieron los patrones estadísticos de un clúster dado y luego produjeron nuevas secuencias artificiales que compartían las mismas huellas composicionales pero distinto orden exacto. Los investigadores intercambiaron experimentalmente estos motivos sintéticos en proteínas donde los segmentos originales habían sido eliminados. De manera notable, en 18 de 21 casos, los motivos diseñados restauraron la separación de fases en células, a veces incluso ajustando la velocidad o la densidad de formación de gotas. Esto demuestra que PhaSeMotif captura reglas de diseño subyacentes que pueden reutilizarse para construir o reparar regiones formadoras de gotas.
Qué significa esto para la biología y la enfermedad
Al vincular aprendizaje profundo interpretable con diseño generativo y pruebas celulares directas, este trabajo convierte la vaga noción de “regiones desordenadas formadoras de gotas” en un conjunto concreto de motivos cortos y composables. Para quienes no son expertos, la conclusión es que los científicos pueden ahora leer y escribir los pequeños segmentos proteicos que controlan cómo los condensados celulares se ensamblan, se mezclan y fallan. Esto abre la puerta a un descubrimiento más rápido de mutaciones causantes de enfermedad en estos segmentos, estudios mecanicistas más claros sobre cómo los condensados organizan la fisiología celular y, eventualmente, la ingeniería racional de proteínas que dirijan gotas con fines terapéuticos o de biología sintética.
Cita: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Palabras clave: condensados biomoleculares, proteínas intrínsecamente desordenadas, separación de fases, aprendizaje profundo, motivos proteicos