Clear Sky Science · es
Hepatocitos reprogramados funcionalmente por células de cáncer colorrectal con alta expresión de KIAA1199 favorecen la acumulación de neutrófilos Egr1+ pro‑metastásicos
Cuando el cáncer de colon apunta al hígado
La mayoría de la gente imagina que el cáncer se disemina porque células errantes se desprenden y llegan a nuevos órganos. Este estudio revela una historia más inquietante: los tumores colorrectales pueden reconfigurar silenciosamente el hígado mucho antes de que lleguen células cancerosas, creando un “suelo” favorable en el que futuros tumores pueden arraigar con facilidad. Comprender esta fase de preparación oculta podría abrir la puerta a tratamientos que detengan las metástasis hepáticas —la principal causa de muerte en el cáncer colorrectal— antes de que comiencen.
Una puesta en marcha sigilosa antes de la llegada del tumor
El cáncer colorrectal suele diseminarse al hígado, aunque sólo algunos tumores lo hacen de forma agresiva. Los autores se centraron en una molécula llamada KIAA1199, abundante en cánceres colorrectales de alto riesgo. En modelos murinos y muestras de pacientes, los tumores con alta expresión de KIAA1199 no sólo crecían más rápido; también preparaban el hígado para convertirse en un “nicho premetastásico”, un microambiente inusualmente acogedor para las células cancerosas entrantes. Incluso cuando las metástasis hepáticas se inducían experimentalmente desde una fuente separada, los animales con tumores de colon KIAA1199‑altos desarrollaban muchas más metástasis hepáticas y morían antes. Esto demostró que señales del tumor primario, no sólo células cancerosas desplazadas, estaban remodelando el hígado por anticipado.
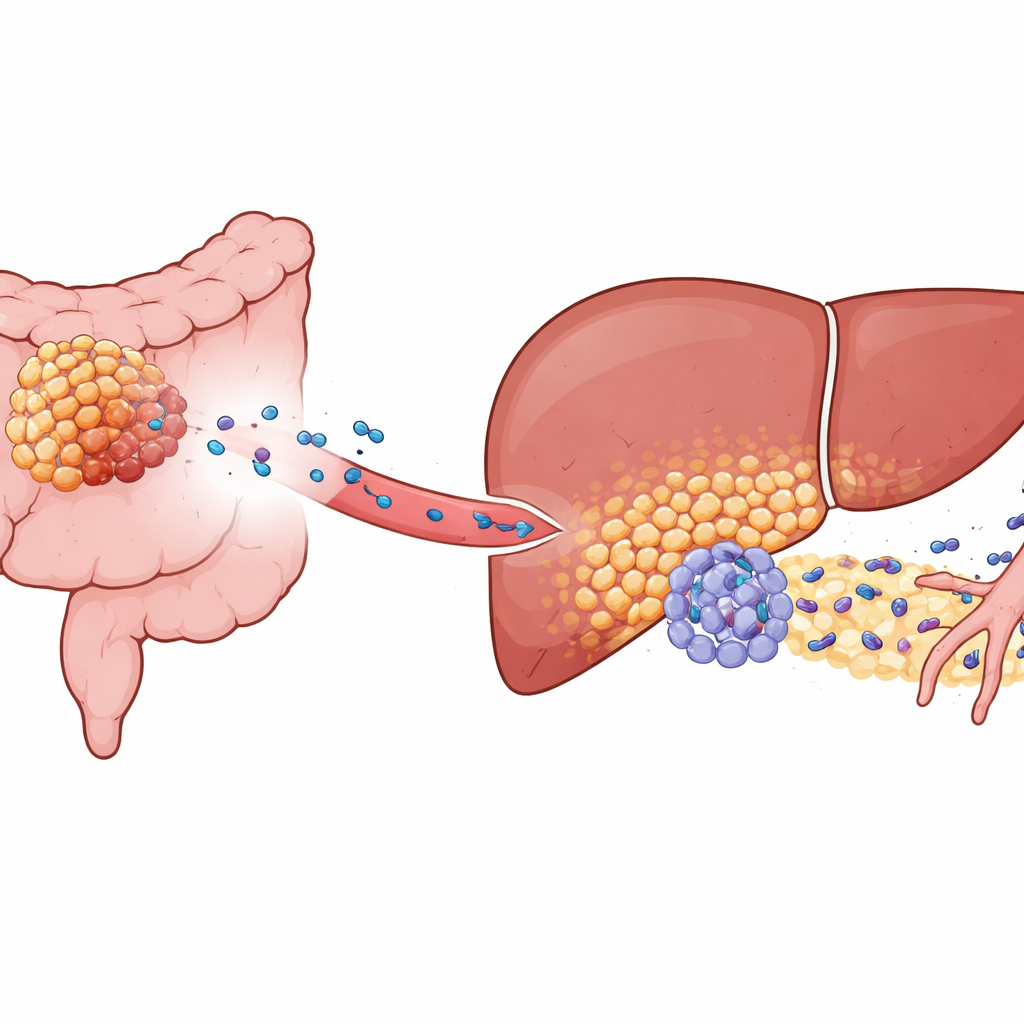
Las células hepáticas reprogramadas se convierten en cómplices del tumor
Indagando más a fondo, los investigadores usaron secuenciación unicelular y mapeo espacial para examinar el tejido hepático a alta resolución. Descubrieron un subconjunto distinto de hepatocitos —normalmente las células funcionales del hígado— que habían sido “reprogramados funcionalmente”. Estas células aparecían sólo cuando estaban presentes tumores KIAA1199‑altos. En lugar de gestionar discretamente el metabolismo, los hepatocitos alterados cambiaron a un estilo metabólico más parecido al maligno y redujeron la actividad de un regulador protector llamado PPARγ, que normalmente ayuda a controlar la inflamación y las respuestas al estrés. Con PPARγ suprimido, estos hepatocitos empezaron a producir altos niveles de una proteína llamada SAA2, que liberaban al entorno, particularmente en el borde donde el tejido hepático encuentra a las células tumorales invasoras.
Convertir a defensores corrientes en neutrófilos pro‑metastásicos
Los neutrófilos —glóbulos blancos conocidos por combatir infecciones— también se comportaron de forma extraña en este hígado preparado. Los autores identificaron un subconjunto especial con una firma “Egr1+”, denominada por un factor de transcripción que reconfigura la función de estas células. En lugar de llegar desde la sangre ya alterados, los neutrófilos parecían ser reeducados localmente por los hepatocitos reprogramados. La SAA2 liberada por los hepatocitos se unía a un receptor llamado FPR2 en los neutrófilos cercanos, activando un circuito de señalización interno PI3K‑AKT que estabilizaba la actividad de Egr1. El resultado fue un neutrófilo de mayor supervivencia y muy activo que secretaba grandes cantidades de VEGFA, un potente impulsor de la formación de nuevos vasos sanguíneos. Estos neutrófilos Egr1+ se agrupaban en la interfaz tumor‑hígado, exactamente donde brotaban vasos nuevos y frágiles.
Construir vasos sanguíneos que reciben a las células tumorales
El estudio muestra que estos neutrófilos reeducados no son meros espectadores: remodelan activamente la vasculatura hepática. En cultivo celular, los factores liberados por neutrófilos Egr1+ hicieron que las células endoteliales proliferaran, migraran y formaran estructuras tubulares semejantes a vasos nuevos. En ratones, la adición de neutrófilos Egr1+ aumentó las metástasis hepáticas y aceleró la muerte. Bloquear pasos clave de la cadena —ya sea la señal SAA2–FPR2 hacia los neutrófilos o la vía PI3K‑AKT aguas abajo— interrumpía la supervivencia de los neutrófilos y la producción de VEGFA, reduciendo el crecimiento vascular y la diseminación metastásica. De igual modo, restaurar la actividad de PPARγ en hepatocitos con el fármaco antidiabético rosiglitazona disminuyó los niveles de SAA2, frenó la aparición de neutrófilos Egr1+ y redujo drásticamente las metástasis hepáticas en modelos preclínicos.
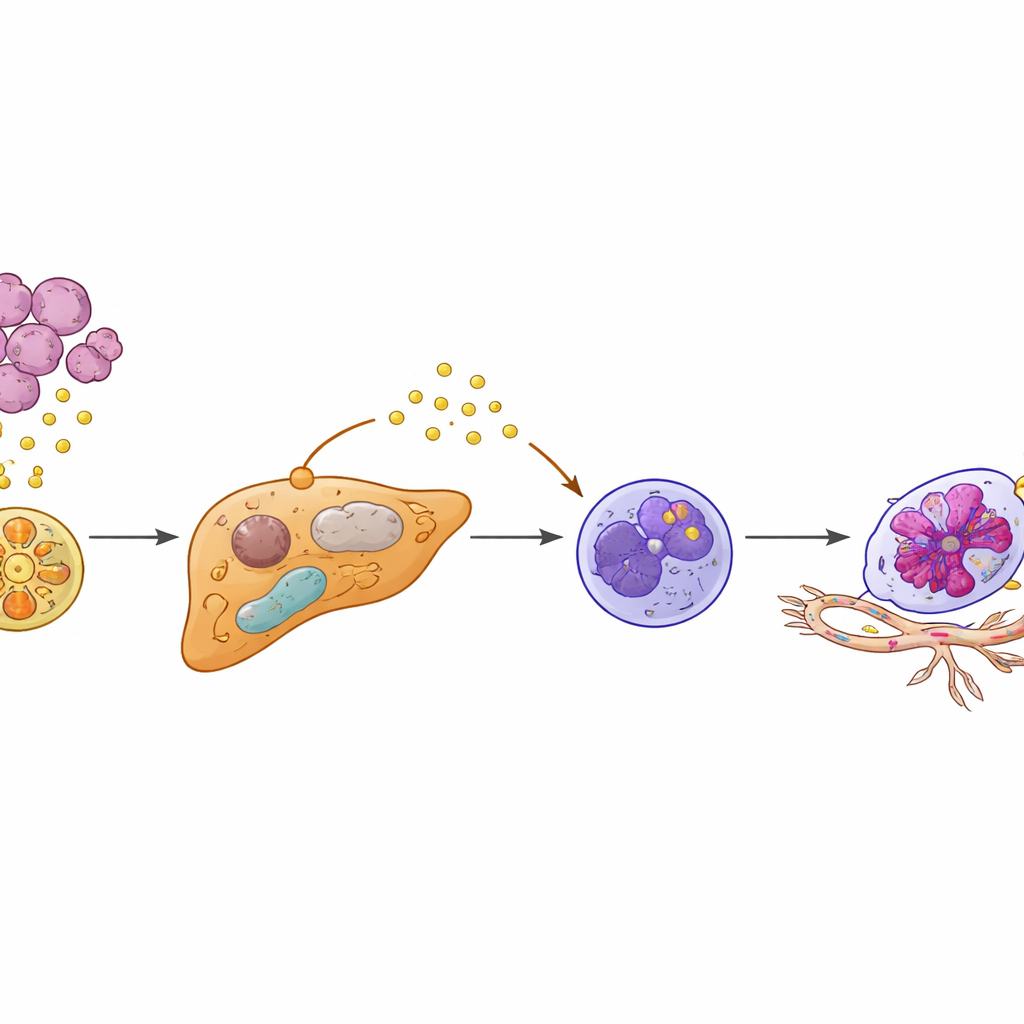
Del mecanismo a la predicción y la prevención
Dado que KIAA1199 en los tumores y SAA2 en el hígado ocupan posiciones altas en esta cascada, los autores probaron si estas proteínas podrían ayudar a identificar a pacientes con alto riesgo de metástasis hepática. En varias cohortes de pacientes, las personas con niveles sanguíneos altos de ambos marcadores eran mucho más propensas a desarrollar metástasis hepáticas y a hacerlo antes. Una simple puntuación combinada KIAA1199–SAA2 superó a cualquiera de los marcadores por separado para predecir el riesgo y se incorporó en un “nomograma” clínico que estima la probabilidad de diseminación hepática de un paciente individual en los próximos dos años. En conjunto, los hallazgos dibujan una imagen nítida: los cánceres de colon KIAA1199‑altos envían señales en vesículas que reprograman hepatocitos, que a su vez convierten a los neutrófilos cercanos en cómplices longevos y formadores de vasos. Al apuntar a este eje KIAA1199–PPARγ/SAA2–Egr1 —mediante fármacos metabólicos, agentes moduladores del sistema inmune o ambos— podría ser posible no sólo tratar las metástasis hepáticas existentes, sino prevenir que se establezcan en primer lugar.
Cita: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Palabras clave: metástasis hepática de cáncer colorrectal, microambiente premetastásico, neutrófilos, reprogramación de hepatocitos, microambiente tumoral