Clear Sky Science · es
Reducir la metilación de la lisina 4 de la histona 3.3 en la eminencia ganglionar medial y el hipotálamo reproduce fenotipos de trastornos del neurodesarrollo
Cómo pequeñas etiquetas químicas moldean el cerebro y el cuerpo
¿Por qué algunos cambios genéticos provocan tanto problemas de aprendizaje como un crecimiento inusual, por ejemplo ser muy pequeño en la infancia pero obeso en la edad adulta? Este estudio examina pequeñas etiquetas químicas en las proteínas que empaquetan el ADN en el cerebro y muestra cómo alterarlas en solo dos regiones clave puede propagarse hasta provocar convulsiones, comportamientos similares a la ansiedad, problemas de memoria y cambios dramáticos en el tamaño corporal en ratones.
Interruptores en los atenuadores del genoma
Dentro de cada célula cerebral, el ADN está envuelto alrededor de proteínas en forma de carrete llamadas histonas. Las marcas químicas colocadas sobre estas histonas actúan como atenuadores, subiendo o bajando la expresión de grupos de genes. Una de estas marcas, añadida en un sitio llamado H3K4, está fuertemente vinculada a la activación génica. Estudios genéticos en humanos han revelado que las personas nacidas con fallos en las enzimas que añaden o quitan esta marca suelen presentar trastornos del neurodesarrollo que combinan discapacidad intelectual, epilepsia y crecimiento corporal anómalo. Sin embargo, no estaba claro qué células cerebrales son más sensibles a esta alteración y cómo su malfunción podría relacionar la excitabilidad cerebral con el metabolismo de todo el organismo.
Dirigirse a dos centros cerebrales críticos
Los investigadores diseñaron ratones en los que una versión mutante de una proteína histona (H3.3K4M) se activaba solo en células procedentes de dos regiones embrionarias del cerebro: la eminencia ganglionar medial, que produce muchas de las células inhibitorias «de freno» del cerebro, y el hipotálamo en desarrollo, que ayuda a regular el apetito, las hormonas y el equilibrio energético. Esta mutación bloquea específicamente la metilación de H3K4 sin eliminar las histonas en sí. Las pruebas confirmaron que la proteína mutante estaba ampliamente presente en las áreas objetivo y que las marcas normales de H3K4 se reducían notablemente allí, mientras que los niveles globales de histonas se mantenían estables. Este diseño imita muchas condiciones humanas en las que solo una copia de un gen relacionado con H3K4 está defectuosa, en lugar de estar completamente ausente.
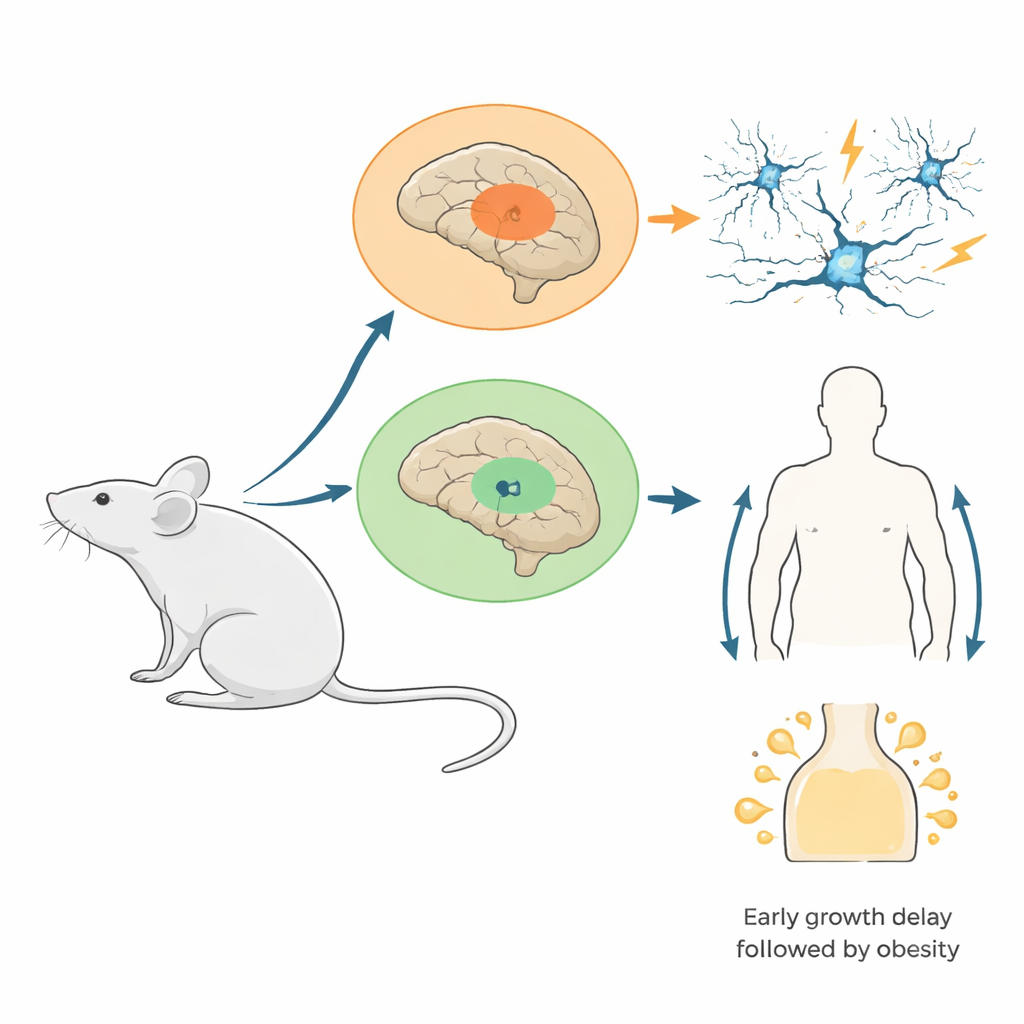
De la pérdida de células de freno a circuitos propensos a convulsiones
A medida que estos ratones crecieron, las consecuencias para los circuitos cerebrales se hicieron evidentes. Los jóvenes mutantes tenían menos interneuronas inhibitorias en la corteza y el hipocampo, especialmente un tipo de disparo rápido que normalmente mantiene los ritmos neuronales con precisión. Registros detallados mostraron que las interneuronas remanentes estaban presentes pero eran más variables en sus propiedades eléctricas, lo que sugiere que su maduración estaba alterada. Cuando se estimuló el hipocampo en cortes cerebrales, las habituales oscilaciones de alta frecuencia «gamma» —ritmos eléctricos vinculados al procesamiento de la información— eran más débiles y lentas, y aparecían eventos anormales en forma de ráfagas. En animales vivos, muchos mutantes, en particular las hembras, desarrollaron convulsiones espontáneas y fueron mucho más sensibles a convulsiones inducidas por fármacos. Temprano en el desarrollo, el equipo rastreó esta pérdida celular principalmente a una mala migración de interneuronas hacia la corteza, no a un aumento de la muerte celular ni a una reducción de la división celular.
Reprogramación de la actividad génica en células vinculadas a convulsiones
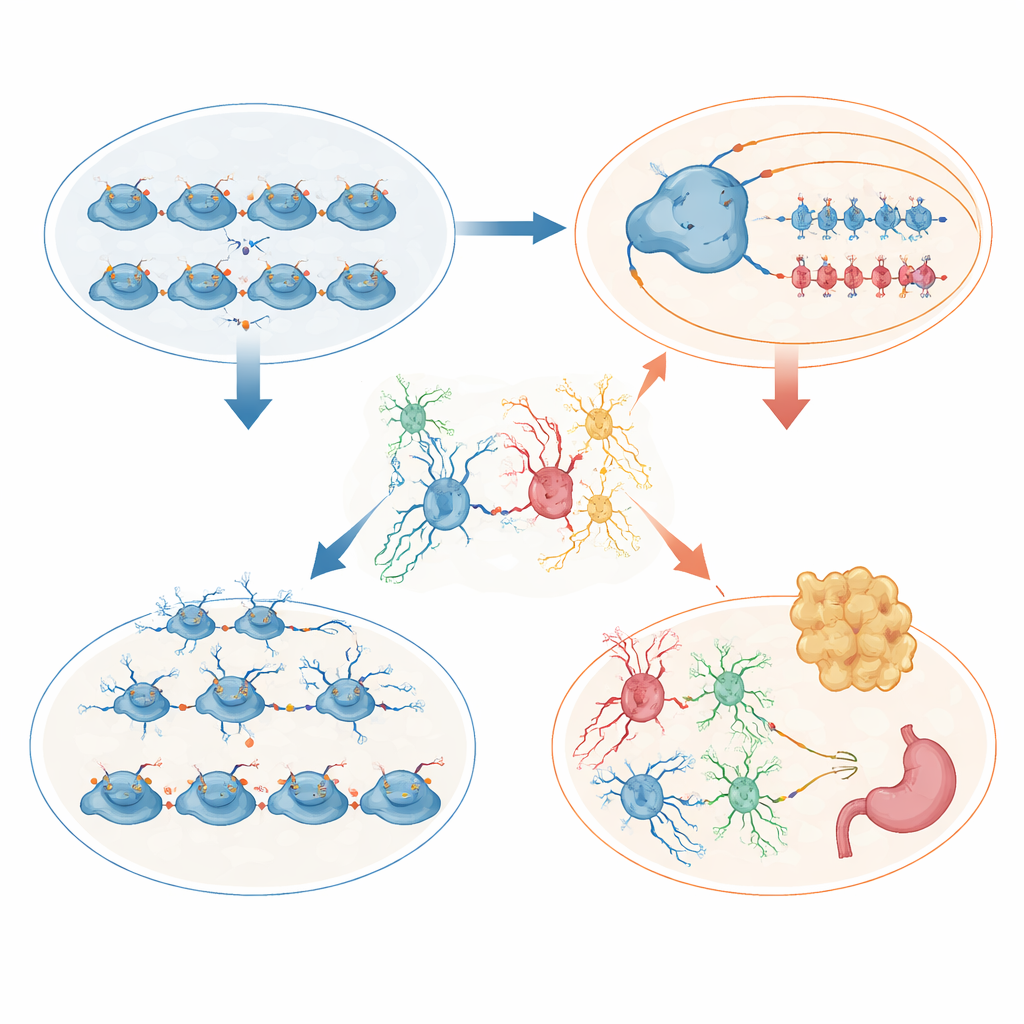
Para conectar estos cambios físicos con el control génico, el equipo utilizó secuenciación de núcleos individuales que lee tanto la actividad génica como la accesibilidad del ADN en células individuales. En la eminencia ganglionar medial embrionaria, la mayoría de los genes que cambió en los mutantes se expresaron menos, incluidos reguladores clave que dirigen a las células hacia destinos inhibitorios específicos. En las interneuronas adultas, el equilibrio entre subtipos cambió, y grupos de genes implicados en la formación de conexiones y en el control de las corrientes de potasio —los flujos que ayudan a fijar la velocidad de disparo— estuvieron mal regulados. El análisis de redes resaltó una disrupción coordinada de genes de canales de potasio que ya se sabe que influyen en la epilepsia y en los ritmos cerebrales, proporcionando un vínculo molecular directo entre la pérdida de una marca de histona, la alteración de la identidad de las interneuronas y la susceptibilidad a las convulsiones.
Desequilibrio hipotalámico y una curva de crecimiento en dos fases
El hipotálamo contó una historia complementaria centrada en el crecimiento corporal. De cachorros, los ratones mutantes eran más pequeños y una fracción considerable murió tempranamente. Los supervivientes, sin embargo, luego comieron más, acumularon grasa y desarrollaron niveles elevados de la hormona leptina, señalando obesidad y probable resistencia a la leptina. El análisis de células individuales del hipotálamo embrionario reveló más células progenitoras en división pero menos células destinadas a núcleos clave relacionados con la alimentación, especialmente regiones que normalmente detectan el estado nutricional y regulan la hormona del crecimiento. En el hipotálamo adulto, la mezcla celular se remodeló: los astrocitos aumentaron bruscamente, los oligodendrocitos disminuyeron, y células especializadas de barrera llamadas tanycitos y la glía vecina perdieron su orden en la interfase del cerebro con las hormonas y nutrientes circulantes. Estos cambios estructurales y en la expresión génica probablemente distorsionan cómo el cerebro percibe las reservas energéticas y controla el apetito.
Ecos conductuales de trastornos del neurodesarrollo humanos
El comportamiento de los ratones reflejó síntomas observados en muchos trastornos del neurodesarrollo. Mostraron mayor comportamiento similar a la ansiedad, marcha alterada, reducción del movimiento espontáneo en el hogar y un rendimiento pobre en tareas que evalúan memoria, reconocimiento de objetos y filtrado de sonidos de sobresalto. Algunas pruebas revelaron acciones más impulsivas. En múltiples medidas, las hembras tendieron a verse más afectadas que los machos, lo que sugiere que los sistemas hormonales y la regulación génica dependientes del sexo pueden interactuar con las marcas de histonas para moldear la vulnerabilidad.
Qué significa esto para la salud humana
En conjunto, los hallazgos muestran que debilitar un conjunto de marcas de histonas en solo dos centros cerebrales embrionarios es suficiente para reproducir una amplia constelación de problemas: menos «frenos» inhibitorios, redes cerebrales inestables, convulsiones, circuitos de alimentación alterados y crecimiento corporal anómalo. Para los no especialistas, el mensaje clave es que las marcas epigenéticas como la metilación de H3K4 no son añadidos vagos sino diales de control precisos que ayudan a que las células cerebrales en desarrollo se conviertan en el tipo correcto, en el lugar correcto y en el momento adecuado. Cuando esos diales están mal ajustados, como en muchos síndromes genéticos raros, el resultado puede ser una combinación estrechamente vinculada de síntomas cognitivos, conductuales y metabólicos. Comprender estas raíces compartidas podría, en última instancia, orientar terapias que corrijan no solo un síntoma, como las convulsiones o la obesidad, sino el sistema interconectado que los origina.
Cita: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Palabras clave: epigenética, interneuronas, hipotálamo, convulsiones, obesidad