Clear Sky Science · es
Separar la separación de fases y la fibrilización preserva la actividad de los condensados biomoleculares
Por qué importa para la salud cerebral
Muchas enfermedades cerebrales, incluida la enfermedad de Alzheimer, implican proteínas que con el tiempo se agrupan en enredos duros y fibrosos. Esas mismas proteínas también pueden formar estructuras más blandas, parecidas a gotas, dentro de las células que ayudan a organizar la bioquímica, algo así como pequeñas estaciones de trabajo líquidas. Este estudio plantea una pregunta crucial: ¿podemos detener el endurecimiento dañino de estas gotas en fibras sin destruir su función útil cotidiana? Los autores muestran que un metabolito celular común, el aminoácido L-arginina, puede hacer exactamente eso para una proteína clave relacionada con el Alzheimer llamada Tau.
De proteína libre a diminutas gotas
Dentro de las células, ciertas proteínas no siempre permanecen uniformemente mezcladas en el fluido intracelular. En su lugar, pueden agruparse en gotas, llamadas condensados biomoleculares, que se comportan como geles muy blandos o líquidos viscosos. El equipo se centró en Tau, una proteína que normalmente ayuda a construir y estabilizar los microtúbulos—filamentos huecos que actúan como vías dentro de las neuronas. Tau también es conocida por formar fibrillas amiloides rígidas, las fibras presentes en los enredos que caracterizan muchas enfermedades neurodegenerativas. Para estudiar cómo evolucionan las gotas de Tau con el tiempo, los investigadores diseñaron una versión de la proteína, llamada SynTag-Tau, que forma condensados activos que envejecen hasta convertirse en fibrillas amiloides en una escala de tiempo experimentalmente conveniente, sin aditivos agresivos.
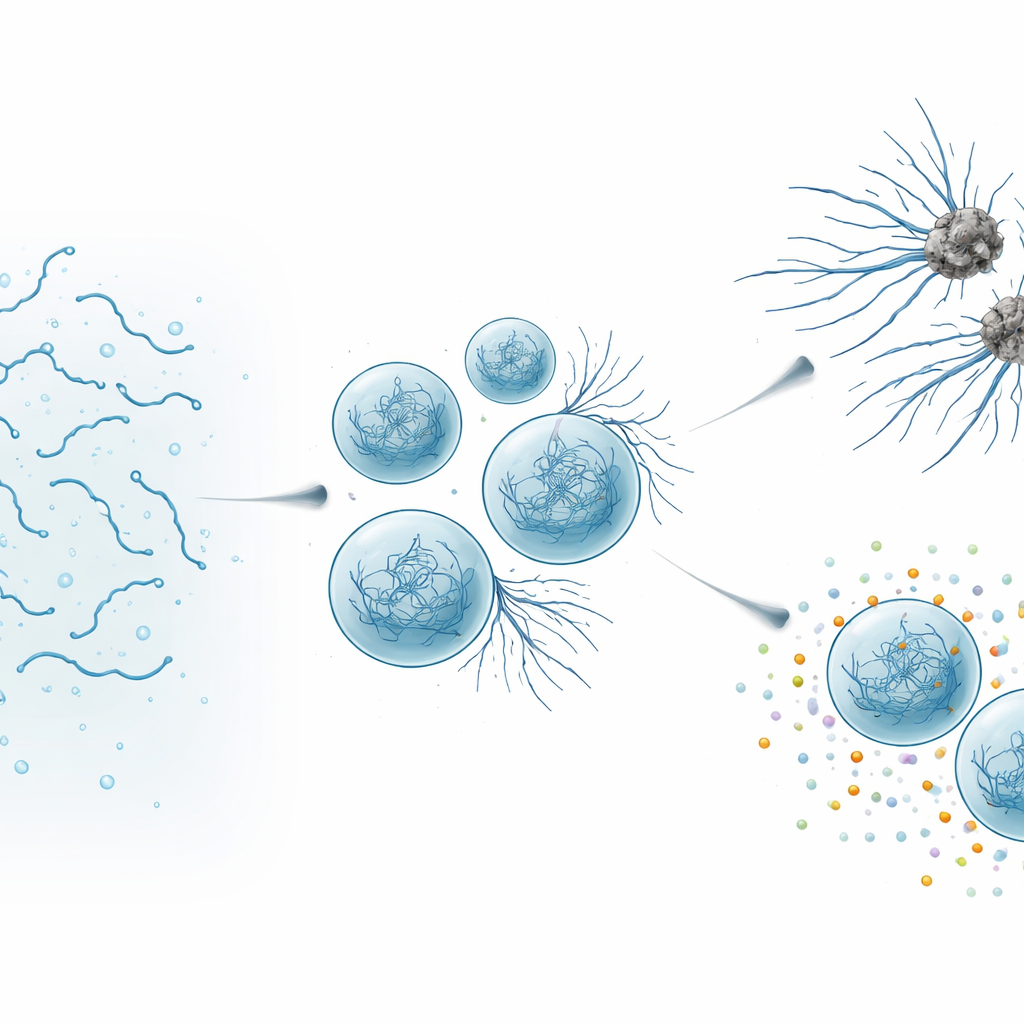
Cuando las gotas útiles se vuelven dañinas
Usando microscopía de alta resolución y mediciones biofísicas, los autores observaron cómo cambiaban las gotas de SynTag-Tau a lo largo de horas. Las gotas recién formadas se comportaban como líquidos: se fusionaban con facilidad, sus moléculas se movían rápidamente y no había indicios de estructura ordenada. Con el tiempo, las gotas se ralentizaron y se endurecieron, y delgadas fibras comenzaron a brotar de sus superficies hacia la solución circundante. Métodos ópticos sensibles mostraron que estas fibras contenían la arquitectura estrechamente empacada de “cross–beta” típica del amiloide. Importante, la interfaz—el límite entre la gota densa y el fluido circundante—actuó como un punto caliente donde las fibrillas aparecieron primero. A medida que las gotas envejecían y brotaban más fibras, la función normal de Tau se vio afectada: los condensados empeoraron en reclutar tubulina, el bloque de construcción de los microtúbulos, y finalmente perdieron por completo su capacidad para soportar el ensamblaje de microtúbulos.
Pequeñas moléculas que inclinan la balanza
Los investigadores se preguntaron entonces si metabolitos simples podían ralentizar o prevenir esta transición de líquido a fibra mientras dejaban intactas las gotas. Al cribar varias pequeñas moléculas de origen natural, encontraron que los aminoácidos cargados positivamente L-arginina y L-lisina retrasaban fuertemente o bloqueaban la formación de fibrillas amiloides a partir de las gotas de SynTag-Tau, sin impedir la formación de gotas a concentraciones realistas de baja escala milimolar. En contraste, aminoácidos con carga negativa como el glutamato y el aspartato aceleraron la formación de fibrillas, y químicos generales que alteran proteínas o bien no ayudaron o perturbaron las propias gotas. Un análogo fluorescente de L-arginina reveló que esta molécula prefiere situarse dentro de los condensados de Tau en lugar de fuera, lo que sugiere que actúa donde más se necesita.
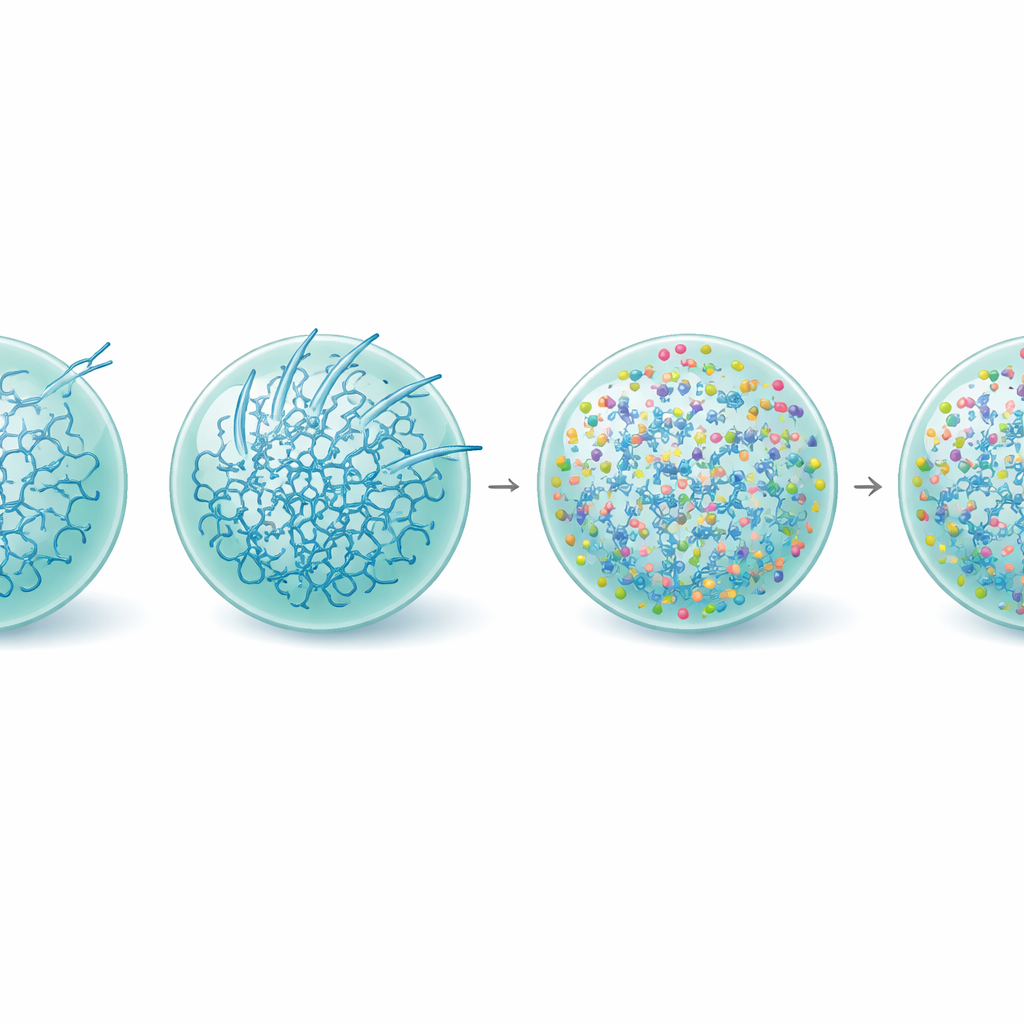
Endurecer la gota, salvar la función
Indagando más, el equipo examinó cómo la L-arginina remodela la vida interna de las gotas de Tau. Mediciones de la estructura proteica mostraron que, con L-arginina presente, la fracción de moléculas Tau que adoptan las formas rígidas ricas en beta asociadas al amiloide se redujo, incluso en gotas más antiguas. La nanorheología basada en vídeo—seguimiento del movimiento de pequeñas partículas dentro de los condensados—reveló que la L-arginina en realidad hacía que las gotas de Tau fueran más viscoelásticas, es decir, que su red interna se volviera más fuerte e interconectada manteniéndose con comportamiento similar al de un fluido. Este fortalecimiento parece mantener el sistema en un estado metaestable y funcional y eleva la barrera energética para la formación de fibrillas, particularmente en la superficie de la gota. En consonancia con esto, los condensados tratados con L-arginina continuaron reclutando tubulina de forma homogénea y soportaron el crecimiento de microtúbulos mucho después de que las gotas no tratadas se hubieran vuelto inactivas.
Qué significa esto para futuras terapias
El trabajo demuestra que las fuerzas que impulsan la formación de gotas proteicas y las que impulsan la formación de fibras dañinas están relacionadas pero son separables. Al ajustar la química dentro de los condensados con un metabolito como la L-arginina, es posible preservar el estado beneficioso y líquido mientras se retrasa o previene la transición a fibras amiloides vinculadas a la enfermedad. Aunque este estudio utiliza un sistema Tau especialmente diseñado in vitro, ofrece una prueba de principio: pequeñas moléculas que fortalezcan selectivamente la estabilidad de los condensados podrían, algún día, ayudar a proteger las células del acumulamiento gradual de agregados proteicos tóxicos sin bloquear los papeles organizativos normales de los condensados biomoleculares.
Cita: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Palabras clave: Proteína Tau, condensados biomoleculares, fibrillas amiloides, L-arginina, neurodegeneración