Clear Sky Science · es
Variantes de FOXJ3 asociadas a epilepsia vinculan un programa transcripcional de la vía PTEN-mTOR con la especificación neuronal y la laminación cortical
Cuando el cableado cerebral se desvía ligeramente
La epilepsia suele comenzar en la infancia, pero en muchos pacientes jóvenes los médicos no detectan nada claramente anómalo en las exploraciones cerebrales. Este estudio aborda una causa oculta: pequeños cambios en un gen llamado FOXJ3 que, de forma discreta, remodelan cómo se construye la capa externa del cerebro, la corteza. Siguiendo la actividad de este gen en familias con epilepsia focal y en cerebros de ratón en desarrollo, los investigadores muestran cómo fallos tempranos en el nacimiento, el movimiento y la estratificación celular pueden terminar provocando convulsiones.
Una malformación sutil detrás de convulsiones difíciles de tratar
Muchos niños con epilepsia focal resistente a medicamentos presentan una condición llamada displasia cortical focal (DCF), en la que parches de la corteza están malformados. Estas regiones contienen neuronas desplazadas y anormalmente grandes y son una causa frecuente de que los fármacos no controlen las crisis. Sin embargo, la causa molecular de la DCF a menudo se desconoce y la RM estándar puede pasar por alto defectos pequeños o superficiales. Los autores empezaron con una familia en la que varios miembros tenían epilepsia focal y signos de DCF. Un análisis genómico minucioso señaló cambios raros en FOXJ3, un gen no vinculado previamente con epilepsia. Casos adicionales extraídos de grandes bases de datos genéticos revelaron más individuos con variantes inusuales de FOXJ3 y convulsiones focales, lo que sugiere que este gen podría ser un actor recurrente en estos trastornos.
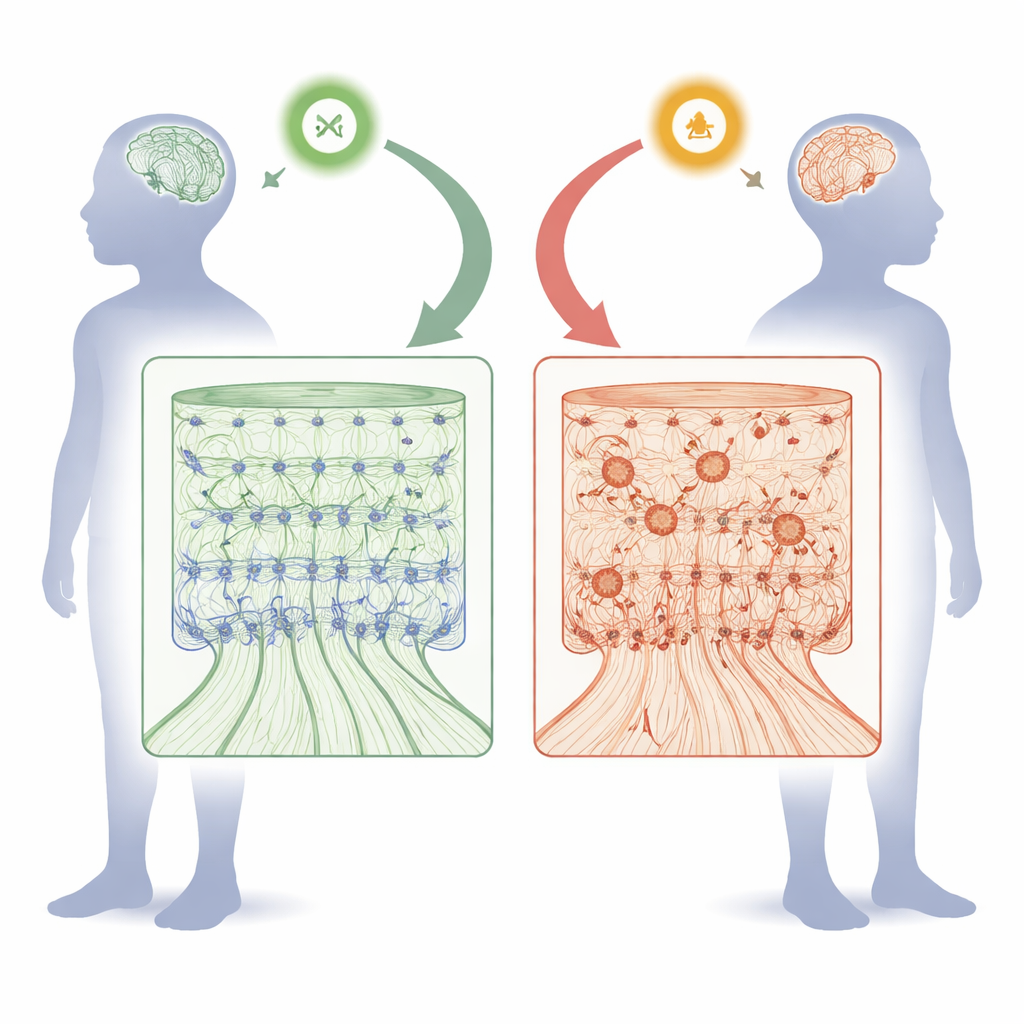
Cómo FOXJ3 ayuda a moldear la superficie pensante del cerebro
Durante el desarrollo fetal, la corteza se monta como un edificio de muchas plantas. Células con rasgos de progenitores que recubren la superficie interna del cerebro se dividen y luego envían neuronas recién nacidas hacia afuera a lo largo de “andamios” radiales para formar seis capas ordenadas. El equipo descubrió que FOXJ3 está activo tanto en estos progenitores como en las neuronas jóvenes, pero su actividad en los progenitores cae naturalmente tras un punto temporal específico a mitad de la gestación. Usando herramientas de silenciamiento génico en embriones de ratón, los investigadores redujeron los niveles de Foxj3 en distintas etapas y observaron lo que ocurría. La pérdida temprana de Foxj3 provocó que las neuronas recién formadas migraran más despacio y se asentaran en capas equivocadas. Células que debían convertirse en neuronas de capas profundas adoptaron en cambio identidades propias de capas superiores, y se produjeron en exceso neuronas proyectivas comisurales, que conectan los dos hemisferios cerebrales. Más tarde en el desarrollo, sin embargo, reducir Foxj3 tuvo efectos mucho más leves, lo que demuestra que su función es altamente dependiente del momento.
Mantener el equilibrio entre división celular y crecimiento
Para entender por qué FOXJ3 tiene tanta influencia, los investigadores combinaron varios enfoques a gran escala. Cartografiaron dónde se une FOXJ3 al ADN y qué genes están activos en miles de células corticales individuales. Esto señaló con fuerza a genes que gobiernan el ciclo celular y el crecimiento cerebral, en especial PTEN, un freno importante sobre una vía de crecimiento conocida como mTOR. En las células progenitoras, la unión de FOXJ3 potenció la actividad de PTEN, lo que a su vez ayudó a las células a salir del ciclo de división, transformarse en neuronas y migrar hacia afuera de forma ordenada. Cuando se redujo Foxj3, más progenitores permanecieron en estado proliferativo, menos salieron del ciclo a tiempo y la migración se estancó en zonas intermedias. De forma crucial, restaurar los niveles de PTEN en cerebros deficientes en Foxj3 revirtió en gran medida los problemas de migración, estratificación y destino celular, mientras que potenciar otro regulador del crecimiento, TSC1, no lo hizo. Esto sitúa a PTEN en el centro del control que ejerce FOXJ3 sobre la construcción cortical.
De vías desreguladas a neuronas agrandadas
El equipo preguntó después cómo se comportan las variantes de FOXJ3 semejantes a las encontradas en pacientes. Una versión asociada a enfermedad de FOXJ3 no logró aumentar los niveles de PTEN y permitió que la vía mTOR se volviera hiperactiva, como mostró un incremento en la fosforilación de una proteína clave relacionada con el crecimiento. En ratones adolescentes diseñados para expresar esta forma mutante en la corteza en desarrollo, las neuronas más tarde aparecieron visiblemente hinchadas, con somas y perímetros mayores, imitando las células dismórficas observadas en la DCF humana. Aun así, la proteína mutante seguía alcanzando correctamente el núcleo, lo que indica que el problema radica en una regulación génica defectuosa y no en una mala localización. En conjunto, estos hallazgos vinculan las mutaciones de FOXJ3 con una cascada de eventos —menos PTEN, más señalización mTOR, retraso en la salida del ciclo celular, migración desordenada y neuronas hipertróficas— que pueden preparar el terreno para redes epilépticas.
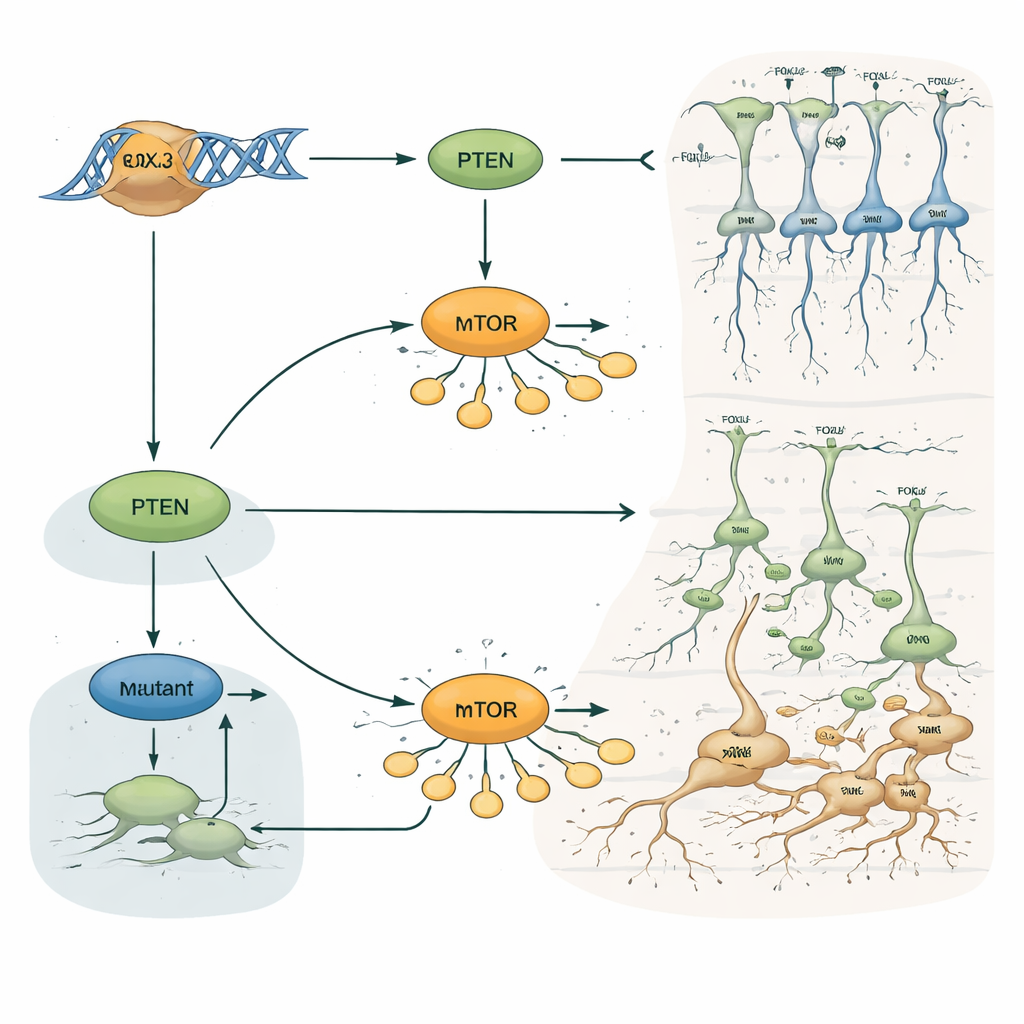
Por qué esto importa para la epilepsia y las lesiones cerebrales ocultas
Para un lector no especialista, el mensaje clave es que un único factor de transcripción, FOXJ3, contribuye a decidir cuándo y dónde nacen las neuronas corticales, cómo se desplazan y en qué capa terminan. Al actuar a través de la vía de crecimiento PTEN–mTOR, FOXJ3 mantiene la construcción del cerebro en su calendario. Cambios raros en este gen pueden inclinar ese equilibrio, provocando pequeños parches de corteza con un cableado y una estratificación incorrectos, incluso cuando las resonancias magnéticas parecen normales. Este trabajo no solo propone a FOXJ3 como una nueva causa genética de displasia cortical focal y epilepsia, sino que también ilustra cómo variaciones sutiles en el desarrollo cerebral temprano pueden repercutir décadas después como convulsiones difíciles de tratar.
Cita: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Palabras clave: displasia cortical focal, gen FOXJ3, vía PTEN mTOR, desarrollo cortical, epilepsia focal