Clear Sky Science · es
Almacenamiento de sodio mejorado en carbono duro mediante un electrolito de co-intercalación de solvente que permite celdas pouch de nivel Ah a bajas temperaturas
Por qué importan las baterías resistentes al frío
Desde coches eléctricos en climas nevados hasta sensores en el Ártico profundo, muchos dispositivos modernos necesitan baterías que sigan funcionando en frío. Las baterías de litio y sodio actuales a menudo pierden potencia o fallan por completo a temperaturas muy bajas porque su química interna se ralentiza. Este estudio explora una nueva forma de construir baterías de ion-sodio —empleando un líquido especialmente diseñado dentro de la batería— para que puedan almacenar y suministrar energía de manera fiable incluso a temperaturas tan bajas como −50 °C.
El desafío de las baterías que se congelan
Las baterías almacenan energía haciendo viajar átomos cargados, llamados iones, entre dos electrodos sólidos a través de un electrolito líquido. En las baterías de ion-sodio, los iones sodio deben atravesar una delgada película superficial e incorporarse a un electrodo negativo a base de carbono conocido como carbono duro. A bajas temperaturas, suceden dos problemas: los iones se mueven más despacio a través del líquido y tienen dificultad para desprender las moléculas de solvente que los rodean antes de entrar en el carbono duro. Al mismo tiempo, la película protectora superficial —llamada interfase sólido-electrolito— tiende a engrosarse y volverse más resistiva en el frío. Todo ello dificulta el movimiento de los iones sodio, por lo que la batería puede entregar mucha menos energía cuando más se necesita.
Una nueva mezcla líquida para facilitar el viaje de los iones
Los investigadores abordaron este problema rediseñando el electrolito de modo que los iones sodio ya no tuvieran que desprender completamente su capa de solvente antes de entrar en el carbono duro. Mezclaron dos solventes a base de éter: dietilenglicol dimetil éter (G2), que se adhiere fuertemente a los iones sodio y favorece un movimiento iónico rápido, y 2-metiloxolano (MO), un líquido menos polar que permanece fluido a temperaturas muy bajas. En el electrolito resultante de “co-intercalación”, los iones sodio se coordinan principalmente con G2, mientras que el MO actúa en gran medida como un solvente libre y no vinculante que ayuda a mantener la mezcla líquida hasta −50 °C. Simulaciones por ordenador y medidas espectroscópicas mostraron que esta mezcla forma una estructura estable en la que los iones sodio y G2 viajan juntos como un pequeño racimo.
Permitir que los iones entren en el carbono sin despojarse
En lugar de obligar a los iones sodio a desprender su capa de solvente en la superficie del electrodo, el nuevo electrolito permite que los racimos sodio–G2 se deslicen directamente a través de la película superficial e ingresen en los espacios en capas del carbono duro. Este proceso, llamado co-intercalación de solvente, evita el lento paso de “despojarse” que normalmente limita el rendimiento en frío. Pruebas microscópicas y espectroscópicas revelaron que la película superficial formada con este electrolito es más delgada y rica en compuestos inorgánicos que en los sistemas convencionales. Esa combinación protege el electrodo mientras permite que los iones lo atraviesen rápidamente. Mediciones de difusión iónica y resistencia eléctrica confirmaron que los iones se mueven más rápido dentro del carbono y a través de la interfaz, especialmente a bajas temperaturas.
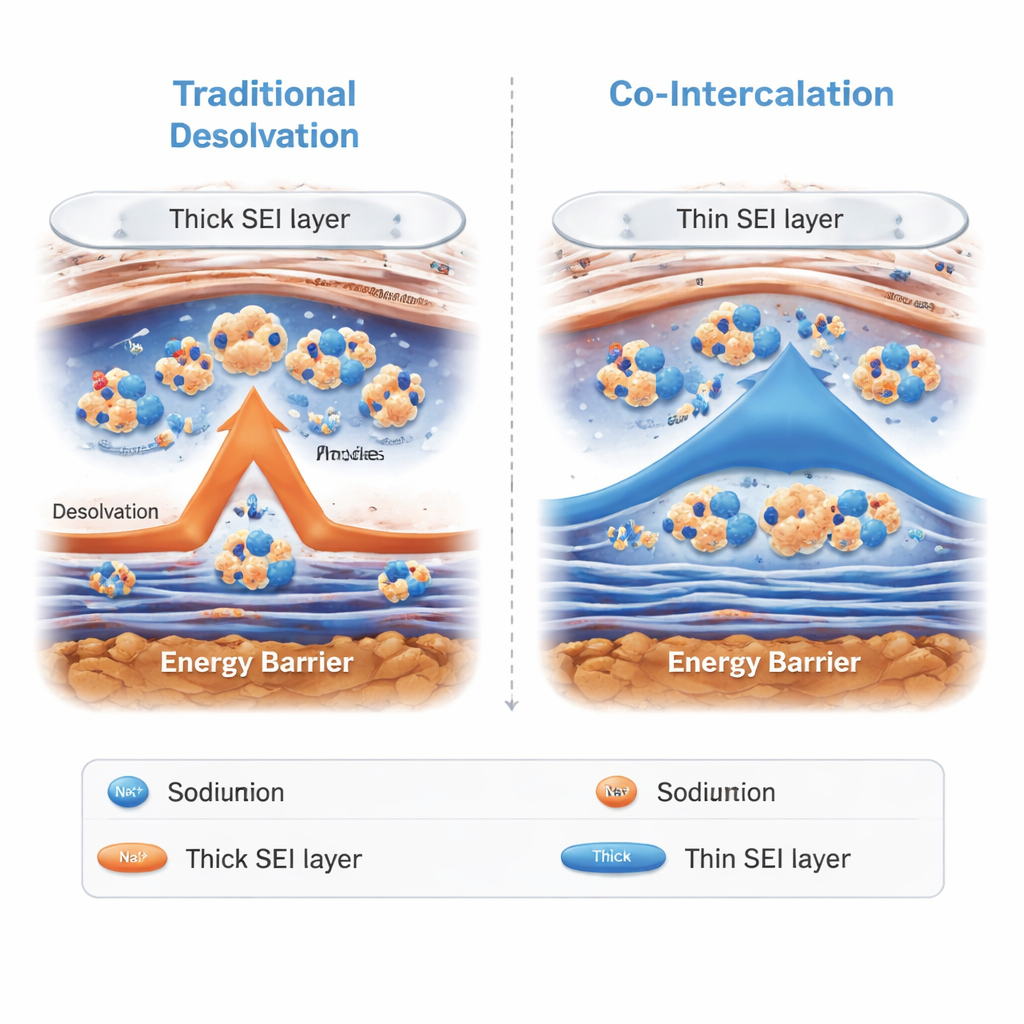
Alto rendimiento incluso a −50 °C
Cuando el equipo probó celdas de tamaño coin usando carbono duro y el nuevo electrolito, encontraron que las baterías mantenían alta capacidad y eficiencia desde la temperatura ambiente hasta −50 °C. A −50 °C, el electrodo de carbono duro aún ofrecía aproximadamente el 80% de su eficiencia de carga inicial y mantuvo más del 90% de su capacidad después de 200 ciclos de carga y descarga. Yendo más allá de las celdas pequeñas, los investigadores construyeron celdas pouch —baterías planas similares a las de la electrónica de consumo— con una capacidad de alrededor de 1,2 amperios-hora. Estas baterías completas de ion-sodio alcanzaron una energía específica de 163 vatios-hora por kilogramo a temperatura ambiente y 107 vatios-hora por kilogramo a −50 °C, mientras seguían alimentando luces LED durante más de 10 horas en una cámara a −50 °C.
Qué significa esto para las baterías en climas fríos del futuro
Para el público general, el mensaje clave es que los autores encontraron una forma de permitir que los iones sodio conserven su útil capa de solvente al entrar en el electrodo de carbono de la batería. Al diseñar un electrolito que permanece líquido en el frío y forma una película superficial delgada y favorable a los iones, eliminaron un importante cuello de botella en el rendimiento a baja temperatura. Este enfoque podría ayudar a que las baterías de ion-sodio —una alternativa más barata a las de ion-litio— sean más prácticas para su uso en climas invernales, regiones de gran altitud y otros entornos duros donde se necesita con urgencia almacenamiento de energía fiable y asequible.
Cita: Li, M., Liu, Z., Zhao, Y. et al. Enhanced sodium storage in hard carbon via solvent co-intercalation electrolyte enabling Ah-level pouch cells at low temperatures. Nat Commun 17, 1478 (2026). https://doi.org/10.1038/s41467-026-69237-y
Palabras clave: baterías de ion-sodio, baterías de baja temperatura, diseño de electrolitos, <keyword>almacenamiento de energía