Clear Sky Science · es
Base molecular de la galactosilación del colágeno por GLT25D1
Cómo pequeñas etiquetas azucaradas ayudan a construir tejidos resistentes
El colágeno es la proteína más abundante del organismo y forma el armazón de la piel, los huesos, los vasos sanguíneos y muchos otros tejidos. Pero el colágeno no actúa solo: debe ser decorado con pequeñas moléculas de azúcar en puntos precisos para adquirir la resistencia y la flexibilidad adecuadas. Este estudio revela, con detalle atómico, cómo una enzima clave, GLT25D1, une un azúcar concreto al colágeno y cómo fallos en este proceso pueden provocar vasos frágiles, problemas musculares y quizá incluso cáncer.
Una mirada más cercana al cambio oculto del colágeno
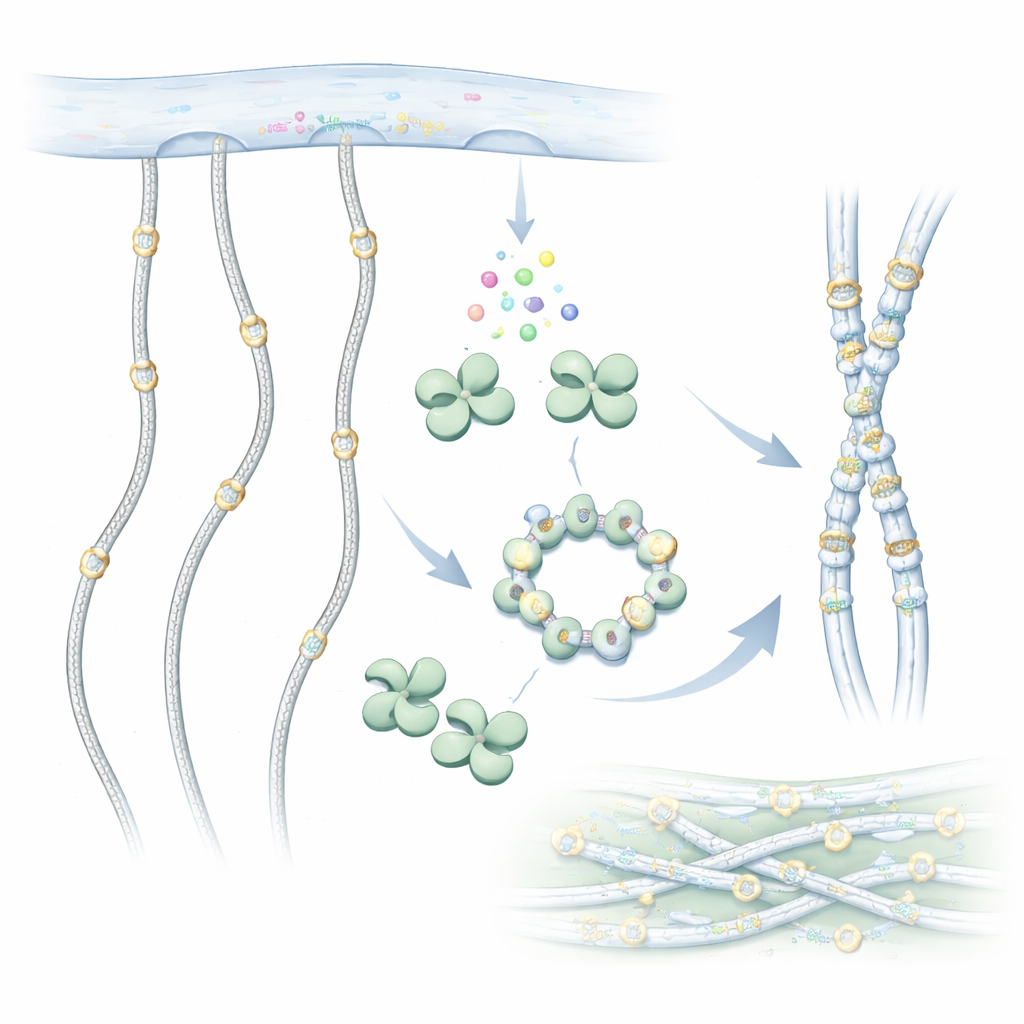
Las moléculas de colágeno son largas cadenas con forma de cuerda que se ensamblan en fibras resistentes fuera de las células. Antes de salir de la célula, sin embargo, son editadas químicamente. Una edición importante es la adición de grupos azucarados a bloques constructores especiales llamados hidroxilisinas a lo largo de la cadena de colágeno. GLT25D1 realiza el primer paso de este etiquetado azucarado, transfiriendo una galactosa desde una molécula donadora a la hidroxilisina. Esta decoración con azúcares está conservada desde animales simples hasta humanos y ayuda al colágeno a plegarse correctamente, a interactuar con las células y a resistir el desgaste.
Revelando la forma de un decorador del colágeno
Para entender cómo funciona GLT25D1, los investigadores emplearon crio‑microscopía electrónica para obtener imágenes de la enzima humana a resolución casi atómica. Descubrieron que cada molécula de GLT25D1 tiene dos lóbulos similares, ambos relacionados con un plegamiento enzimático común en proteínas transferidoras de azúcares. Estos lóbulos se emparejan para formar dímeros alargados, y tres dímeros pueden ensamblarse además en un hexámero con forma de anillo. En esos ensamblajes, los verdaderos motores —los centros catalíticos— están muy separados, una disposición que podría permitir que varios sitios de adición de azúcar funcionen a lo largo de una cadena de colágeno estirada simultáneamente.
Las partes activas: dónde ocurre realmente la transferencia de azúcar
El equipo resolvió estructuras de GLT25D1 unida tanto a su donador de azúcar como a un péptido corto tipo colágeno que contiene hidroxilisina. Este complejo ternario mostró que solo el segundo lóbulo, llamado dominio C‑terminal, realiza en realidad la química. Allí, la molécula donadora se aloja en un bolsillo estabilizado por un ion metálico, mientras el péptido se sitúa en una ranura estrecha que impone un patrón local específico: una hidroxilisina seguida inmediatamente por una glicina diminuta. Un único residuo de aspartato actúa como base química, activando el grupo hidroxilo de la hidroxilisina para que pueda atacar el azúcar y completar la transferencia. Alteraciones en cualquiera de estos aminoácidos clave reducen drásticamente o abolir la actividad, confirmando sus roles esenciales.
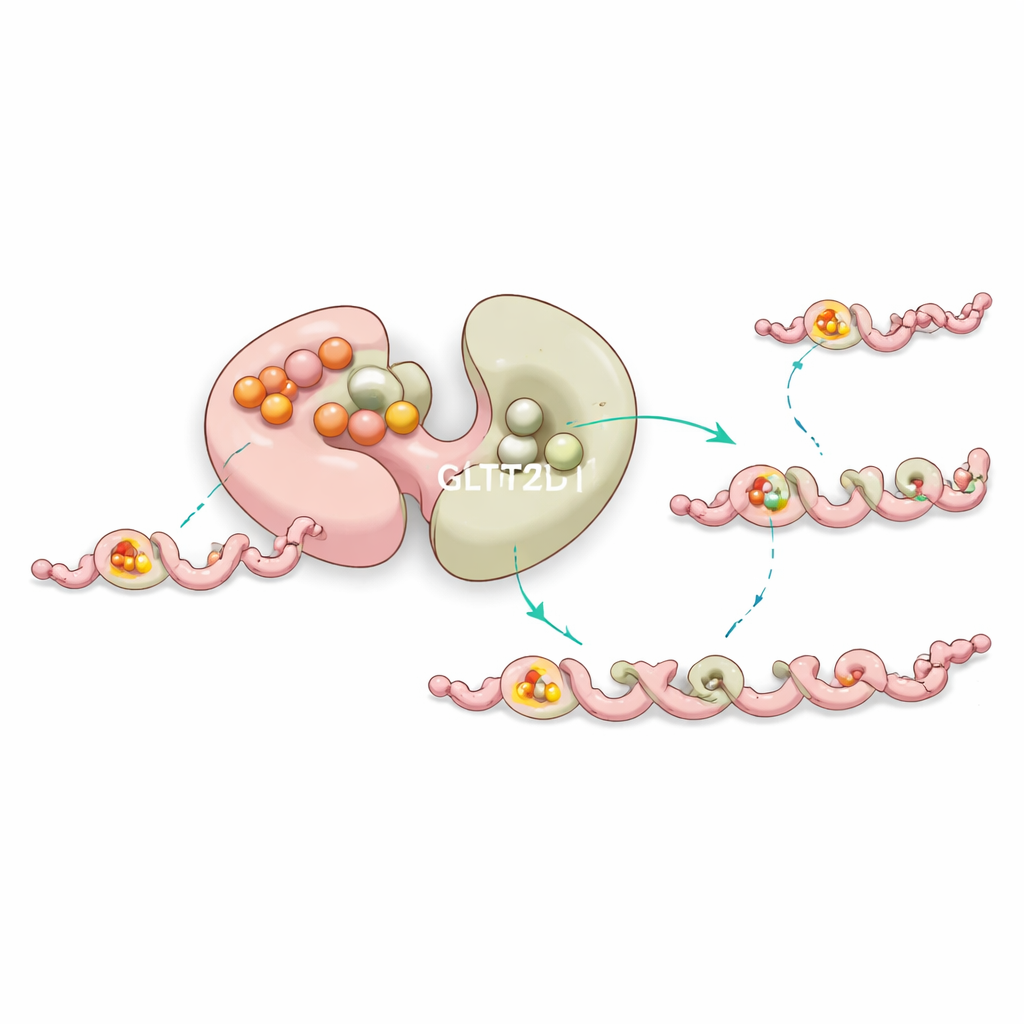
Un estabilizador incorporado y control a larga distancia
De forma curiosa, el primer lóbulo de GLT25D1 une el donador de azúcar con gran afinidad pero no realiza la transferencia. En su lugar, experimentos y simulaciones por ordenador sugieren que este sitio “silencioso” ayuda a estabilizar la enzima y ajusta sutilmente el comportamiento del lóbulo activo mediante comunicación a larga distancia dentro de la proteína. Las mutaciones cerca de este bolsillo no catalítico suelen desestabilizar la enzima o cambiar su eficiencia, lo que sugiere que la naturaleza emplea este sitio de unión adicional como una forma de control interno de calidad para mantener la modificación del colágeno en buen funcionamiento.
Cuando el decorador falla: vínculos con la enfermedad
Al mapear mutaciones derivadas de pacientes sobre su modelo estructural, los autores pudieron explicar cómo los errores en GLT25D1 conducen a enfermedades humanas. Algunas mutaciones eliminan por completo el lóbulo catalítico, otras desestabilizan el núcleo proteico y otras atacan directamente los sitios de unión del azúcar o del colágeno. Estos defectos reducen o eliminan la incorporación de azúcares al colágeno y se han vinculado a enfermedades de pequeños vasos cerebrales, problemas cognitivos y defectos musculoesqueléticos. Las mutaciones asociadas al cáncer también se agrupan en regiones cruciales, lo que sugiere que una decoración alterada del colágeno puede influir en el crecimiento y la diseminación tumoral.
Por qué esto importa para la salud y futuros tratamientos
Al trazar un plano tridimensional detallado de GLT25D1 en acción, este trabajo explica cómo se añaden etiquetas azucaradas precisas al colágeno y por qué este paso es tan importante para la integridad de los tejidos. Para el público general, el mensaje clave es que pequeños cambios químicos en el colágeno pueden tener efectos desproporcionados en los vasos sanguíneos, los huesos y posiblemente en el riesgo de cáncer. El mapa estructural de GLT25D1 ofrece ahora una guía para diagnosticar variantes dañinas y para diseñar terapias —ya sean pequeñas moléculas que estabilicen enzimas defectuosas o estrategias basadas en genes— que podrían algún día corregir los defectos de etiquetado azucarado del colágeno en su origen.
Cita: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Palabras clave: glicosilación del colágeno, GLT25D1, matriz extracelular, enfermedad vascular, estructura por crio‑EM